
Органическая химия.Казань
.pdf
20
NH2
< СH3-NH2
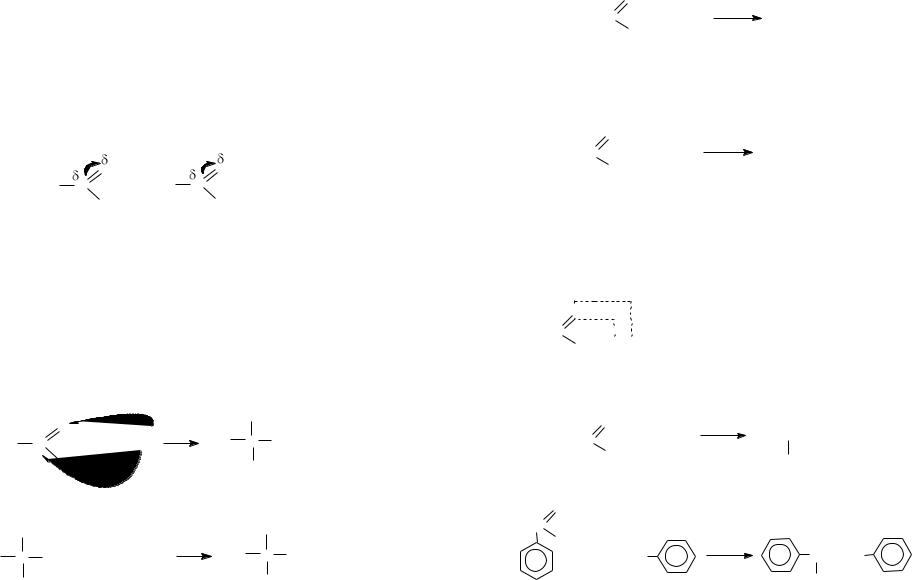
анилин метиламин В ряду ароматических аминов – п-нитроанилин, анилин, п-метиланилин,
основность увеличивается, т.к. нитрогруппа – электроноакцептор, а метильная группа – электронодонор.
NH2 |
NH2 |
NH2 |
NO2 |
|
CH3 |
|
|
|
п-нитроанилин |
анилин |
п-метиланилин |
увеличение основности
Таким образом, электронодоноры увеличивают основность, а электроноакцепторы уменьшают основность органических соединений.
Уп р а ж н е н и я
1.Расположите в ряд по последовательному уменьшению кислотности следующие соединения: пропионовая кислота, 2-хлорпропионовая кислота, 2,2- дихлорпропионовая кислота, масляная кислота, 2,2,3,3-тетрахлорпропионовая кислота, этанол, 4-этилфенол.
2.Расположите в ряд по последовательному увеличению основности следующие соединения: аммиак, п-нитроанилин, триэтиламин, этиламин, диэтиламин, анилин, метилфениламин.
3.Расположите в ряд по последовательному увеличению кислотности следующие соединения: 4-нитробензойная кислота, 2,4,6-тринитробензойная кислота, бензойная кислота, 3-метоксифенол, фенол, циклогексанол, циклогексанкарбоновая кислота.
4.Расположите в ряд по последовательному уменьшению основности следующие соединения: метиламин, трифениламин, триметиламин, диметиламин, аммиак, дифениламин, анилин.
5.Расположите в ряд по последовательному уменьшению кислотности следующие соединения: фенол, гексанол-2, гидрохинон, 2,4-динитрофенол, 2,4,6- тринитрофенол, глицерин, этанол.
6.Расположите в ряд по последовательному увеличению основности следующие соединения: гидразин, изопропиламин, анилин, триизопропиламин, аммиак, диизопропиламин, 2-аминобензальдегид.
21
7.Изобразите водородные связи между двумя молекулами N- этилацетамида.
8.Изобразите водородную связь между молекулой трибутиламина и моле-
кулой 2-метилпропантиола-1.
9.Изобразите водородную связь в молекуле 3-метил-4-оксипентанона-2.
10.Изобразите водородные связи в молекуле ксилита(пентанпента- 1,2,3,4,5-ола).
11.Из следующих соединений выберите те, для которых характерно образование межмолекулярных водородных связей и изобразите эти связи: толуол, пропанол-2, изопрен, м-ксилол, фенол, камфора, муравьиная кислота.
12.Из следующих соединений выберите те, для которых характерно образование внутримолекулярных водородных связей и изобразите эти связи: ацетон, салициловая кислота, п-крезол, анилин, 1-оксипентанон-3, метанол.
Углеводороды
Алканы
В молекулах алканов атомы С и H соединены между собой прочными ζ- связями, эти связи неполярны. При обычных условиях алканы относительно нереакционноспособны. На них не действуют концентрированные кислоты и щелочи, они не окисляются сильными окислителями – KMnO4 и K2Cr2O7. Но при высоких температурах или под действием УФ-облучения алканы могут вступать в реакции радикального замещения (SR). Легче всего происходит замещение протона при третичном атоме углерода, труднее всего при первичном.
Реакции галогенирования |
|
|
|
|
||
|
|
|
Cl |
|
||
|
|
h |
|
|
|
|
CH3-CH-CH3 + Cl2 |
CH3-C-CH3 |
+ HCl |
||||
to |
||||||
|
CH3 |
|
|
|
||
|
|
CH3 |
|
|||
2-метилпропан |
|
2-хлор-2-метилпропан |
||||
CH3-CH3 + Cl2 |
h |
CH3-CH2-Cl + HCl |
|
to |
|||
|
|
||
этан |
|
хлорэтан |
Циклоалканы
Реакционная способность циклоалканов зависит от размера цикла. Это связано с устойчивостью цикла.
Циклопропан и циклобутан проявляют двойственный характер, т.е. реагируют как алканы – с замещением атома водорода на атом галогена, и как алкены
– с присоединением молекулы галогена (при этом происходит разрыв цикла).

|
|
|
|
|
22 |
|
|
|
|
|
|
h |
|
|
+ HCl |
|
|
|
|
+ Cl2 |
|
|
Cl |
|
|
|
|
|
|
||
циклопропан |
хлорциклопропан |
||||||
|
|
|
|
FeBr3 |
|
|
|
|
|
|
|
+ Br2 |
Br-CH2-CH2-CH2-Br |
||
циклопропан |
1,3-дибромпропан |
||||||
Циклопентан и циклогексан по своим химическим свойствам аналогичны алканам. Для них более характерны реакции замещения при облучении УФсветом.
h |
Cl + HCl |
+ Cl2 |
|
циклопентан |
хлорциклопентан |
h |
Cl |
+ Cl2 |
+ HCl |
циклогексан |
хлорциклогексан |
Алкены
Химические свойства алкенов определяются наличием двойной связи. Для алкенов характерны реакции электрофильного присоединения АЕ, протекающие
сразрывом π-связи, т.к. она менее прочная, чем ζ-связь.
1.Реакция галогенирования
CH3-CH=CH2 + Br2 |
CH3-CH-CH2 |
|
|
|
|
|
Br Br |
|
пропен |
1,2-дибромпропан |
|
2. Реакция с галогеноводородами
Данная реакция протекает по правилу Марковникова: протон присоединяется к более гидрированному атому углерода.
CH3-CH=CH2 + HBr |
CH3-CH-CH3 |
|
Br |
пропен |
2-бромпропан |
23
Реакция может протекать и против правила Марковникова (протон присоединяется к менее гидрированному атому углерода) в том случае, если рядом с двойной связью стоит акцепторная группа.
|
O |
|
|
O |
CH2=CH-C |
+ HBr |
|
CH2-CH2-C |
OH |
|
OH |
|
|
|
|
Br |
|||
|
|
|
||
пропеновая кислота |
3-бромпропановая кислота |
|||
(акриловая кислота) |
|
|
|
|
3. Реакция с водой в кислых условиях
Эта реакция может протекать также по правилу и против правила Марковникова.
|
H+ |
CH3-CH-CH3 |
||||
CH3-CH=CH2 |
+ H2O |
|||||
|
|
|
||||
|
|
|
OH |
|
||
пропен |
|
пропанол-2 |
|
|||
O |
H+ |
|
|
|
O |
|
CH2=CH-C |
+ H2O |
|
CH2-CH2-C |
OH |
||
OH |
|
|
|
|||
OH |
||||||
|
|
|
||||
акриловая кислота |
3-оксипропановая кислота |
|||||
4. Реакция окисления
Алкены легко окисляются многими окислителями. При мягком окислении разрывается π-связь и образуются двухатомные спирты.
CH -CH=CH |
+ 2 KMnO |
+ 4 H O |
CH3-CH-CH2 + 2 MnO2 + 2 KOH |
||
3 |
2 |
4 |
2 |
|
|
|
|
|
|
OH OH |
|
пропен |
|
|
|
пропандиол-1,2 |
|
Эта реакция носит название мягкого окисления по Вагнеру.
Алкадиены
Наибольшее значение имеют сопряженные диены, в молекулах которых двойные связи чередуются с одинарными связями. Сопряженные диены обладают большей реакционной способностью по сравнению с другими диенами.
24
Для сопряженных диенов характерны реакции АЕ, которые протекают с образованием продуктов как 1,2-, так и 1,4-присоединения.
|
1,4 |
|
CH2-CH=CH-CH2 |
|||||
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
CH2=CH-CH=CH2 + Br2 |
|
|
Br |
|
Br |
|||
|
1,2 |
1,4-дибромбутен-2 |
||||||
|
||||||||
|
|
|
|
|
|
|
|
|
бутадиен-1,3 |
|
|
|
|
CH2-CH-CH=CH2 |
|||
|
|
|
|
|||||
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
Br |
Br |
||||
|
|
|
3,4-дибромбутен-1 |
|||||
Ароматические углеводороды (арены)
Соединения, имеющие плоский замкнутый цикл, единую сопряженную π- электронную систему, называются ароматическими. Бензол и его гомологи имеют циклическое строение и содержат в цикле три сопряженные двойные связи, поэтому являются ароматическими.
|
CH3 |
C2H5 |
|
|
CH3 |
или |
|
CH3 |
|
|
|
бензол |
толуол |
этилбензол о-ксилол |
Данные соединения вступают в такие реакции, в результате которых сохраняется ароматичность, т.е. в реакции замещения, а именно в реакции SE.
1. Реакция галогенирования
FeBr3 |
Br |
|
+ HBr |
|
+ Br2 |
|
|
||
|
|
|
||
бензол |
бромбензол |
|
||
2. Реакция нитрования |
|
|
|
|
H2SO4 |
NO2 |
|
|
|
+ HNO3 |
+ H2O |
|||
|
||||
бензол |
нитробензол |
|
||
3. Реакция сульфирования
|
|
25 |
|
+ H SO |
SO3H |
+ H2O |
|
|
|||
2 |
4 |
|
|
бензол |
|
бензолсульфоновая кислота |
|
4. Реакция алкилирования
AlCl3 |
CH |
+ CH3Cl |
3 + HCl |
бензол |
толуол |
5. Реакции окисления гомологов бензола
Бензол устойчив к окислению, но гомологи бензола окисляются в бензойную кислоту.
|
|
|
CH3 |
|
|
|
COOH |
||
|
|
|
|
||||||
5 |
|
|
|
+ 6 KMnO4 + 9 H2SO4 |
5 |
|
|
|
+ 6 MnSO4 + 3 K2SO4 + 14 H2O |
|
|
|
|
|
|
||||
или, в сокращенном виде
CH3 |
COOH |
|
[O] |
толуол |
бензойная кислота |
Влияние заместителей на реакционную способность кольца в реакциях электрофильного замещения
Различают два вида заместителей:
1. уже имеющиеся в бензольном кольце электронодонорные заместители повышают электронную плотность бензольного кольца и направляют входящие группы в орто- и пара-положения. К таким заместителям относятся: Cl, Br, I, CH3, C2H5, OH, OCH3, NH2, SH и т.д.
26
|
NH |
NH2 |
NH2 |
|
2 |
|
|
|
|
Br |
|
2 |
+ 2 Br2 |
+ |
+ 2 HBr |
|
|
|
Br |
|
анилин |
орто- |
пара- |
|
|
броманилин |
броманилин |
2. Электроноакцепторные заместители понижают электронную плотность в кольце и направляют входящие группы в мета-положение. К ним относятся:
NO2, COOH, CN, SO3H, COH.
COOH |
COOH |
|
H2SO4 |
+ HNO3 |
+ H2O |
|
NO2 |
бензойная кислота |
мета-нитробензойная |
|
кислота |
У п р а ж н е н и я
1.Напишите реакцию 2-метилпентана с одним молем брома при облучении УФ-светом, назовите продукт реакции по систематической номенклатуре. К какому типу относится эта реакция?
2.Напишите реакцию 2-метилпропена с водой в присутствии кислоты, назовите продукт по систематической номенклатуре, укажите тип реакции.
3.Напишите реакции толуола с хлором при облучении УФ-светом и в присутствии FeCl3, укажите типы обеих реакций и назовите их продукты.
4.Напишите реакции 2-метилбутена-1 и 3,3-дифторбутена-1 с HCl, укажите тип реакций, назовите их продукты.
5.Напишите реакцию бутена-2 с водным раствором KMnO4, назовите продукт реакции. Чьѐ имя носит эта реакция?
6.Напишите реакции циклопропана с бромом при облучении УФ-светом и в присутствии ZnBr2, назовите продукты реакций и укажите типы реакций.
7.Напишите реакцию акриловой кислоты с водой в кислой среде. Укажите тип реакции и назовите продукт реакции по систематической номенклатуре.
6.Из приведенных ниже соединений выберите те, которые взаимодействуют с бромистым водородом, напишите эти реакции и назовите продукты реакций по систематической номенклатуре: 2,3-диметилпентан, стирол, 1,3- диэтилциклогексан, 1,1-диметилциклопропан, 3-метилгептен-3, м-ксилол, 1- винил-2-метилциклогексан.
27
7.Напишите реакции изопрена с одним молем брома и с избытком брома в кислой среде. Укажите тип реакции и назовите продукты.
8.Из приведенных ниже веществ выберите те, которые взаимодействуют с водородом, напишите эти реакции и назовите продукты реакций: пентин-2, 1,3,5- триэтилциклогексан, 2,4-диметилоктан, гексади-1,3-ен, бутан, 3,3- диметилциклопропен, этилбензол, циклобутан.
9.Напишите реакции горения н-гептана, метана, ацетилена, бутади-1,3-ена, циклопропана, кумола, этилена в избытке кислорода. Какая из этих реакций является наиболее экзотермической?
10.Из приведенных ниже веществ выберите те, которые взаимодействуют с водным раствором нитрата серебра, напишите эти реакции и назовите продукты реакций: бутин-2, гексин-1, пропадиен(аллен), толуол, ацетилен, 2-метилпропан, пропин, изопрен, гексин-3, 3-метил-3-фенилциклопропен, метилциклогексан.
11.Напишите реакцию 3-метилпентана с разбавленной HNO3, назовите продукт реакции. Чьѐ имя носит эта реакция?
Спирты и фенолы
Спирты – это органические соединения, в состав которых входят одна или несколько гидроксильных групп (окси-групп –ОН), связанных с насыщенным атомом углерода.
По числу гидроксильных групп спирты делятся на одноатомные и много-
атомные.
Примеры одноатомных спиртов:
СH3OH |
C2H5OH |
CH2=CH-CH2OH |
метанол |
этанол |
пропен-2-ол-1 |
Примеры многоатомных (двух- и трехатомных) спиртов:
|
CH2-CH2 |
|
CH2-CH-CH2 |
|
|
|
|
|
|
OH OH |
OH OH OH |
|||
этандиол-1,2 |
пропантриол-1,2,3 |
|||
(этиленгликоль) |
(глицерин) |
|||
Спирты делятся на первичные, вторичные и третичные в зависимости от того, с каким атомом углерода (первичным, вторичным или третичным) связана гидроксильная группа.
|
|
CH3 |
|
CH3-CH2-CH2-CH2OH |
CH3-CH-CH3 |
CH3-C-CH3 |
|
|
|
||
|
OH |
OH |
|
бутанол-1 |
пропанол-2 |
2-метилпропанол-2 |
|
|
(изопропиловый спирт) |
(трет-бутиловый спирт) |
|

28
Химические свойства
1. Реакции спиртов со щелочными металлами с образованием алкоголятов
2 С2H5OH + 2 Na → 2 С2H5ONa + H2
этилат натрия
Реакции со щелочами с образованием алкоголятов не идут, т.к. алкоголяты щелочных металлов разлагаются в присутствии влаги.
С2H5OH + NaOH
2. Реакции спиртов с галогеноводородами
С2H5OH |
+ HCl → C2H5Cl + H2O |
этанол |
хлорэтан |
CH3-CH-CH3 + HBr |
CH3-CH-CH3 + H2O |
||
|
|
|
|
OH |
Br |
||
пропанол-2 |
2-бромпропан |
||
3. Реакции внутримолекулярной дегидратации (элиминирования) с образованием непредельных углеводородов
|
|
|
|
H SO , t>140o |
|
|
|
|
CH -CH-CH-CH |
2 |
4 |
CH -CH=CH-CH |
3 |
+ H2O |
|||
|
|
|||||||
3 |
|
3 |
|
|
3 |
|
||
|
|
|
|
|
|
|
|
|
H |
OH |
|
|
|
|
|
||
|
|
бутанол-2 |
|
|
бутен-2 |
|
||
Реакция элиминирования протекает по правилу Зайцева – отщепление протона происходит от менее гидрированного атома углерода.
4. Реакции межмолекулярной дегидратации а) между двумя молекулами спирта с образованием простых эфиров
|
|
|
|
H2SO4, t<140o |
С2H5OH |
|
|||
|
||||
С2H5OH |
C2H5-O-C2H5 + H2O |
|||
|
||||
|
|
|
|
|
этанол |
диэтиловый эфир |
|||
|
|
|
|
29 |
|
|
|
||
С2H5 |
OH |
H2SO4, t<140o |
||
С3H7OH |
C2H5-O-C3H7 + H2O |
|||
|
||||
|
|
|
|
|
этанол + пропанол |
метилпропиловый эфир |
|||
Продукты этих реакций - простые эфиры гидролизу не подвергаются.
б) между молекулами спирта и карбоновой кислоты с образованием сложных эфиров (реакция этерификации)
|
O |
|
|
H+ |
O |
||
СH3-C |
|
|
|
+ C H OH |
СH3-C |
+ H2O |
|
|
|
|
|||||
|
OH |
2 |
5 |
|
OC2H5 |
||
|
|
|
|
||||
|
|
|
|
||||
уксусная кислота этанол |
этилацетат |
||||||
Образующиеся сложные эфиры легко подвергаются гидролизу. В результате кислотного гидролиза образуются исходные спирт и карбоновая кислота, а в результате щелочного гидролиза образуются спирт и соль карбоновой кислоты.
5. Реакции окисления спиртов
Первичные спирты сначала окисляются до альдегидов, при дальнейшем окислении образуются карбоновые кислоты.
[O] |
O [O] |
|
O |
|
CH3OH |
H-C |
|
H-C |
|
|
|
OH |
||
|
H |
|
|
|
|
|
|
|
|
метанол |
формальдегид |
муравьиная кислота |
||
[O] |
O |
[O] |
O |
|
CH3-CH2-OH |
CH3-C |
|
|
CH3-C |
|
|
H |
|
OH |
|
|
|
|
|
этанол |
уксусный альдегид |
|
уксусная кислота |
|
Вторичные спирты при окислении образуют кетоны.
CH3- |
CH-CH3 |
[O] |
CH3-C-CH3 |
||
|
|||||
|
|
|
|
|
|
OH |
|
O |
|||
пропанол-2 |
|
пропанон-2 |
|||
|
30 |
OH |
O |
|
[O] |
циклопентанол циклопентанон Третичные спирты не окисляются.
6. Качественная реакция на многоатомные спирты, по которой можно отличить многоатомные спирты от одноатомных
При реакции многоатомных спиртов со щелочным раствором гидроксида меди (II) образуется внутрикомплексная соль меди (II), имеющая синюю окраску. Одноатомные спирты этой реакции не дают.
|
|
CH2-OH |
|
|
CH2-O |
HO- |
CH2 |
2 |
|
+ Cu(OH) |
2 |
|
Cu |
|
+ 2 H2O |
|
|||||||
|
CH2-OH |
CH2-OH |
O-CH2 |
||||
|
|
||||||
этиленгликоль |
|
|
гликолят меди (II) |
||||
Фенолы – это производные ароматических углеводородов, у которых один или несколько атомов водорода замещены на гидроксильную группу.
OH |
OH |
OH |
OH |
OH |
|
|
|
|
OH |
|
OH |
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
OH |
|
|
|
|
фенол гидрохинон пирокатехин |
резорцин |
пирогаллол |
|
||
Химические свойства
1.Реакции со щелочами и щелочными металлами с образованием фенолятов
Вотличие от спиртов фенолы реагируют со щелочами, т.к. обладают слабыми кислыми свойствами (см. «Кислотность и основность»).
OH |
ONa |
+ NaOH |
+ H2O |
фенол |
фенолят натрия |
31
2. Реакции получения сложных эфиров
При взаимодействии хлорангидридов карбоновых кислот с фенолами образуются сложные эфиры кислот.
|
O |
OH |
|
+ |
|
|
|
|
|
H |
O |
+ HCl |
|||
CH3 |
C |
+ |
CH3 |
C |
|||
|
|||||||
|
Cl |
|
|
|
O |
|
|
хлорангидрид |
фенол |
|
|
фенилацетат |
|
||
уксусной кислоты
3. Реакции фенолов как производных ароматических углеводородов
Для фенолов характерны реакции электрофильного замещения. Фенольная ОH-группа является электронодонором и, соответственно, ориентантом I рода (орто- и пара-ориентантом).
а) реакция галогенирования
Галогенирование фенолов протекает очень легко при комнатной температуре при действии хлорной или бромной воды.
OH |
|
OH |
|
|
H2O |
Br |
Br |
+ 3 HBr |
|
+ 3 Br2 |
|
|
||
|
|
|
||
|
|
Br |
|
|
фенол |
2,4,6-трибромфенол |
|
||
б) реакция нитрования |
|
|
|
|
OH |
|
OH |
|
|
H2SO4 |
O2N |
NO2 + 3 H O |
||
+ 3 HNO3 |
||||
|
|
2 |
||
NO2
2,4,6-тринитрофенол (пикриновая кислота)
в) реакция сульфирования

|
|
|
32 |
|
|
OH |
|
OH |
|
||
|
|
|
|
||
|
+ 2 H SO |
100oC |
|
SO3H |
+ 2 H2O |
|
|
||||
|
|||||
|
4 |
|
|
||
|
2 |
|
|
|
|
|
|
|
|
|
|
SO3H
4-оксибензол-
1,3-дисульфоновая кислота
г) реакция алкилирования
OH |
|
|
OH |
|
|
AlCl3 |
|
||
+ 3 CH3Cl |
CH3 |
CH3 + 3 HCl |
||
|
CH3
2,4,6-триметилфенол
4. Качественная реакция на фенолы
При реакции фенолов с хлоридом железа (III) FeCl3, образуются окрашенные комплексы. Фенол с FeCl3 дает фиолетовое окрашивание, гидрохинон – зеленое, пирокатехин – зеленое, резорцин – фиолетовое и пирогаллол – красное окрашивание.
5. Окисление фенолов
Фенолы легко окисляются с образованием хинонов.
OH |
O |
|
[O] |
O
фенол п-бензохинон
OH |
O |
|
[O] |
||
|
||
|
[H] |
|
OH |
O |
|
|
||
гидрохинон |
п-бензохинон |
33
Фенол как антисептик был впервые применен в 1867 г. в хирургической операции. В связи с выраженной токсичностью он обычно используется только для дезинфекции инструментов, белья и т.п. в виде слабого (3-5 %) водного раствора.
Тимол (2-изопропил-5-метилфенол) содержится в виде эфира в траве чабреца (тимиана, Thymus vulgaris), имеет малую токсичность, поэтому может применяться не только наружно для полосканий рта и носоглотки, но и внутрь как антисептик при заболеваниях желудочно-кишечного тракта, а также как противоглистное средство.
Резорцин – антисептик для наружного применения против экзем, себореи, грибковых заболеваний. Входит в состав шампуней.
Уп р а ж н е н и я
1.Из приведенных ниже веществ выберите те, которые взаимодействуют с металлическим калием, напишите эти реакции, назовите продукты реакций: кумол, бутанол-2, пентади-1,3-ен, 2-хлорпропан, 3-этилфенол, дибутиловый эфир, ацетилен, циклопропанол.
2.Какое из двух веществ – 2-бромфенол или 4-этоксициклогексанол – взаимодействует с водным раствором гидроксида лития? Напишите эту реакцию, назовите еѐ продукт, объясните разницу в реакционной способности исходных субстратов.
3.Напишите реакцию 2-метилпропанола-2 с HI, укажите тип этой реакции, назовите продукт реакции.
4.Напишите следующие реакции, назовите их продукты:
H2SO4
а) СH3CH2CH2CH2OH  t<140oC
t<140oC
H2SO4
б) (CH3)3C-OH
t>160oC
в) CH2=CH-CH2OH + 2 HBr 
г)C(NO2)3-CH2OH + NaOH (H2O)
д)CH2OH-CHOH-CH2OH + Li (изб)
5.Из приведенных ниже веществ выберите те, которые взаимодействуют с HCl, напишите эти реакции, укажите их тип, назовите их продукты: 1- метилциклопентанол-1, 2-изопропилфенол, этиленгликоль, 3-винилфенол, 2- метилпропен-2-ол-1, глицерин, 4-нитрофенол, циклопропанол, гидрохинон.
6.Из приведенных ниже веществ выберите те, которые взаимодействуют с водным раствором гидроксида калия, напишите эти реакции, назовите их продукты: 3-изопропилциклогексанол-1, 2-хлорфенол, 3-этилпентанди-2,4-ол, метанол, 2,2,2-трифторэтанол, 2-метилбутанол-2, α-нафтол, циклобутанол, резорцин.
34 7. Из приведенных ниже веществ выберите те, которые взаимодействуют с
CuO, напишите эти реакции, назовите их продукты: 2-метилбутанол-1, 3- метилпентанол-3, 3-метилбутанол-2, пропанди-1,3-ол, 1-метилциклопропанол-1, циклопропанол, гидрохинон, пентанди-1,3-ол, гептантри-2,4,6-ол, бензиловый спирт.
Альдегиды и кетоны
Альдегиды – это органические соединения, у которых карбонильная группа >C=O соединена с атомом водорода и алкильной (метильной, этильной и т.д.) группой.
Кетоны – это органические соединения, у которых карбонильная группа >C=O соединена с двумя алкильными группами.
- |
|
- |
+ O |
+ |
O |
R C |
R C |
|
H |
|
R' |
Двойная связь между атомами углерода и кислорода в карбонильной группе сильно поляризована, электронная плотность оттянута от атома углерода к атому кислорода, в результате чего атом кислорода приобретает частичный отрицательный заряд, а атом углерода – частичный положительный. Поэтому альдегиды и кетоны участвуют в реакциях нуклеофильного присоединения.
Химические свойства
1. Реакции нуклеофильного присоединения а) реакция со спиртами
Спирты присоединяются к альдегидам с образованием полуацеталей. В избытке спирта и кислых условиях реакция идет дальше с образованием ацета-
лей.
|
|
|
- |
|
|
|
|
OH |
|
|
+ |
O |
|
|
- + |
CH3 |
C OC2H5 |
CH |
3 |
C |
|
|
+ C |
H OH |
||
|
|
H |
|
2 |
5 |
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1-этоксиэтанол-1 |
|
|
|
|
|
|
|
|
(полуацеталь) |
|
|
|
OH |
|
|
|
|
H+ |
OC2H5 |
|
|
|
|
|
|
|
C OC2H5 |
|
CH |
|
C OC H |
+ C2H5OH |
CH3 |
||||
3 |
|
|
2 |
5 |
|
|
|
|
|
|
H |
|
|
|
|
|
H |
35
б) реакция с синильной кислотой |
|
|
|
|
|
|
|
|
|
||
|
O |
|
OH- |
|
|
OH |
|||||
CH3-CH2-C |
|
|
|
|
|
|
|
|
|
||
H |
+ HCN |
CH3-CH2-C |
|
|
|
|
CN |
||||
|
|
|
|
||||||||
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|||
пропаналь |
|
|
2-оксибутанонитрил |
||||||||
в) реакция с гиросульфитом натрия |
|
|
|
|
|
|
|
|
|||
O |
|
|
|
OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH3-CH2-C |
+ NaHSO |
CH -CH -C |
|
|
|
|
SO Na |
||||
|
|||||||||||
H |
|
3 |
3 |
2 |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|||||
пропаналь |
|
|
гидросульфитное производное |
||||||||
|
|
|
пропаналя |
|
|
||||||
г) реакции с азотсодержащими нуклеофилами
При взаимодействии альдегидов и кетонов с первичными аминами образуются N-замещенные имины.
O
CH3-CH2-C + NH2-CH3  CH3-CH2-C=N-CH3 + H2O H
CH3-CH2-C=N-CH3 + H2O H 




H
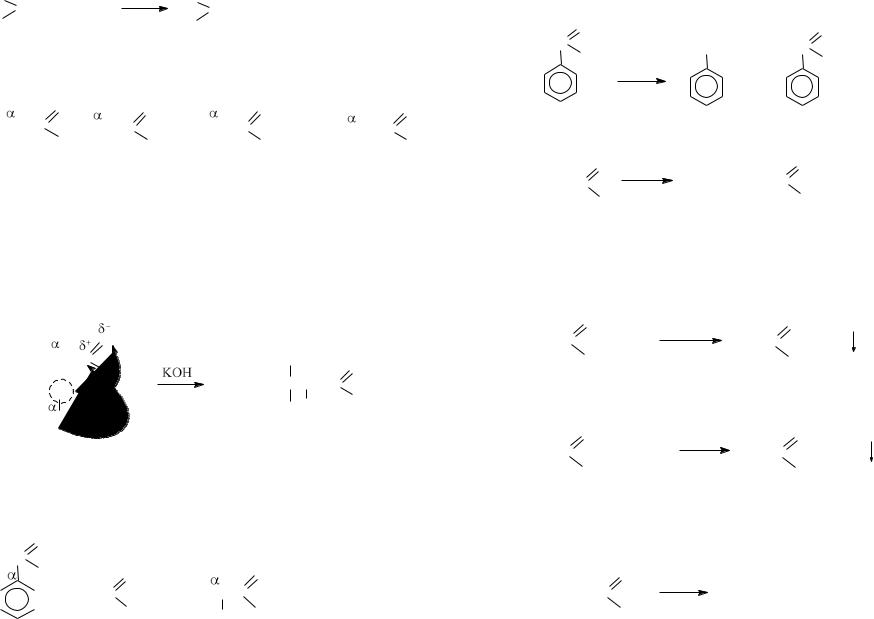
При взаимодействии альдегидов и кетонов с гидразинами получаются гидразоны, с фенилгидразином – фенилгидразоны, с гидроксиламином – оксимы.
|
O |
CH3-C=N-NH2 + H2O |
|
CH -C |
+ H2N-NH2 |
|
|
3 |
H |
|
|
|
H |
|
|
|
|
|
|
ацетальдегид гидразин |
гидразон ацетальдегида |
|
|
O |
|
|
|
C |
|
|
|
H |
|
|
|
+ |
NH2-NH |
C=N-NH |
+ H2O |
|
|
H |
|
полуацеталь |
1,1-диэтоксиэтан (ацеталь) |
бензальдегид фенилгидразин |
фенилгидразон бензальдегида |
|
|
36
CH3 |
|
CH |
|
|
|
C=O + NH2OH |
3 |
C=N-OH |
+ H2O |
CH3 |
CH |
|||
|
|
3 |
|
|
ацетон |
гидроксиламин |
оксим ацетона |
|
|
2. Реакция альдольной конденсации
|
|
O |
|
O |
O |
|
|
CH3 |
O |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
||||
CH3- |
CH- C |
|
CH -C |
|
CH3-CH2-C |
CH -CH -CH |
|
C |
||
|
|
|
||||||||
|
|
H |
3 |
H |
H |
3 2 |
|
|
|
|
|
|
|
|
|
|
|
H |
|||
CH3 |
|
|
|
|
|
|
|
|
|
|
2-метилпропаналь |
этаналь |
пропаналь |
2-метилбутаналь |
|||||||
Если в молекуле альдегида при α-углеродном атоме имеется хотя бы один атом водорода, то при действии разбавленных щелочей протекает реакция альдольной конденсации,. Протон, находящийся при α-углеродном атоме подвижен, т.к. рядом находится сильный акцептор – карбонильная группа. При действии щелочей протон отщепляется и переходит к кислороду карбонильной группы другой молекулы альдегида, а образующийся карбанион присоединяется к углероду.
|
O |
|
|
|
CH3-CH2-C |
H |
OH |
O |
|
|
|
|||
H |
|
CH3-CH2-C -CH-C |
H |
|
O |
H CH3 |
|||
|
|
|||
CH3-CH-C |
|
|
||
H |
|
|
||
|
|
|
||
3. Реакция Канниццаро |
|
|
||
Если в молекуле альдегида при α-углеродном атоме нет протона (как в приведенных ниже примерах), то в присутствии щелочей протекает реакция диспропорционирования – реакция Канниццаро.
|
|
O |
|
|
|
|
|
С |
H |
|
CH3 |
|
|
|
|
O |
O |
|||
|
|
|
|
|
||
|
|
|
H-C |
CH3-C-C |
H |
|
|
|
|
||||
|
|
|
H |
CH3 |
||
|
|
|
||||
|
|
|
|
|
||
бензальдегид формальдегид |
2,2-диметилпропаналь |
|||||
|
|
|
(нет α-углерода) |
|
|
|
37
При этом из двух молекул альдегида, вступающих в реакцию, одна молекула восстанавливается в спирт, а другая окисляется в кислоту.
|
O |
|
|
O |
С |
|
|
|
|
H |
СH2OH |
С |
|
|
|
OK |
|||
|
|
KOH |
|
|
|
|
|
|
|
2 |
|
|
+ |
|
бензальдегид |
бензиловый |
бензоат калия |
||
|
|
спирт |
|
|
O KOH |
O |
2 H-C |
CH3OH + H-C |
H |
OK |
формальдегид |
метанол формиат калия |
4. Реакции окисления
Альдегиды окисляются в карбоновые кислоты.
а) реакция «серебряного зеркала»
O |
|
NH4OH, t |
O |
CH3-C + Ag O |
|
||
CH3-C |
+ Ag |
||
H |
2 |
|
OH |
|
|
||
ацетальдегид |
|
уксусная кислота |
|
б) реакция с гидроксидом меди (II)
O |
|
|
O |
|
CH3-C + Cu(OH) |
CH -C |
+ Cu O |
||
H |
2 |
3 |
OH |
2 |
|
|
|
||
красный осадок
Кетоны в этих условиях не окисляются.
5. Реакции восстановления
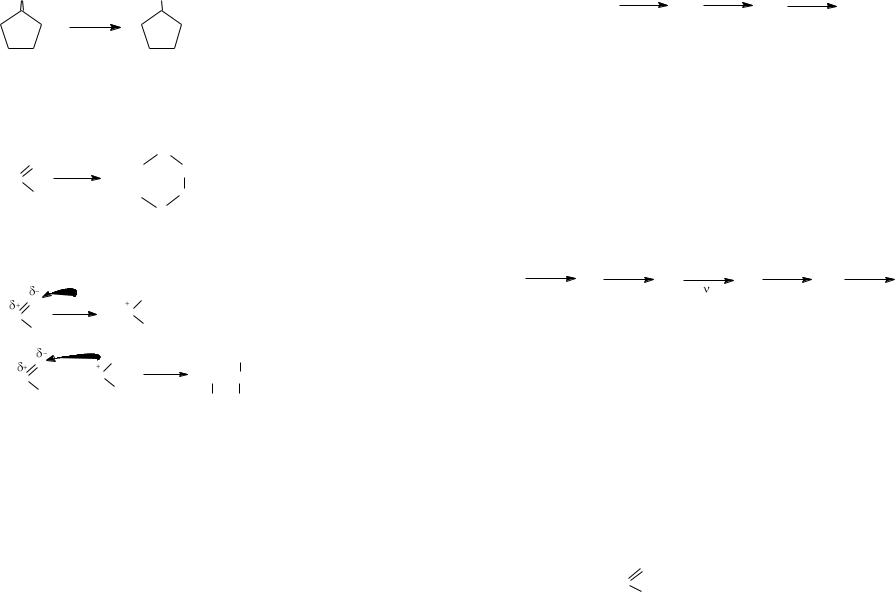
Альдегиды восстанавливаются в первичные спирты, кетоны – во вторичные спирты.
O |
[H] |
|
|
CH3-C |
CH3-CH2OH |
||
|
|||
H |
|
|
|
ацетальдегид |
|
этанол |
|
38 |
O |
OH |
|
[H] |
циклопентанон циклопентанол
6. Реакции полимеризации
При полимеризации формальдегида в присутствии минеральных кислот образуется преимущественно полимер циклической структуры – параформ.
|
O |
H+ |
O |
|||
|
|
|
||||
3 |
H-C |
|
|
CH2 |
|
CH2 |
|
|
|||||
|
H |
|
O |
O |
||
|
|
|
|
CH2 |
||
формальдегид |
параформ |
|||||
С увеличением радикала при карбонильной группе наряду с полимером циклической структуры образуется полимер линейной структуры.
O |
+ |
|
OH |
H |
R-C |
|
|
1) R-C |
|
H |
|
H |
|
|
|
|
|
|
|
O |
|
OH |
OH |
+ R-C |
+ |
||
2) R-C |
H |
R-C-O-C-R |
|
H |
|
H H |
|
|
|
|
Отличия альдегидов от кетонов
1.Альдегиды более реакционноспособны в реакциях нуклеофильного присоединения.
2.Альдегиды окисляются в карбоновые кислоты, кетоны не окисляются.
3.Альдегиды полимеризуются, кетоны не вступают в реакции полимериза-
ции.
Уп р а ж н е н и я
1.Напишите реакции 3-метилпентаналя со следующими реагентами: про- панол-2(эквимольное количество), метанол(избыток), этантиол(избыток). Укажите тип реакций, назовите продукты реакций.
2.Расшифруйте цепочку взаимодействий, напишите все реакции, укажите
типы реакций, назовите их продукты:
39
бромциклопропан |
KOH, H2O ... |
CuO |
... |
C2H5OH (изб.) ... |
|
3.Напишите реакцию этандиаля с избытком фенилгидразина, укажите тип реакции, назовите еѐ продукт.
4.Напишите реакции гексанона-2 со следующими реагентами: HCN(KCN),
H2NOH, NaHSO3, CH3SH(избыток), СН3СН2СН2ОН(избыток), (СН3)2СНNH2, CH3CH2CH2CH2OH(эквимольное количество). Укажите тип реакций, назовите их продукты. Какие из этих реакций приводят к образованию хиральных продуктов? Отметьте в этих продуктах асимметрические атомы углерода.
5.Напишите реакцию альдольной конденсации 3-метилбутаналя, укажите тип этой реакции, напишите еѐ механизм и назовите продукт.
6.Напишите реакции трифторацетальдегида со следующими реагентами: вода, фенол(эквимольное количество), гидразин, бутанол-2(избыток), мочевина. Укажите тип реакций, назовите их продукты.
7.Напишите реакцию Канниццаро для 2,2-диметилпропаналя, назовите продукты реакции.
8.Расшифруйте цепочку взаимодействий, напишите все реакции, укажите
типы реакций, назовите их продукты:
1 моль СH3Br |
KOH |
... |
1 моль Cl2 |
... |
CuO |
... |
KOH |
... |
|
бензол |
... |
|
|
|
|
||||
|
FeBr3 |
H2O |
|
h |
|
|
|
|
|
9. Напишите реакцию циклопентанона с анилином, укажите еѐ механизм, назовите продукт реакции.
|
10.Из приведенных ниже альдегидов выберите те, которые вступают в реак- |
цию |
альдольной конденсации, и те, которые вступают в реакцию Канниццаро, |
напишите эти реакции для соответствующих альдегидов, назовите продукты: 3- метилбензальдегид, 2-этилциклопропанкарбальдегид, 2,2-диметилпентаналь, 3,3-диметилпентаналь, 1-метилциклогексанкарбальдегид, формальдегид.
11.Напишите реакцию формальдегида с γ-аминомасляной кислотой, укажите еѐ механизм, назовите продукт реакции.
12.Напишите реакции формальдегида и бутаналя с синильной кислотой, укажите их тип, назовите продукты реакций. Укажите, какой из продуктов хиральный.
Карбоновые кислоты
Карбоновые кислоты – это органические соединения, в состав которых входят одна или несколько карбоксильных групп.
O
R-C
OH
По числу карбоксильных групп различают одноосновные карбоновые кислоты, двухосновные и многоосновные. В зависимости от того, каким является радикал, кислоты делятся на предельные, непредельные и ароматические.
