
Органическая химия.Казань
.pdf
80
8 |
Серин |
HO-CH2-CH-COOH |
Ser |
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
9 |
Треонин |
CH3-CH-CH-COOH |
Thr |
|
|
|
|
||
|
|
OH NH2 |
|
|
|
|
|
|
|
10 |
Цистеин |
HS-CH2-CH-COOH |
Cys |
|
|
|
|
|
|
|
|
NH2 |
|
|
11 Mетионин |
CH3-S-CH2-CH2-CH-COOH |
Met |
|
|
|
|
|
|
NH2 |
|
|
12 Аспарагиновая |
HOOC-CH2-CH-COOH |
Asp |
|
кислота |
|
|
|
NH2 |
|
||
|
|
||
13 |
Аспарагин |
NH2CO-CH2-CH-COOH |
Asn |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
||
|
|
|
|
|
|
|
|
|
|
14 |
Глутаминовая |
HOOC-CH2-CH2-CH- COOH |
Glu |
||||||
|
кислота |
|
|||||||
|
|
|
|
|
|
NH2 |
|
||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
15 |
Глутамин |
NH2CO-CH2-CH2-CH- COOH |
Gln |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
16 |
Пролин |
|
|
|
|
COOH |
Pro |
||
|
|
|
|
||||||
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|||
|
|
|
N |
|
|||||
|
|
|
H |
|
|||||
|
|
|
|
|
|
81 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
17 |
Гистидин |
|
|
N |
|
|
|
CH -CH-COOH |
His |
||||
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
N |
2 |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
NH2 |
|
||||
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
18 |
Триптофан |
|
|
|
|
|
|
CH2- |
|
CH-COOH |
Trp |
||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
NH2 |
|
||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
N |
|
||||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
H |
|
||||||
|
|
|
|
|
|
|
|||||||
19 |
Лизин |
NH2-CH2-CH2-CH2-CH2- CH-COOH |
Lys |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
||||||||||
20 |
Аргинин |
NH2-C-NH-CH2-CH2-CH2- CH-COOH |
Arg |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
NH2 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Все природные α-аминокислоты (кроме глицина) содержат асимметрический атом углерода и поэтому могут существовать в виде оптических изомеров. Природные аминокислоты, входящие в состав белков, относятся к L-ряду.
|
COOH |
|
COOH |
||||
H2N |
|
|
H |
H |
|
|
NH |
|
|
|
|
||||
|
|
|
|
|
|
2 |
|
|
R |
|
R |
||||
L-аминокислота |
D-аминокислота |
||||||
Химические свойства
Аминокислоты, как соединения, имеющие в своем составе аминогруппу и карбоксильную группу, проявляют свойства аминов, свойства карбоновых кислот и специфические свойства, обусловленные одновременным присутствием аминогруппы и карбоксильной группы.
82
1. Реакции образования солей
Аминокислоты являются амфотерными соединениями, что обусловлено одновременным присутствием в молекуле основной (NH2) и кислотной (COOH) групп.
а) реакции аминокислот с кислотами
|
|
|
CH3-CH-COOH + HCl |
|
CH3-CH-COOH |
||||||
|
|
|
|
|
|
|
+ |
NH Cl- |
|||
|
|
|
NH2 |
|
|||||||
|
|
|
|
|
|
|
3 |
|
|||
|
|
|
аланин |
солянокислая соль аланина |
|||||||
|
б) реакции аминокислот со щелочами |
|
|
|
|
|
|||||
HO |
|
|
CH2-CH-COOH + 2 NaOH |
NaO |
|
|
|
CH2-CH-COONa + H2O |
|||
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
NH2 |
|||
в) образование внутренней соли
Аминокислоты в нейтральной среде существуют в виде внутренней соли – биполярного иона, который называется также цвиттер-ионом.
CH -CH-COOH |
CH -CH-COO - |
||
3 |
|
3 |
|
|
|
+ |
|
NH2 |
NH3 |
||
2. Реакция дезаминирования
Аминокислоты, содержащие первичную аминогруппу, подвергаются дезаминированию в реакции с азотистой кислотой.
CH -CH-COOH |
+ HNO |
CH3-CH-COOH + N |
+ H O |
||
3 |
|
2 |
|
2 |
2 |
NH2 |
|
OH |
|
||
аланин |
|
молочная кислота |
|
||
3. Реакция декарбоксилирования
α-Аминокислоты при нагревании в присутствии гидроксида бария подвергаются декарбоксилированию с образованием аминов. В биологических системах декарбоксилирование протекает в присутствии фермента декарбоксилазы.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
83 |
|
|
|
|
|
|
|
|
|
|
|
CH3-CH-COOH |
Ba(OH)2, t |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
CH3-CH2 + CO2 |
|
|||||||||||||||||||
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|||
|
|
|
|
аланин |
|
|
|
|
|
|
|
этиламин |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
декарбоксилаза |
HO-CH2-CH2-NH2 |
+ CO2 |
|||||||||||
HO-CH -CH-COOH |
|
|||||||||||||||||||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
серин |
|
|
|
|
|
|
|
|
|
|
|
|
коламин |
|
||||||||
4. Реакции α-, β-, γ-аминокислот, протекающие при нагревании |
||||||||||||||||||||||||
а) нагревание α-аминокислот |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
CH3 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
CH3-CH-C |
|
|
|
|
CH |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
OH |
t |
HN |
|
|
|
|
C=O |
|
||||||||||||||
|
|
|
|
NH2 |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ 2 H2O |
||||||
|
|
|
|
|
|
|
|
|
|
NH2 |
|
O=C |
|
|
|
|
NH |
|
||||||
|
|
|
|
|
HO |
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
CH |
|
|||||||||||||
|
|
|
|
|
|
|
|
C-CH-CH3 |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|||||
|
|
|
|
|
|
|
аланин |
|
дикетопиперазин |
|
||||||||||||||
б) нагревание β-аминокислот |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
CH3-CH-CH-COOH |
t |
CH -CH=CH-COOH |
+ NH |
|||||||||||||||||||||
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
3 |
|
|
NH2 H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
β-аминомасляная кислота |
|
кротоновая кислота |
|
|||||||||||||||||||||
в) нагревание γ-аминокислот |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
CH2-CH2 |
|
||||||
|
|
CH2-CH2-CH2-C |
|
|
t |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
C=O + H2O |
|||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||
NH2 |
|
|
|
|
OH |
|
|
|
CH -NH |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
||||
γ-аминомасляная кислота |
|
|
|
|
лактам |
|
||||||||||||||||||
5. Реакция образования комплексной соли с Cu(OH)2
Аминокислоты, реагируя с Cu(OH)2, образуют комплексные медные соли синего цвета.

|
|
84 |
|
|
|
|
|
O |
|
|
|
NH2-CH2-C |
O |
|
|
|
|
+ 2 H2O |
|
2 NH2-CH2-COOH |
+ Cu(OH)2 |
Cu |
O |
|
|
|
|
|
|
|
|
NH2-CH2-C |
|
|
|
|
|
O |
|
6. Реакция образования пептидов (первичной структуры белка) |
|
|||
O |
O |
O |
|
|
NH2-CH-C-OH + NH2-CH-C-OH + NH2-CH-C-OH |
|
|
||
CH3 |
CH2 |
CH2 |
|
|
|
OH |
COOH |
|
|
O |
O |
O |
|
|
NH2-CH-C- NH-CH-C- NH-CH-C-OH + 2 H2O |
|
|
||
CH3 |
CH2 |
CH2 |
|
|
|
OH |
COOH |
|
|
пептидная
связь
Основным источником α-аминокислот для живого организма служат пищевые белки. Многие α-аминокислоты синтезируются в организме, некоторые же необходимые для синтеза белков α-аминокислоты не синтезируются в организме и должны поступать извне. Такие аминокислоты называют незаменимыми: валин, лейцин, изолейцин, лизин, треонин, метионин, фенилаланин, триптофан.
Метионин используют в медицине для лечения и профилактики токсических поражений печени и при диабете. Природный метилметионинсульфонийхлорид называют витамином U. Им богаты капуста, петрушка и томаты. Он рекомендуется для лечения язвы желудка. Этот витамин играет в биопроцессах роль донора метильных групп.
CH-COOH
|
|
|
MeS+ |
NH2 |
|
Cl- |
|
|
Триптофан – используется для лечебного питания. Глутаминовая кислота
– находит применение при лечении заболеваний ЦНС (эпилепсии, психозов; у детей – при полиомиелите и задержке психического развития). Ее натриевая соль используется как вкусовая и консервирующая добавка в пищевые продукты.
85
Метиловый эфир L-аспарагилL-фенилаланина (аспартам, аспартат) ис-
пользуют при диабете как малокалорийный заменитель сахара.
γ-Аминомасляная кислота является природным веществом и была обнаружена в головном мозге млекопитающих в 1950 г. Установлено, что она играет роль медиатора торможения при передаче нервных импульсов. ГАМК (аминалон, гаммалон) применяют при лечении нарушений нервной системы: расстройство речи, ослабление памяти, атеросклероз мозговых сосудов, умственная отсталость у детей. Она обладает ноотропными свойствами – стимулирует обучение, улучшает умственную деятельность и память.
6-Аминогексановая (ε-аминокапроновая) кислота применяется в медицине для остановки сильных кровотечений, так как она способствует эффективному свертыванию крови.
Производные п-аминобензойной кислоты
Среди многих тысяч производных п-аминобензойной кислоты найден ряд эффективных местных анестетиков – веществ, подавляющих чувствительность (возбудимость) нервных окончаний. Такие ее эфиры как анестезин, новокаин и дикаин стали успешно заменять в клинике алкалоид кокаин, не вызывая при этом болезненного привыкания к лекарству.
NH |
2 |
NH |
2 |
|
NH-(CH2)3-CH3 |
||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
СOOC2H5 |
O=CO-(CH2)2N(C2H5)2 |
O=CO-(CH2)2N(C2H5)2 |
|||
анестезин |
новокаин |
дикаин |
|||
Уп р а ж н е н и я
1.Напишите образование биполярных ионов для следующих аминокислот: серина, триптофана, аспарагина, аланина, лейцина, метионина, пролина, аргинина.
2.Напишите реакции фенилаланина со следующими реагентами: кальций, соляная кислота, гидроксид натрия, ацетальдегид, пропанол-2, ацетилхлорид. Укажите типы реакций, назовите их продукты.
3.Напишите реакции азотистой кислоты со следующими аминокислотами: треонин, изолейцин, глицин, γ-аминомасляная кислота, аланин, лизин, аспарагиновая кислота, глутаминовая кислота. Назовите продукты реакций.
4.Напишите реакции декарбоксилирования in vitro следующих аминокислот: серин, лизин, гистидин, фенилаланин, триптофан, аспарагиновая кислота, глутамин, аргинин. Назовите продукты реакций.
5.Напишите реакции формальдегида со следующими аминокислотами: изолейцин, лизин, глицин, метионин, тирозин, фенилаланин, ε-аминокапроновая кислота. Назовите продукты реакций.
86
6.Напишите реакции образования дикетопиперазинов из следующих аминокислот: аланин, глицин, метионин, валин, лейцин, фенилаланин, серин, изолейцин.
7.Напишите реакции образования α,β-непредельных кислот из следующих аминокислот: β-аминомасляная кислота, 3-амино-3-фенилпропановая кислота, 2-аминоциклогексанкарбоновая кислота. Назовите продукты реакций.
8.Напишите реакции образования β-лактамов из следующих аминокислот: β-аминопропионовая кислота, β-аминомасляная кислота, β-аминовалериановая кислота. В молекулах каких лекарственных препаратов есть β-лактамный цикл?
9.Напишите реакции образования соответствующих лактамов из следую-
щих аминокислот: γ-аминомасляная кислота, δ-аминовалериановая кислота,ε- аминокапроновая кислота.
10.Напишите образование трипептида из следующих аминокислот: цистеин, лейцин, триптофан. Укажите пептидные связи, концевые группы и асимметрические атомы углерода.
11.Напишите образование трипептида из следующих аминокислот: аспарагиновая кислота, гистидин, глицин. Укажите пептидные связи, концевые группы
иасимметрические атомы углерода.
12.Напишите образование трипептида из следующих аминокислот: аргинин, пролин, лизин. Укажите пептидные связи, концевые группы и асимметрические атомы углерода.
13.Укажите основные функции белков в живых организмах. Приведите примеры простых и сложных белков.
Гетероциклические соединения
Гетероциклические соединения – это органические соединения, в циклах которых, кроме атомов углерода, содержатся атомы других элементов, называемые гетероатомами (атомы азота, серы, кислорода и др.). Размер цикла может быть различным. Наибольшее распространение в природе имеют пяти- и шестичленные циклы.
Пятичленные гетероциклы с одним гетероатомом
N |
O |
S |
H |
|
|
пиррол |
фуран |
тиофен |
Эти соединения обладают ароматическим характером, т.к. в них образуется сопряженная система из 4 π-электронов атома С и 2 ρ-электронов гетероатома (ρπ-сопряжение).
Наиболее важное биологическое значение имеют азотсодержащие гетероциклические соединения.
87
Химические свойства
1. Реакции ароматического характера
В реакциях электрофильного замещения водород замещается в α- положении.
N
H
Так как пиррол является «ацидофобным», т.е. в присутствии кислот полимеризуется, то в реакциях электрофильного замещения используют специфические реагенты, не содержащие протонов (Н+).
а) Реакция нитрования
|
|
|
|
O |
|
|
|
|
|
+ CH3COOH |
|
|
|
+ СH3-C |
|
|
|
|
|
NO |
|
|
N |
O-NO2 |
|
N |
|
2 |
||||
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
|
|
||||
пиррол |
|
2-нитропиррол |
|
|
||||||
б) реакция сульфирования
|
|
|
+ C H N SO |
3 |
|
|
|
|
|
|
|
|
+ C5H5N |
|
5 |
5 |
|
|
|
|
|
|
|
SO3H |
|
||||
|
N |
|
|
|
|
|
|
N |
|
|||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
||||||
|
H |
|
|
|
|
|
|
|
|
|||||
пиррол |
|
|
|
2-сульфопиррол |
|
|||||||||
в) реакция галогенирования |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
C2H5OH |
Br |
|
|
|
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
+ 4 Br2 |
|
|
|
|
|
|
|
+ 4 HBr |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
N |
|
|
Br |
|
N |
|
|
|
Br |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
H |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
пиррол |
|
|
2,3,4,5-тетрабромпиррол |
|
||||||||||
88
2. Реакции присоединения (гидрирования)
+ 2 H |
кат. |
|
2 H |
|
|
|
|
N |
|
N |
N |
H |
|
H |
H |
пиррол |
|
пирролин |
пирролидин |
3. Реакции со щелочными металлами
Пиррол обладает кислыми свойствами, т.к. неподеленная электронная пара атома азота участвует в образовании единой сопряженной системы.
2 |
+ 2 K |
2 |
+ H2 |
N |
|
N |
|
H |
|
K |
|
|
|
|
|
пиррол |
|
пиррол-калий |
|
Производные пиррола занимают особое место в ряду биологически важных соединений. Основу витамина В12, а также «пигментов жизни» -гемоглобина, хлорофилла, цитохрома – составляют порфириновые тетрапиррольные макроциклы. Среди синтетических производных пирролидина выделяются две группы биологически активных веществ: психотропные и антигипертензивные лекарственные средства. Первым из группы психотропных препаратов стал пирацетам (ноотропил, нормабрейн). Он легко проникает через гематоэнцефалический барьер (ГЭБ) в отличие от своего химического аналога γ-аминомасляной кислоты. Пирацетам применяют и при лечении больных, перенесших черепномозговую травму, инсульт, атеросклеротическое поражение сосудов мозга у старых людей, при умственной отсталости у детей.
 N
N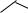 O CH2C(O)NH2
O CH2C(O)NH2
пирацетам
Из производных пирролидина выделяются два лекарственных вещества, вошедших в практику в качестве антигипертензивных (сердечно-сосудистых, снижающих артериальное давление) средств – каптоприл (капотен) и эналаприл (вазотек).
|
|
|
89 |
|
|
|
|
N |
СOOH |
N |
СOOH |
||||
|
|
|
|
||||
|
|
|
|
|
|
||
O=CCH(Me)CH2SH |
O=CCH(Me)NH- |
|
CHC(O)OEt |
||||
|
|||||||
каптоприл |
|
|
CH2CH2Ph |
||||
|
|
эналаприл |
|||||
|
|
|
|
|
|||
Фуран и его производные напоминают соединения пиррольного ряда. Фуран ацидофобен и подобно пирролу при действии минеральных кислот подвергается полимеризации с раскрытием цикла, что сопровождается смолообразованием. При действии подходящих электрофильных реагентов фуран легко вступает в реакции электрофильного замещения – нитруется ацетилнитратом в пиридине и сульфируется пиридинсульфотриоксидом. Заместитель при этом вступает в α- положение. Фуран может присоединять водород в присутствии никелевого катализатора с образованием тетрагидрофурана, который широко используется в качестве растворителя.
К производным фурана относится витамин С (аскорбиновая кислота), который сначала получил известность как противоцинговый препарат. Он эффективно поддерживает сопротивляемость организма инфекциям и простудам. Этот витамин повышает эластичность стенок сосудов, снимает отложение на них холестерина и останавливает развитие атеросклероза. Установлено, что водорастворимый витамин С действует как антиоксидант, дезактивируя свободные радикалы сигаретного дыма (последние увеличивают адгезионную способность лейкоцитов крови и способствуют, таким образом, отложению бляшек на стенках кровеносных сосудов, увеличивая риск сердечно-сосудистых и легочных заболеваний).
|
|
|
|
O |
||||
O |
|
|
|
|
|
|
|
CHOH-CH2OH |
|
|
|
|
|||||
|
|
|
|
|
|
|
||
|
|
|
|
|
||||
HO |
|
|
|
|
OH |
|||
|
|
|
|
|||||
|
|
|
|
|||||
аскорбиновая кислота
Шестичленные гетероциклы с одним гетероатомом
N
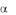
Пиридин

90
В молекуле пиридина (как и в бензоле) имеется общее π-электронное облако из шести электронов, пять из которых предоставляют атомы углерода и один электрон дает атом азота. Но ароматические свойства пиридина выражены слабее, чем у бензола. Это связано с влиянием электроотрицательного атома азота.
Химические свойства
1. Реакции электрофильного замещения
Реакции электрофильного замещения в пиридине протекают преимущественно в β-положение.
а) Реакции нитрования
|
|
|
|
t |
|
|
|
|
|
|
NO2 |
||
|
|
|
+ HONO2 |
|
|
|
|
|
|
+ H2O |
|||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
N |
|
|
|
|
|
N |
|
|
||||
пиридин |
3-нитропиридин |
||||||||||||
б) Реакции галогенирования |
|
|
|||||||||||
|
|
|
t |
|
|
|
|
|
Br |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
+ HBr |
|
|
|
|
+ Br2 |
|
|
|
|
|
|
|
|
|
|
|
N |
|
N |
|
|
||||||||
пиридин |
3-бромпиридин |
|
|
||||||||||
в) Реакции алкилирования |
|
|
|||||||||||
|
|
|
|
t |
|
|
|
|
|
|
CH3 |
||
|
|
|
+ CH3Cl |
|
|
|
|
+ HCl |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
N |
|
|
|
N |
|
|
||||||
пиридин |
3-метилпиридин |
||||||||||||
2. Реакции нуклеофильного замещения
Реакции нуклеофильного замещения в пиридине протекают в α-положении.
+ NaOH |
|
+ NaH |
N |
N |
OH |
|
||
пиридин |
2-оксипиридин |
|
|
91 |
+ NaNH2 |
+ NaH |
N |
N NH2 |
пиридин |
2-аминопиридин |
3. Реакции по аминогруппе (основные свойства)
+ HCl |
Cl- |
N |
N |
|
H |
пиридин |
хлорид пиридиния |
4. Реакции восстановления |
|
+ 6 H |
|
N |
N |
|
H |
пиридин |
пиперидин |
5. Реакции окисления
Пиридин устойчив к окислению, но его гомологи легко окисляются.
CH3 |
COOH |
|
+ [O] |
N |
N |
3-метилпиридин |
пиридинкарбоновая кислота |
|
(никотиновая кислота) |
В настоящее время из 1500 наиболее известных лекарственных веществ, применяемых в медицине, 5% составляют препараты пиридинового и 6 % - пре-
параты пиперидинового рядов. Витамин В5 (ниацин, никотиновая кислота) пре-
дотвращает развитие пеллагры – болезни кожи, которая сопровождается нервными расстройствами, потерей памяти, а в тяжелых случаях приводит к смерти. Ниацин участвует в регуляции деятельности нервной системы и желудочнокишечного тракта, поддерживает нормальный метаболизм, ингибируя выброс свободных жирных кислот, уменьшает уровень холестерина в плазме крови. Его не только применяют в клинике для лечения пеллагры, но и рекомендуют также
92
при инфекционной желтухе, бронхиальной астме, гипертонии, сердечнососудистых заболеваниях. В последние десятилетия показано, что комплекс никотинамида с хлоридом железа можно использовать для эффективного восполнения потерь железа в организме. В виде комплекса с хлоридом кобальта он рекомендован при лечении переломов костей. Никотиновая кислота тормозит рост саркомы, а ее соль с алюминием (III) оказывает антиспастическое и сосудорасширяющее действие. В виде никотинамида этот витамин входит в состав коферментов НАД+ и НАДФ (см. стр. )
Ниацин использован для синтеза кордиамина – аналептика и стимулятора ЦНС.
|
|
|
O |
|
|
|
C |
C2H5 |
|
|
|
|
N |
|
|
|
|
C2H5 |
|
N |
||||
|
||||
кордиамин |
|
|||
Производные 4-пиридинкарбоновой кислоты (изоникотиновой) применяются в качестве противотуберкулезных препаратов. Одним из наиболее широко используемых антитуберкулезных средств является изониазид. Конденсацией изониазида с ванилином получают еще один противотуберкулезный препарат – фтивазид, обладающий меньшей токсичностью, чем его предшественник.
O=CNHNH2 |
O=CNHN=CH- |
OH |
|
|
OCH3 |
N |
N |
|
изониазид |
фтивазид |
|
Пятичленные гетероциклы с двумя гетероатомами
N
N N N
N
H H
пиразол имидазол
Пиразол и имидазол представляют собой сопряженные системы. Вследствие влияния второго атома азота пиразол и имидазол более стабильны, чем пиррол (более ароматичны).
93
Химические свойства
1. Реакции с кислотами и щелочными металлами
Имидазол и пиразол являются амфотерными соединениями – слабыми NHкислотами и основаниями.
|
N |
N H Cl- |
|
|
|
+ |
|
|
+ HCl |
|
|
|
N |
N |
|
|
H |
H |
|
|
N |
N |
|
2 |
+ 2 K |
2 |
+ H2 |
|
N |
N |
|
H K
2. Реакции электрофильного замещения
Реакции электрофильного замещения протекают в положение 4 или 5.
а) Реакции нитрования
|
|
|
|
N |
O2N |
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
+ HNO3 |
|
|
|
|
|
|
|
+ H O |
|
|
N |
|
|
|
|
|
N |
2 |
|||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
H |
|
|||||
имидазол |
4-нитроимидазол |
|
|||||||||||
б) Реакции галогенирования |
|
|
|
|
|
|
|
||||||
|
|
|
|
N |
Br |
|
|
|
N |
|
|||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
+ Br2 |
|
|
|
|
|
|
|
+ HBr |
|
|
N |
|
|
N |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
|
||||||||
имидазол |
4-бромимидазол |
|
|||||||||||

|
|
|
|
94 |
||
в) Реакции алкилирования |
|
|
|
|||
|
|
|
N |
|
|
N |
|
|
|
|
|
||
|
|
|
+ CH3Cl |
|
|
+ HCl |
|
N |
N |
||||
|
|
|
|
|
|
|
|
H |
CH3 |
||||
Имидазольное кольцо часто встречается в синтетических лекарственных препаратах и биогенных веществах. Незамещенный имидазол проявляет некоторую биоактивность, ингибируя фермент тромбоксан В-2 (который участвует в превращениях арахидоновой кислоты). Это приводит к росту концентрации простациклина и приостанавливает свертывание крови. Гистамин является биогенным амином и выполняет в организме роль нейромедиатора. В свободном состоянии он может вызывать аллергические реакции. В виде дигидрохлорида его используют при лечении полиартрита, ревматизма и аллергических заболеваний.
H2N-CH2-CH2 N
N
H
гистамин
Щестичленные гетероциклы с двумя гетероатомами
N |
|
N |
|
|
|
N |
N N |
N |
пиримидин пиридазин пиразин
Наибольшее практическое значение из них имеет пиримидин.
1. Реакции с кислотами
Пиримидин обладает более слабыми основными свойствами, чем пиридин, вследствие влияния второго атома азота, поэтому вступает в реакцию с одним молем кислоты.
|
+ |
N |
Cl- H N |
|
+ HCl |
N |
N |
пиримидин |
пиримидинийхлорид |
95
2.В реакции электрофильного замещения пиримидин не вступает.
3.Реакции нуклеофильного замещения
N |
|
t |
|
N |
|
+ NaNH2 |
|
|
|
+ NaH |
|
N |
|
|
N |
NH2 |
|
пиримидин |
|
2-аминопиримидин |
|||
|
|
|
78 |
|
|
N |
|
|
|
N |
|
+ NaOH |
|
|
|
+ NaH |
|
|
|
|
|
|
|
N |
|
|
N |
OH |
|
|
|
|
|
||
пиримидин |
|
|
2-оксипиримидин |
||
Производные пиримидина |
|
|
|
|
|
O |
|
O |
|
|
NH2 |
HN |
HN |
|
CH3 |
N |
|
O N |
O |
N |
|
O |
N |
|
|
|
|||
H |
|
H |
|
|
H |
|
|
|
|
|
|
урацил |
тимин |
|
цитозин |
||
Для них характерно явление лактам-лактимной таутомерии.
O |
|
OH |
|
O |
|
OH |
HN |
N |
|
HN |
CH3 |
N |
CH3 |
O N |
HO |
N |
O |
N |
HO |
N |
|
|
|||||
H |
|
|
|
H |
|
|
|
NH2 |
NH2 |
|
N |
N |
|
|
|
O |
N |
HO N |
|
|
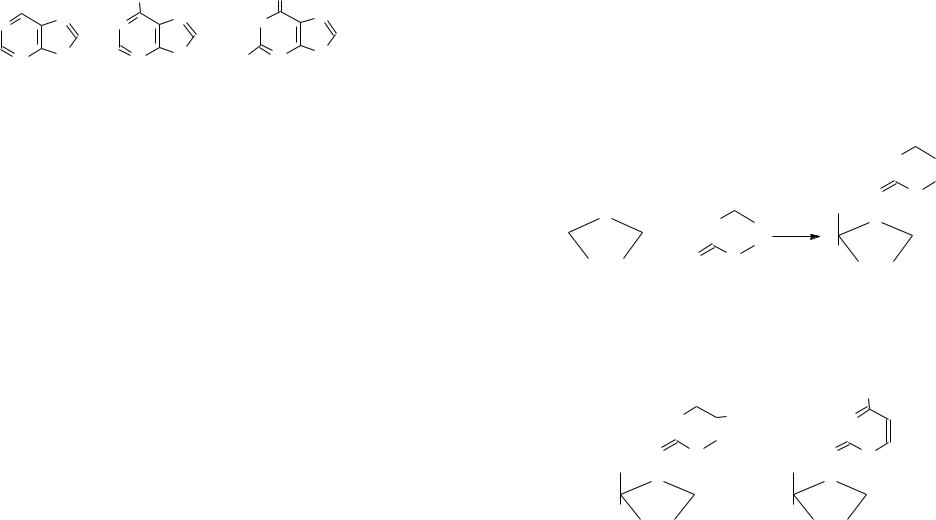
H
Пурин является амфотерным соединением, представляющим собой слабую кислоту и слабое основание.
|
|
|
|
96 |
|
|
|
Пурин и его производные |
|
|
|
|
|||
|
|
NH2 |
|
|
O |
|
|
N |
N |
N |
N |
HN |
|
N |
|
|
|
|
|
||||
N |
N |
N |
N |
H2N |
N |
N |
|
H |
|||||||
|
H |
|
H |
|
|
||
пурин |
|
аденин |
|
|
гуанин |
|
|
Уп р а ж н е н и я
1.Напишите формулы следующих трехчленных гетероциклов: оксиран, азиридин, тииран. Напишите реакции этих гетероциклов с соляной кислотой.
Назовите продукты реакций.
2. Напишите реакцию ступенчатого гидрирования пиррола. Объясните разницу в основности между пирролом и пирролидином. Напишите реакцию пирролидина с HBr.
3. |
Напишите реакцию тиофена с серной кислотой, укажите тип реакции, |
назовите еѐ продукт. |
|
4. |
Напишите реакции пиридина со следующими реагентами: Br2, КОН, |
KNH2, H2. Укажите типы реакций, назовите их продукты. В каком из этих про- |
|
дуктов |
возможна лактим-лактамная таутомерия? Сравните основность пири- |
дина и |
пиперидина. |
5. |
Напишите реакции имидазола с металлическим калием и с соляной ки- |
слотой. Объясните амфотерный характер имидазола.
6. Напишите все возможные таутомерные формы для 2,4,6 – триоксипиримидина и 2,4,6 – триаминопиримидина.
7. Какой из продуктов в этой цепочке применяется как лекарственный препарат?
8. .Напишите реакции серотонина со следующими реагентами: КОН, азотистая кислота(избыток), НСl, СН3СОCl(избыток).
9. Напишите реакцию изоникотиновой кислоты с гидразином. Где применяется продукт этой реакции?
Нуклеотиды и нуклеиновые кислоты
Нуклеиновые кислоты являются составной частью всех живых клеток., играют главную роль в передаче наследственных признаков (генетической информации) и управлении процессом биосинтеза белка. Существует два различных типа нуклеиновых кислот – рибонуклеиновые кислоты (РНК) и дезоксирибонуклеиновые кислоты (ДНК). РНК отличается от ДНК моносахаридным остатком: в
97
состав РНК входит рибоза, а в состав ДНК входит дезоксирибоза. Кроме того, в состав РНК входят четыре нуклеиновых основания – урацил, цитозин, аденин, гуанин. В состав ДНК входят тимин, цитозин, аденин, гуанин. Нуклеиновые кислоты представляют высокомолекулярные соединения. Их полимерные цепи построены из мономерных единиц – нуклеотидов, в связи с чем нуклеиновые кислоты называют полинуклеотидами.
Нуклеозиды и нуклеотиды
1. Реакция образования нуклеозида
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HN |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
HOCH2 |
|
|
|
|
|
|
O |
|
|
|
|
|
N |
|||||||||||
O |
|
|
OH |
|
|
|
|
|
|
HOCH2 |
O |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
HN |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
H |
|
H |
|
|
+ |
|
|
|
|
|
|
H |
H |
|
|
|
|
+ H2O |
|||||
H |
|
|
|
|
H |
O N |
H |
|
|
|
|
H |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
||||
|
OH |
OH |
|
|
|
OH |
OH |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
β-рибофураноза |
|
урацил |
|
|
|
уридин |
|
|
|
|
|
||||||||||||
Пиримидиновые нуклеозиды
|
|
|
|
|
|
O |
|
|
|
|
|
NH2 |
|||||
|
|
|
HN |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
СH3 |
|
|
|
O |
N |
||||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
N |
|||||||
HOCH2 |
O |
|
|
|
|
|
|
HOCH2 |
O |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
H |
|
H |
|
|
|
H |
|
H |
|
|
||||||
|
|
|
|
|
|
|
|
||||||||||
H |
|
|
|
|
H |
H |
|
|
|
H |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
OH |
OH |
||||||||
тимидин |
|
|
|
|
|
|
|
цитидин |
|||||||||

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
98 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Пуриновые нуклеозиды |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
N |
|
|
|
HN |
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
N |
|
|
|
H2N |
|
|
N |
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
HOCH2 |
|
|
|
|
|
|
|
|
|
HOCH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
H H |
|
|
|
|
|
|
H |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
аденозин |
|
|
|
|
|
|
|
гуанозин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
2. Реакции образования нуклеотидов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
а) образование нуклеотида, входящего в состав ДНК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
HN |
|
|
|
|
|
|
|
|
СH3 |
|
|
|
|
|
OH |
|
|
|
|
|
|
HN |
|
|
|
|
|
|
|
|
|
СH3 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
O |
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
N |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
HOCH2 |
O |
|
|
|
|
|
|
|
|
|
|
O=P |
-O-CH2 |
|
O |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
H |
|
|
H |
|
|
|
|
|
+ H3PO4 |
|
|
|
|
|
H |
|
H |
|
|
|
|
|
|
+ H2O |
|||||||||||||||||
|
|
|
|
H |
|
|
|
H |
|
|
|
|
|
|
H |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH H |
|
|
|
|
|
|
|
|
|
|
||||||||||
б) образование нуклеотида, входящего в состав РНК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
NH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
N NH2 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
HOCH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
O=P |
-O-CH2 |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
O |
|
|
|
OH |
+ |
|
|
HN |
|
|
|
|
|
N |
+ H3PO4 |
OH |
|
|
H |
H |
+ 2 H2O |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|||||||||||||
H |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
H2N N |
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
|
|
|
|
|||||
|
OH |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
99
При лечении некоторых опухолевых заболеваний в качестве лекарственных средств используют синтетические производные пиримидинового и пуринового рядов, по строению похожие на естественные метаболиты (в данном случае – на нуклеиновые основания), но не полностью им идентичные, т.е. являющиеся антиметаболитами. Конкурируя с метаболитами, они нарушают на разных этапах синтез нуклеиновых кислот в организме.
Нуклеозидполифосфаты. Никотинамиднуклеотиды.
Нуклеотиды имеют большое значение не только как строительный материал для нуклеиновых кислот. Они участвуют в биохимических процессах, и особенно важны в роли коферментов, т.е. веществ, тесно связанных с ферментами и необходимых для проявления ферментативной активности.
Большое значение в живых организмах играют нуклеотиды, содержащие в своем составе трифосфатные группировки – АТФ – аденозин-5’-трифосфорная кислота. С участием АТФ и АДФ в организме осуществляется важнейший биохимический процесс – перенос фосфатных групп.
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
||
O |
O O |
|
|
|
|
|
|
|
|
N |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
N |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
HO-P-O-P-O-P |
-O-CH2 |
|
O |
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH OH OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
H |
H |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
H |
|
|
|
|
H |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
||||
АТФ является своеобразным аккумулятором энергии в живых организмах. При гидролизе АТФ связи Р-О-Р легко разрываются, при этом выделяется большое количество энергии ≈ 33 кДж/моль.
