
- •Первый закон термодинамики. Термодинамические системы. Взаимопревращения теплоты, работы и энергии. Работа типа pv. Сохранение энергии.
- •Первый закон термодинамики и химические реакции
- •Теплота, энергия и молекулярное движение
- •Энтропия и неупорядоченность системы
- •Изменение свободной энергии при совершении внешней работы
- •Термодинамические процессы в почвах
- •Лекция 6 «переменные состояния и потенциалы почвенных термодинамических систем»
- •Термодинамические потенциалы
- •Термическое равновесие.
- •Механическое равновесие.
- •Равновесие фаз.
- •Химические реакции.
Термическое равновесие.
Рассмотрим адиабатическую систему, состоящую из образца почвы, заключенного в жесткую диатермическую оболочку, находящуюся в контакте с тепловым резервуаром. Почва и резервуар в свою очередь окружены изолирующей оболочкой. Простым примером сложной системы такого типа является небольшое количество почвы, помещенное в металлический стакан, плотно закрытый пластиковой крышкой и погруженный в водяную баню (термостат) с двойными теплоизоляционными стенками. Для системы почва—термостат можно записать в дифференциальной форме следующее фундаментальное соотношение, описывающее любой бесконечно малый процесс:
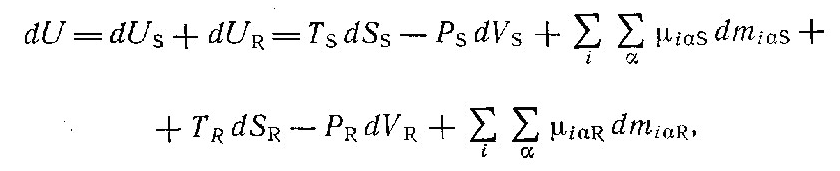 (8.1)
(8.1)
где индексы S и R относятся соответственно к «почве» и «термостату». Общее условие равновесия в сложной системе состоит в том, что полная внутренняя энергия в рассматриваемых условиях должна находиться в относительном минимуме. Это условие следует из второго закона, который указывает, что общим критерием равновесия является существование относительного максимума полной энтропии. Действительно, если бы равновесное состояние соответствовало бы максимуму S и при этом не наблюдался бы минимум U, можно было бы и дальше понижать U, отнимая механическую энергию при фиксированном S. Затем эту механическую энергию можно было бы полностью превратить в тепло, и вернув его обратно в систему, восстановить U до прежнего значения. Однако при этом добавлении тепла возросло бы S, что противоречит исходной гипотезе о максимуме S. Это противоречие означает, что при максимуме S прежде всего должно быть в минимуме U, поэтому воображаемый процесс понижения U невозможен.
Предположим, что между почвой и термостатом происходит перенос бесконечно малого количества тепла. Вследствие природы оболочки, разделяющей обе подсистемы,
dVS = dVR = dmiαR = dmiαS = О
для любого подобного процесса, и уравнение (8.1) сводится к
dU=TSdSS+TRdSR
Поскольку сложная система есть система адиабатическая, она работает в условиях, при которых dSS = —dSR (т. е. теплообмен с внешней средой отсутствует и энтропия не меняется). Поэтому при любых бесконечно малых изменениях
dU = (TS -TR)dSS. (8.2)
Если сложная система первоначально находилась в равновесии, рассмотренный выше бесконечно малый теплообмен представляет собой виртуальный процесс, подчиненный условию dU = 0 — одному из признаков минимума U. Поскольку dSS есть произвольное виртуальное изменение, можно заключить, что в равновесии равен нулю коэффициент при dSS и
Ts = TR. (8.3)
Критерием термического равновесия между почвой и тепловым резервуаром является равенство их абсолютных температур.
Если сложная система первоначально была неравновесной, то бесконечно малый процесс представляет реальный процесс, подчиненный условию dU < 0. Поэтому уравнение (8.2) заменяется неравенством
(TS - TR) dSS < 0. (8.4)
Если теперь dSS > 0, тепловая энергия должна двигаться из резервуара в почву. Неравенство (8.4) в этом случае показывает, что Ts <Tr. С другой стороны, если dSS <0, почва теряет тепло, и это неравенство требует, чтобы было TS > Tr. Следовательно, тепловая энергия всегда переносится из системы с более высокой Т к системе с меньшей Т. В равновесии обе системы имеют одинаковую температуру.
