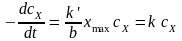- •3. Основные закономерности химических процессов.
- •3.1 Основные понятия и законы химической термодинамики
- •Однородная система – одинаковые химические и физические свойства во всех частях системы.
- •Термическое равновесие (все части системы находятся при одинаковой температуре) есть необходимое условие термодинамического равновесия.
- •3. 2. Характеристические функции
- •3.3. Критерии возможности и направленности самопроизвольного процесса и условия равновесия
- •3.4. Основные термодинамические функции индивидуальных веществ
- •3.5. Термодинамические функции реакций
- •3.5.1. Зависимость теплового эффекта реакции от температуры
- •3.7. Энергия Гиббса смеси. Химический потенциал компонента
- •3.8. Термодинамический закон действующих масс (тздм)
- •3.9. Направление протекания химической реакции. Использование термодинамического закона действующих масс для расчета состава равновесной смеси
- •3.10. Влияние температуры и давления на химическое равновесие
- •3.11. Химическое равновесие в гетерогенных системах.
- •3.12. Химическая кинетика
- •3.13. Константы скоростей химических реакций
- •3.14. Теория (модель) активированного комплекса
- •3.15. Химическая кинетика в гетерогенных системах
- •Выделяют следующие стадии гетерогенного катализа:
Выделяют следующие стадии гетерогенного катализа:
диффузия (или конвекция) участников реакции к поверхности катализатора;
адсорбция (хемосорбция) участников реакции на поверхности;
химические реакции между адсорбированными веществами;
десорбция продуктов реакции;
обратная диффузия (или конвекция) продуктов реакции из зоны реакции.
Подчеркнутые стадии трудно разделить, они являются самыми медленными и определяют скорость процесса.

Рис. 3.6. Основные стадии реакции X Y на поверхности катализатора (К):
хемосорбция реакция десорбция
К + X КX КY К + Y.
Скорость собственно химической реакции пропорциональна адсорбированному количеству вещества X:
xmax – максимальная поверхностная концентрация; k', b – постоянные, зависящие от температуры. |
|
При
малых концентрациях (низкие давления)
b
»
cX
получается уравнение скорости реакции
1-го порядка:
|
При
высоких концентрациях (высокие
давления)
b «
cX
получается уравнение скорости нулевого
порядка:
|
В области давлений между обоими граничными случаями получают дробный порядок реакции между 0 и 1.
Многие поверхностно катализируемые реакции при повышенных температурах могут также параллельно протекать в виде соответствующих гомогенных газовых реакций.
На практике катализаторы внедряют в структуру определенных веществ ("носителей"). Благодаря этому достигается увеличение поверхности, и затрудняются нежелательные эффекты рекристаллизации или спекания катализатора. Малые добавки некоторых веществ (часто – веществ-носителей) могут повысить каталитическую активность катализатора.
Биологически действующими катализаторами являются энзимы, или ферменты (в большинстве случаев – в коллоидной форме). Они состоят из вещества-носителя (чаще всего – белковоподобного тела) и собственно активной группы. Носители, как правило, повышают активность катализатора.
Каталитическое действие энзимов характеризуется резко повышенной селективностью.

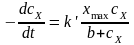 .
Размерность
.
Размерность
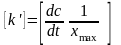 .
.