- •Преждевременное половое развитие: клиника, диагностика, лечение
- •Введение
- •Классификация преждевременного полового развития
- •Истинное преждевременное половое развитие
- •Идиопатическое
- •Церебральное
- •2. Ложное преждевременное половое развитие
- •Врожденная дисфункция коры надпочечников (дефицит 21- и 11β -гидроксилазы)
- •2.2. Стероидсекретирующие опухоли надпочечников
- •2.3. Стероидсекретирующие опухоли гонад
- •2.5. Семейная форма экстрагонадной повышенной активности ароматазы
- •3. Г0над0тр0пиннезависим0е ппр
- •4. Неполные формы преждевременного полового развития
- •4.1. Преждевременное адренархе
- •42. Преждевременное телархе
- •5. Общие принципы диагностики и дифференциальной диагностики различных форм преждевременного полового развития
- •5.1. Процедура теста с лг-рг
- •52. Дифференциальная диагностика преждевременного полового развития
- •Опухоли яичек:
- •Тестотоксикоз:
- •Гранулезоклеточные опухоли яичников:
- •Фолликулярные кисты:
- •6. Лечение преждевременного полового развития
- •6.1. Агонисты лг-рг в лечении истинного ппр
- •62. Лечебная тактика в отношении новообразований цнс
- •6.3. Медикаментозная терапия тонадотропиннезависимых форм ппр
2.5. Семейная форма экстрагонадной повышенной активности ароматазы
Патогенез. Семейная форма экстрагонадной повышенной активности ароматазы проявляется в виде гинекомастии у мальчиков и раннего полового развития у девочек. Заболевание имеет аутосомно-доминантный тип наследования. Причиной заболевания являются мутации гена CYP19, кодирующего фермент Р450-ароматазу. Ароматазная активность широко представлена в различных тканях: гонадах, надпочечниках, мозге, фибробластах кожи, адипоцитах, тканях молочной железы, клетках костной ткани. Повышение экспрессии ароматазы может приводить к значительной экстрагонадной эстрогенемии.
Клиника. Клинические симптомы избыточной эстрогенемии начинают проявляться у детей с 6-7 лет, совпадая с периодом физиологического адренархе. В этот период надпочечники начинают секретировать андрогены: ДГЭА и андростендион. Последний служит источником для периферического ароматизирования и превращения в эстрогены. В настоящее время доказано, что повышенная концентрация эстрогенов у этих больных не является следствием повышенной секреции в гонадах, а опосредована только периферической конверсией андрогенов в эстрогены. У детей обоего пола избыток эстрогенов приводит к значительному ускорению костного возраста и снижению конечного роста. Истинный пубертат у мальчиков задержан. Проведение стимуляционной пробы с ЛГ-РГ не приводит к пубертатному повышению уровня гонадотропинов. Это связано с негативным влиянием избытка эстрогенов на гипоталамо-гипофизарную ось. Объем яичек у взрослых пациентов достигает лишь нижней границы нормы. Фертильность снижена. У женщин с гиперактивностью ароматазы менструальная функция и фертильность не нарушены, но часто наблюдаются макромастия и патологические изменения молочных желез и матки, связанные с гиперэстрогенемией.
Лечение гиперэстрогенемии при повышенной ароматазной активности проводится препаратами, блокирующими активность ароматазы (тестолактон) Однако опыт применения препаратов в подобных случаях ограничен, также отсутствуют сведения о влиянии их длительного применения на ростовой прогноз и гонадотропную функцию.
3. Г0над0тр0пиннезависим0е ппр
Выделение гонадотропиннезависимых форм ППР в самостоятельную патогенетическую форму произошло достаточно недавно, когда расширение диагностических возможностей позволило доказать спонтанную активацию функции гонад без гонадотроп- ной стимуляции и без признаков опухолевого перерождения гонад. Достижения в области молекулярной биологии позволили подойти к пониманию патогенетических процессов, приводящих к уникальной ситуации - спонтанному созреванию половых желез без участия гонадотропного стимула. В настоящее время к гонадотропиннезависимым формам ППР относят два заболевания: синдром Мак-Кьюна-Олбрайта-Брайцева и семейную форму ППР у мальчиков - тестотоксикоз.
Синдром Мак-Кьюна-Олбрайта-Брайцева (МОБ) характеризуется триадой симптомов: пигментными пятнами кофейного цвета с характерными географическими очертаниями, полиостальной фиброзно-кистозной дисплазией и эндокринными нарушениями, самым частым из которых является ППР. Заболевание встречается спорадически и преимущественно у девочек. Отсутствуют сведения о семейных случаях заболевания. Помимо ППР могут встречаться и другие эндокринные нарушения: двусторонняя адреналовая гиперплазия, тиреотоксикоз неиммунного генеза, узловой и диффузный эутиреоидный зоб, гиперпаратиреоз, СТГ-продуцирующие аденомы гипофиза. Описан также целый ряд соматических нарушений: сердечная тахиаритмия, гипербилирубинемия, гастроинстициналь- ный полипоз, гиперплазия тимуса, селезенки, поджелудочной железы. Проявление клинических симптомов при синдроме МОБ чрезвычайно вариабельно.
Патогенез. В настоящее время основным патогенетическим механизмом развития многочисленных органных и метаболических нарушений при синдроме МОБ считают мутацию гена Gsa-протеина (a-субъединицы гуанин-нуклеотидсвязывающего протеина), осуществляющего критическую роль в нормальном трансмембранном сигнале путем связывания рецепторов поверхности клетки к многочисленным лигандам (тройным гормонам, включая ЛГ и ФСГ, нейротрансмиттерам) с внутриклеточным эффектором - аденилатцикла- зой. Появление мутантных форм С-белков приводит к постоянной активации цАМФ, не требующей присутствия тропных гормонов, и автономной гормональной секреции, в частности, эстрогенов в пер- систирующем фолликуле. Аналогичным образом возможна активация и других эндокринных желез при синдроме МОБ. Мутации гена имеют соматический характер, происходят в период раннего эмбриогенеза. Мутантный ген имеет мозаичное распределение, что определяет распространенность и выраженность патологических изменений.
Клинико-гормональная характеристика. Наиболее ярким доклиническим маркером синдрома МОБ являются характерные пигментные пятна, имеющиеся с рождения или появляющиеся в течение первого года жизни. Пятна имеют светло-кофейную окраску и неправильные «географические» очертания. Распределение пятен носит асимметричный характер, наиболее частой зоной локализации являются поясничная область, ягодицы, внутренняя поверхность бедер, лицо, шея (рис. 8). Интенсивность кожных проявлений может служить прогностическим показателем тяжести эндокринных и неэндокринных нарушений при синдроме МОБ.
ППР при этом синдроме имеет ряд клинических особенностей: раннее начало заболевания, преобладание менструального синдрома, медленное прогрессирование костного созревания, спонтанные ремиссии и спонтанные рецидивы. В яичниках обнаруживаются крупные фолликулярные кисты, секретирующие большое количество эстрогенов. В некоторых случаях кисты могут иметь гигантские размеры и многокамерное строение, имитируя опухоль яичников. В большинстве случаев кисты находятся только в одном яичнике. Киста персистирует в течение нескольких недель или месяцев, затем спонтанно регрессирует, что объясняет волнообразный характер клинических проявлений ППР.
Р ис.
8. Больная Д. 11 лет. Синдром Мак-Кьюна-Олбрайта-
Брайцева (пигментные изменения кожи,
типичная деформация бедренной кости
по типу «пастушьего посоха» вследствие
патологического перелома)
ис.
8. Больная Д. 11 лет. Синдром Мак-Кьюна-Олбрайта-
Брайцева (пигментные изменения кожи,
типичная деформация бедренной кости
по типу «пастушьего посоха» вследствие
патологического перелома)
При гормональном обследовании в период активности процесса выявляется чрезвычайно высокий уровень 32. Уровень гонадотропных гормонов низкий, реакция на введение ЛГ-РГ отсутствует. При достижении пубертатного возраста, несмотря на продолжающуюся персистенцию овариальных кист, происходит активация гонадостата, уровень гонадотропных гормонов в ответ на стимуляцию ЛГ-РГ значительно повышается. В некоторых случаях активация гонадотропной функции происходит в допубертатном возрасте, и го- надотропиннезависимый характер ППР сочетается с гонадотропинзависимым. Имеются сообщения о сохраненной фертильности у женщин с синдромом МОБ.
Заболевания щитовидной железы занимают второе после ППР место в эндокринных нарушениях при синдроме МОБ. С наибольшей частотой встречаются случаи узлового зоба, реже - диффузного зоба. Очаговая и диффузная гиперплазия сопровождается тиреотоксикозом, однако могут встречаться и эутиреоидные случаи. Тиреотоксикоз не сопровождается повышением антител к рецептору ТТГ, терапия тиреостатиками не эффективна. Применяются оперативное удаление зоба или радионуклидная терапия. Реже встречаются случаи узловой гиперплазии коры надпочечников с явлениями гиперкортизолизма и СТГ- и пролактин-секретирующие аденомы гипофиза (рис. 9).
Рис.
9. Частота эндокринных и неэндокринных
нарушений при синдроме
МакКьюна-Олбрайта-Брайцева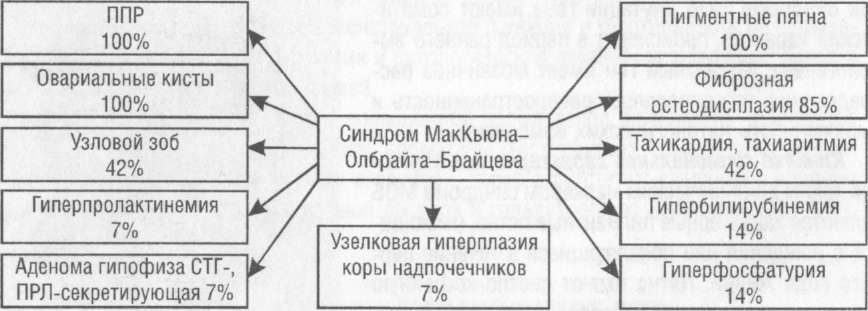
Наиболее тяжелым проявлением синдрома МОБ является фиброзно-кистозная дис- плазия костной ткани, имеющаяся у 80-90% больных. Процесс костно-фиброзной деформации может быть генерализованным, затрагивая почти все кости скелета. Это приводит к многочисленным тяжелым деформирующим переломам. В более легких случаях костные аномалии выявляются лишь рентгенологически (рис. 10). С наибольшей частотой костные нарушения отмечаются в трубчатых костях конечностей, костях свода черепа и лицевого скелета. Процесс повреждения костной ткани имеет тенденцию к асимметрии, распределяясь на стороне тела, имеющей пигментные образования. При отсутствии переломов костные повреждения могут проявляться в виде типичной деформации бедра по типу «пастушьего посоха», дугообразного искривления тибиальных костей и ребер, асимметрии лица. Деформации и переломы являются основными факторами, снижающими конечный рост больных. Конечный рост девочек с синдромом МОБ, не имевших переломов, соответствует 25-50 перцентили.
Среди других неэндокринных проявлений синдрома МОБ с максимальной частотой выявляются кардиоваскулярные нарушения: тахикардия, нарушения сердечного ритма. Эти нарушения могут являться причиной ранней внезапной смерти этих больных.
Тестотоксикоз - семейная форма ППР у мальчиков, характеризующаяся автономной активацией стероидной и фертильной функции яичек без участия гонадотропной стимуляции. Заболевание встречается у лиц мужского пола в одной семье, имеет аутосомно- доминантный тип наследования, возможны спорадические случаи.
Патогенез. Причиной заболевания служит наличие активирующих мутаций в гене рецептора ЛГ, приводящих к повышению сигнальной трансдукции и повышению секреции Т. Наличие мутаций изменяет структуру рецептора, приводя к постоянному связыванию и активации G-протеинового комплекса, стимулирующего пострецепторную активность клетки.
Клинико-гормональная характеристика. Характерно раннее начало и быстрое прогрессирование клинических симптомов ППР. Выраженная андрогенизация приводит к раннему закрытию зон роста и резкому снижению конечного роста больных (рис. 11).
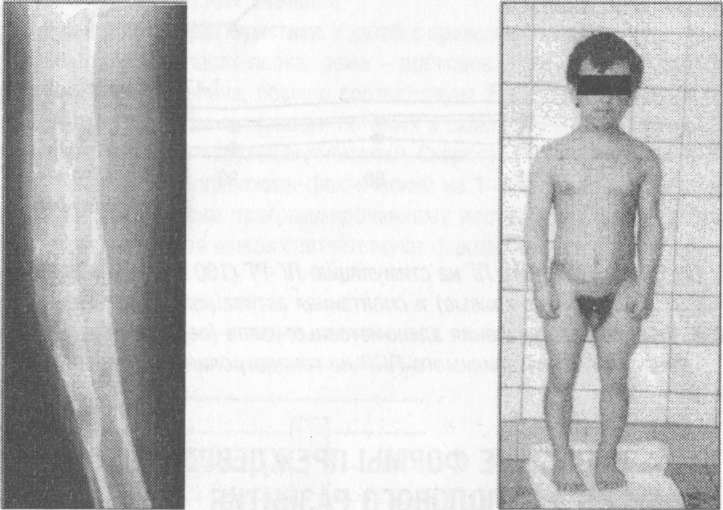
Рис.
10.Рентгенологическая картина фиброзной
стеодисплазии при синдроме
Мак-Кьюна-Олбрайта- Брайцева
Рис.
11. Больной И. (3 года) с гонадотропиннезависимой
формой ППР (тестотоксикоз). Конечный
рост 125 см
При проведении тестикулярной биопсии выявляется преждевременное созревание клеток Лейдига и герменативных клеток с явлениями сперматогенеза. В ряде случаев выявляется односторонняя и двусторонняя аденоматозная гиперплазия клеток Лейдига. Однако у большинства больных объем яичек увеличен незначительно и не соответствует уровню определяемого Т и стадии достигнутого пубертата. Возможной причиной этого несоответствия является первоначальная стимуляция клеток Лейдига; созревание спер- матогенного эпителия, составляющего 60% объема яичек, запаздывает.
При гормональном исследовании выявляют низкие показатели ЛГ и ФСГ - базаль- ные и стимулированные ЛГ-РГ. Уровень Г значительно повышен и соответствует нормам для взрослых мужчин. Однако в пубертатном возрасте устанавливается гипоталамо-ги- пофизарный контроль тестикулярной функции, у взрослых субъектов возможна нормальная фертильность, но описаны случаи развития первичной тестикулярной недостаточности (рис. 12).
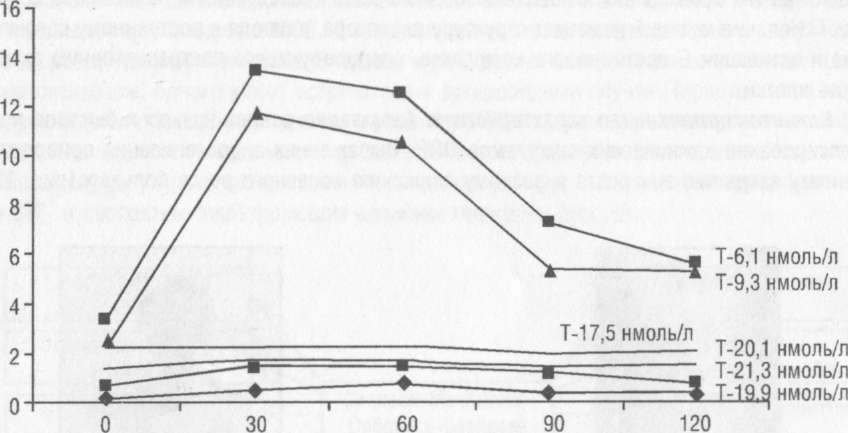
Лг(ЕД/л)
Время
(мин.)
Рис.
12. Динамика ответа ЛГ на стимуляцию
ЛГ-РГ (100 мкг в/в) у мальчиков с
тестотоксикозом (нижние кривые) и
спонтанная активация гонадотропной
функции после оперативного удаления
аденоматозных узлов (верхние кривые).
Смена гонадотропиннезависимого ППР
на гонадотропинзависимое ППР