
- •Преждевременное половое развитие: клиника, диагностика, лечение
- •Введение
- •Классификация преждевременного полового развития
- •Истинное преждевременное половое развитие
- •Идиопатическое
- •Церебральное
- •2. Ложное преждевременное половое развитие
- •Врожденная дисфункция коры надпочечников (дефицит 21- и 11β -гидроксилазы)
- •2.2. Стероидсекретирующие опухоли надпочечников
- •2.3. Стероидсекретирующие опухоли гонад
- •2.5. Семейная форма экстрагонадной повышенной активности ароматазы
- •3. Г0над0тр0пиннезависим0е ппр
- •4. Неполные формы преждевременного полового развития
- •4.1. Преждевременное адренархе
- •42. Преждевременное телархе
- •5. Общие принципы диагностики и дифференциальной диагностики различных форм преждевременного полового развития
- •5.1. Процедура теста с лг-рг
- •52. Дифференциальная диагностика преждевременного полового развития
- •Опухоли яичек:
- •Тестотоксикоз:
- •Гранулезоклеточные опухоли яичников:
- •Фолликулярные кисты:
- •6. Лечение преждевременного полового развития
- •6.1. Агонисты лг-рг в лечении истинного ппр
- •62. Лечебная тактика в отношении новообразований цнс
- •6.3. Медикаментозная терапия тонадотропиннезависимых форм ппр
одностороннее увеличение яичка.
Тестотоксикоз:
низкий базальный уровень гонадотропинов;
отсутствие ответа гонадотропинов на стимуляцию ЛГ-РГ
пубертатный или очень высокий уровень тестостерона;
размер яичек больше допубертатной нормы, но меньше стадии полового развития, возможен одно- или двусторонний аденоматоз.
ДЕВОЧКИ
Истинное преждевременное половое развитие:
пубертатный базальный уровень гонадотропинов;
пубертатный ответ гонадотропинов на стимуляцию ЛГ-РГ, главным образом ЛГ;
увеличение яичников и матки;
при наличии объемного образования ЦНС - характерная КТ или МР-картина.
Периферическое преждевременное половое развитие
Гранулезоклеточные опухоли яичников:
низкий базальный уровень гонадотропинов;
отсутствие ответа гонадотропинов на стимуляцию ЛГ-РГ;
очень высокий уровень эстрадиола;
увеличение яичника при физикальном, ультразвуковом и МРТ-исследовании.
Фолликулярные кисты:
низкий базальный уровень гонадотропинов;
допубертатный характер ответа ЛГ на стимуляцию ЛГ-РГ, но характер ответа ФСГ может быть пубертатным;
уровень эстрадиола может быть как низким, так и высоким, в зависимости от величины овариальных кист;
ультразвуковое исследование выявляет наличие овариальных кист.
6. Лечение преждевременного полового развития
Лечение ППР преследует две основные цели: • подавление развития вторичных половых признаков, вызывающих эмоциональные и психологические проблемы у ребенка и его родителей;
• снижение темпов костного созревания, позволяющее улучшить ростовой прогноз.
К лечению должны быть предъявлены два основных требования: отсутствие токсического влияния используемых препаратов и обратимость их гормоноподавляющего эффекта.
6.1. Агонисты лг-рг в лечении истинного ппр
Значительный прогресс в лечении истинного ППР достигнут с введением в клиническую практику агонистов (аналогов) ЛГ-РГ. Химическое замещение в молекуле природного люлиберина различных аминокислот в положении 6 приводит к увеличению сродства к рецепторам ЛГ-РГ и повышению резистентности к разрушающим его энзимам. Это увеличивает биологическую активность пептидов и продолжительность их действия. Постоянное введение агонистов, поддерживающих их стойкую повышенную концентрацию в циркуляции, приводит к десенситизации гонадотрофов гипофиза, снижению секреции гонадотропных гормонов и, в конечном итоге, снижению секреции половых стероидов. Подобный механизм действия ЛГ-РГ при постоянном введении лежит в основе клинического применения агонистов в лечении истинного ППР (рис. 22).
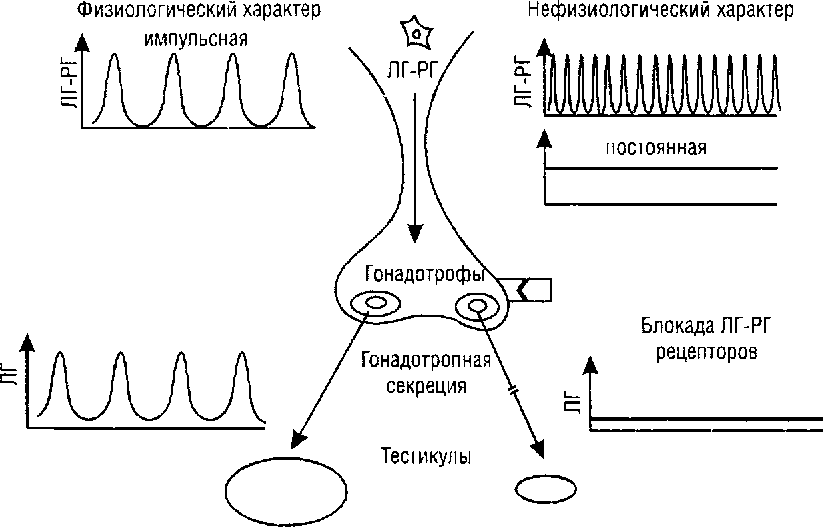
Рис. 22. Механизм антигонадотропного действия аналогов ЛГ-РГ. Импульсный характер секреции ЛГ-РГ стимулирует секрецию гонадотропинов. Поддержание высокой постоянной концентрации ЛГ-РГ приводит к блокаде гонадотропной функции
Все аналоги ЛГ-РГ являются декапептидами и подвержены разрушающему действию пептидаз, поэтому перорапьное введение оказывается неэффективным. Первые генерации аналогов вводились интраназально и подкожно; поддержание уровня постоянной концентрации требовало многократного введения в течение суток, что создавало большие трудности и снижало эффективность лечения.
Революцией в лечении явилось создание депонированных препаратов - агонистов ЛГ-РГ. В настоящее время на российском рынке представлено несколько препаратов - депоаналогов ЛГ-РГ (рис. 23). Наиболее оптимальным для лечения ППР является дифе- релин, представленный фирмой Бофур Ипсен Интернасьональ. Препарат зарегистрирован в России, имеет показания для лечения ППР и с успехом используется в течение последних трех лет. Активной молекулой в диферелине является трипторелин - синтетический аналог, в котором произведена замена аминокислоты /.-глицин в позиции 6 на Д-триптофан (рис. 24). В результате этого изменения трипторелин обладает высокой способностью связываться с ЛГ-РГ рецепторами в гипофизе и является более устойчивым к разрушающему воздействию пептидаз. Полученная молекула в 100 раз активнее натурального пептида и действует более продолжительное время.

Активный компонент трипторелин введен в состав микросфер, содержащих лактид- гликолид-полимер. Это обеспечивает медленное высвобождение активнодействующего трипторелина и поддержание постоянной его концентрации на протяжении четырех недель. Препарат вводится внутримышечно; представлен фирмой-изготовителем в виде готового к употреблению набора, в состав которого входят шприц, содержащий микрокапсулы, и раствор-суспензия. Кратность введения - 1 раз в 28 дней. Доза препарата в среднем должна соответствовать 100 мкг/кг веса. В практике можно рекомендовать всем детям с весом более 30 кг вводить диферелин 3,75 мг (полное содержание препарата в ампуле). Детям с весом меньше 30 кг следует вводить 1,8 мг диферелина.
Для назначения терапии агонистами ЛГ-РГ должны быть использованы следующие критерии:
подтверждение гонадотропинзависимого характера ППР (максимальный подъем ЛГ на стимуляцию ЛГ-РГ > 10 ЕД/л);
быстрое прогрессирование клинических симптомов заболевания (ускорение костного возраста, опережающего фактический на два года и более; ускорение скорости роста более 250 за предшествующий год);
наличие повторных менструаций у девочек до 7 лет и увеличение объема яичек более 8 мл у мальчиков до 8 лет.
Медленно прогрессирующие формы ППР у девочек в возрасте после 5-6 лет не требуют терапии!
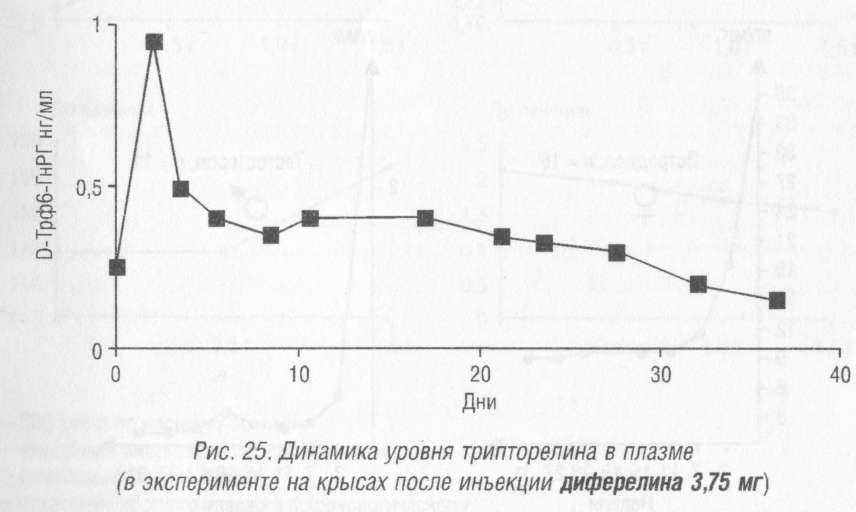
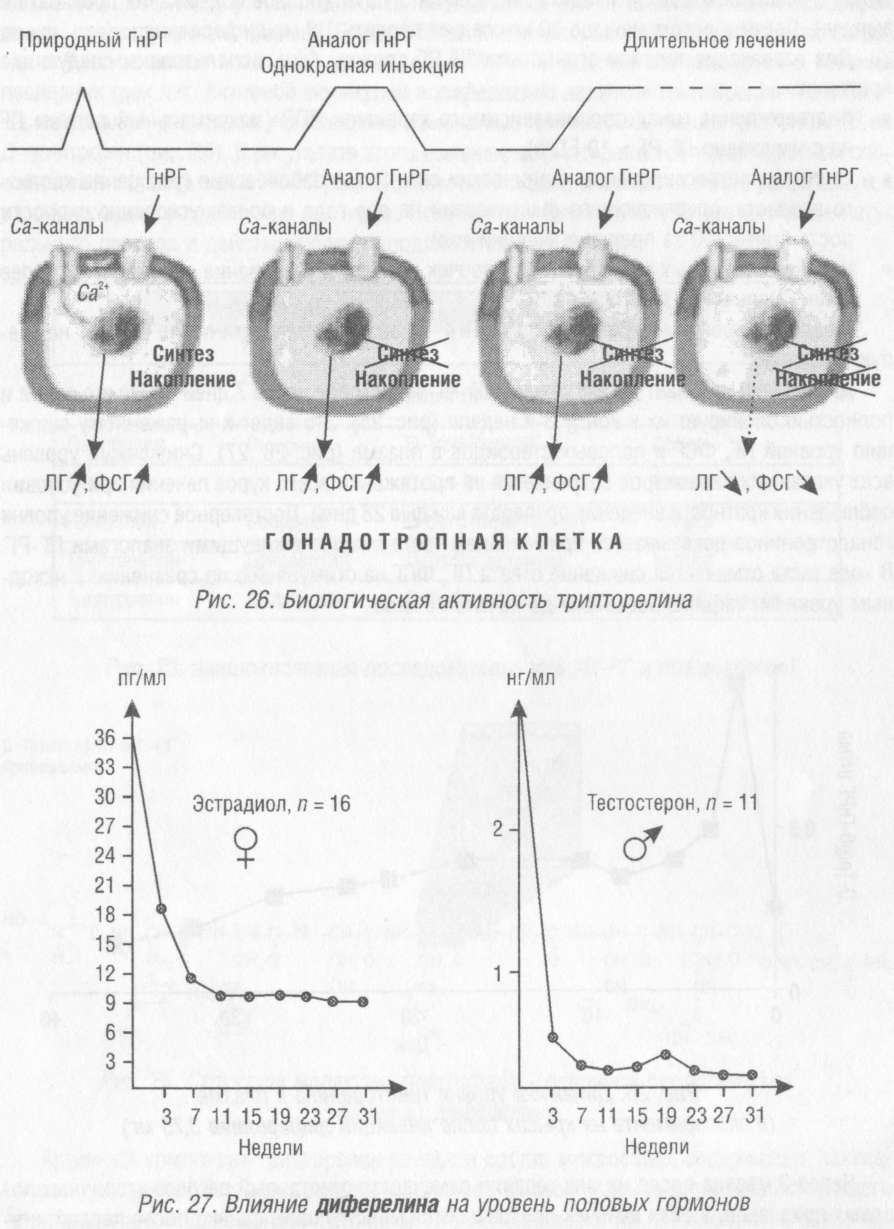
Диферелин начинает дисрегуляцию ЛГ-РГ рецепторов через 7 дней после инъекции и полностью блокирует их к концу 3-й недели (рис. 25). Это ведет к выраженному снижению уровней ЛГ, ФСГ и половых стероидов в плазме (рис. 26, 27). Сниженный уровень всех указанных параметров сохраняется на протяжении всего курса лечения при условии соблюдения кратности введения препарата каждые 28 дней. Достоверное снижение уровня гонадотропинов доказывается применением теста с короткоживущими аналогами ЛГ-РГ. В ходе теста отмечается снижение ответа ЛГ, ФСГ на стимуляцию по сравнению с исходным уровнем, зафиксированным до начала лечения.
Через 3 месяца после начала терапии отмечается отчетливый регресс вторичных половых признаков. У всех девочек прекращаются менструации, однако после первой инъекции возможна менструальная реакция. Уменьшаются объем и интенсивность развития железистой ткани молочных желез, однако не следует ожидать их полного исчезновения. Достоверно снижается объем яичников и уменьшаются размеры матки, к концу первого года лечения эти показатели могут соответствовать допубертатному уровню.
У мальчиков быстро исчезают эрекции, полностью исчезают аспе на коже, улучшается поведение ребенка, снижаются эмоциональная лабильность, аффективность, агрессивность. Стабилизируется развитие вторичного оволосения, но его полного исчезновения не происходит. На фоне лечения объем яичек у мальчиков не прогрессирует, и к концу года терапии можно отметить уменьшение тестикулярного объема. Однако ни у одного из наблюдаемых нами мальчиков не отмечено снижение объема яичек до препу- бертатного уровня.
У детей обоего пола на фоне введения депоаналогов через 1-1,5 года снижается скорость роста с 12-10 до 4-5 см/год, что соответствует норме для фактического возраста ребенка. Параллельно с этим тормозится скелетное созревание. Следует отметить, что у детей, чей костный возраст до начала лечения достигал пубертатных значений (11,5 года у девочек и 12-13 лет у мальчиков), прогресс костного созревания на фоне терапии прекращается. У детей с меньшим костным возрастом возможно его естественное прогрессирование (ежегодное увеличение на 1 см). К концу третьего года лечения отношение костного возраста к хронологическому снижается. Это позволяет надеяться на значительное улучшение ростового прогноза после окончания терапии (рис. 28).
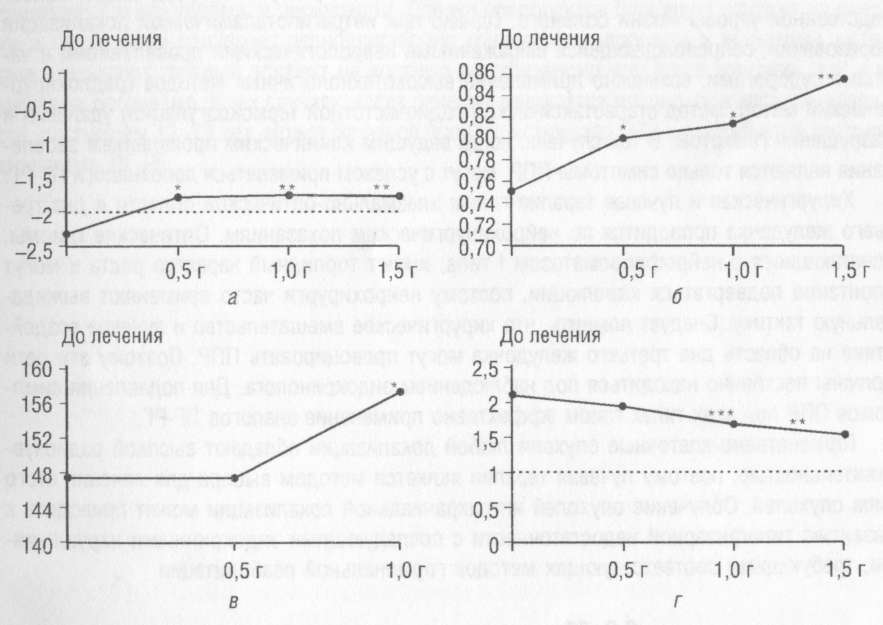
а - SDS роста по костному возрасту
б - отношение ростового возраста к костному
в - ожидаемый конечный рост
г - отношение костного возраста к хронологическому
*Р < 0,05; < 0,01; < 0,001 (по отношению к величине параметра до начала лечения)
Рис. 28. Динамика ростовых показателей у детей на фоне терапии ДД
Необходимо отметить, что подобные изменения более отчетливы у детей с ранним началом лечения, при костном возрасте, не превышающем 12 лет.
Важными аспектами терапии являются быстрая обратимость гонадотропной супрессии и восстановление процессов полового созревания через 3-12 месяцев после отмены лечения.
Препарат хорошо переносится всеми больными, не имеет токсического влияния. За весь период наблюдения нами не отмечено никаких серьезных побочных эффектов, заставляющих прекратить терапию. В ряде случаев наблюдалось увеличение веса больных и вегетативные проявления по типу «приливов», которые проходили через 2-3 месяца терапии. При длительном применении препарата у детей отмечено снижение костной плотности (остеопения). Назначение препаратов кальция и витамина Д3 улучшает минерализацию костной ткани. Необходимо отметить, что все нежелательные эффекты препарата объясняются быстрым снижением уровня половых стероидов и отмечаются только у детей с поздним началом лечения, когда высокий уровень половых гормонов имелся у ребенка в течение 2-3 лет.
