- •Предисловие
- •Тема 1. Введение. Структура курса
- •1.1. Цель и задачи изучения дисциплины. Структура курса.
- •1.2. История развития науки о металлах.
- •1.3. Значение конструкционных материалов и способов их обработки в промышленности и строительном производстве.
- •Тема 2. Строение и свойства металлов
- •2.1. Основные сведения о кристаллическом строении металлических тел.
- •2.2. Типы кристаллической решетки.
- •2.3. Особенности строения кристаллических тел.
- •2.4. Особенности существования кристаллических тел.
- •2.5. Дефекты кристаллического строения.
- •2.6. Изучение макро- и микроструктуры металлов и сплавов.
- •2.7. Свойства металлов и сплавов.
- •2.8. Методы испытания механических свойств.
- •Основные марки строительных сталей и их механические характеристики
- •Механические свойства строительной стали по гост 27772-88*
- •Тема 3. Металлические сплавы
- •3.1. Основные понятия о металлических сплавах.
- •3.2. Диаграмма состояния двойных сплавов.
- •3.2.1. Основная информация о диаграмме состояния.
- •3.2.2. Порядок построения диаграммы состояния.
- •3.3. Железоуглеродистые сплавы.
- •3.3.1. Компоненты и основные структурные составляющие железоуглеродистых сплавов.
- •3.3.2. Характеристика основных точек и линий диаграммы.
- •3.3.3. Структура сталей.
- •3.3.4. Чугуны. Структура чугунов.
- •3.4. Влияние углерода и легирующих элементов на свойства стали.
- •3.5. Цветные металлы и их сплавы.
- •Тема 4. Производство черных и цветных металлов
- •4.1. Основные понятия в металлургии.
- •4.2. Основные способы получения металлов из руд.
- •4.3. Топливо и огнеупорные материалы металлургического производства.
- •4.4. Производство чугуна.
- •4.4.1. Материалы для выплавки чугуна.
- •4.4.2. Подготовка исходных материалов к плавке.
- •4.4.3. Доменный процесс.
- •4.5. Производство стали.
- •4.5.1. Кислородно-конвертерный способ.
- •4.5.2. Выплавка стали в мартеновских печах.
- •4.5.3. Выплавка стали в электрических печах.
- •4.5.4. Разливка стали.
- •4.6. Производство цветных металлов.
- •4.6.1. Производство алюминия.
- •4.6.2. Производство меди.
- •4.6.3. Производство титана.
- •Тема 5. Обработка металла давлением
- •5.1. Общие сведения.
- •5.2. Прокатное производство.
- •5.3. Волочение.
- •5.4. Прессование.
- •5.5. Свободная ковка.
- •5.6. Горячая объемная штамповка.
- •5.7. Холодная объемная штамповка.
- •5.8. Листовая штамповка.
- •Тема 6. Термическая и химико-термическая обработка стали
- •6.1. Превращения при нагреве стали.
- •6.2. Превращения в стали при охлаждении.
- •Характеристика структурных составляющих закаленной стали
- •6.3. Основные виды термической обработки стали.
- •6.4. Химико-термическая обработка сталей.
- •Тема 7. Углеродистые и легированные стали. Классификация, свойства, применение
- •7.1. Классификация сталей.
- •1. По структуре:
- •2. По способу производства:
- •3. По химическому составу.
- •4. По качеству.
- •5. По степени раскисления.
- •6. По назначению:
- •7.2. Конструкционные стали.
- •7.2.1. Углеродистые стали обыкновенного качества.
- •7.2.2. Углеродистые и легированные качественные стали.
- •7.2.3. Стали высококачественные и особо высококачественные.
- •7.2.4. Цементуемые углеродистые и легированные стали.
- •7.2.5. Улучшаемые углеродистые и легированные стали.
- •7.2.6. Высокопрочные легированные стали.
- •7.2.7. Рессорно-пружинные стали.
- •7.2.8. Шарикоподшипниковые стали.
- •7.2.9. Износостойкие стали.
- •7.3. Инструментальные стали.
- •7.4. Легированные стали специального назначения.
- •7.5. Стали, применяемые для конструкций зданий и сооружений.
- •Марки стали, заменяемые сталями по гост 27772-88
- •7.6. Определение марки стали экспресс-методом.
- •Тема 8. Общие сведения о коррозии металлов
- •Список литературы
- •Содержание
- •Тема 1. Введение. Структура курса 5
- •Тема 2. Строение и свойства металлов 15
- •Тема 3. Металлические сплавы 32
- •Тема 4. Производство черных и цветных металлов 50
- •Тема 5. Обработка металла давлением 68
- •Тема 6. Термическая и химико-термическая обработка стали 87
- •Тема 7. Углеродистые и легированные стали. Классификация, свойства, применение 99
- •Тема 8. Общие сведения о коррозии металлов 115
- •«Металлы и сварочные работы в строительстве»
- •«Технология металлов»
Тема 3. Металлические сплавы
3.1. Основные понятия о металлических сплавах.
В технике в чистом виде металлы практически не применяются, зачастую используют металлические сплавы, под которыми понимаются сложные вещества, состоящие из двух и большего числа компонентов. В состав металлических сплавов, кроме металлов, могут входить и неметаллы – углерод, марганец, кремний, фосфор, сера и др.
Металлические сплавы, как и чистые металлы, имеют характерную кристаллическую решетку, т.е. являются кристаллическими веществами. Однако их свойства (механические, химические, технологические и др.) могут значительно отличаться от свойств чистых (исходных) металлов.
Наиболее распространенным способом получения сплавов является сплавление входящих в него компонентов, в результате чего получают механическую смесь, твердый раствор или химическое соединение.
1
Рис.
3.1. Микроструктура
механической смеси (схема)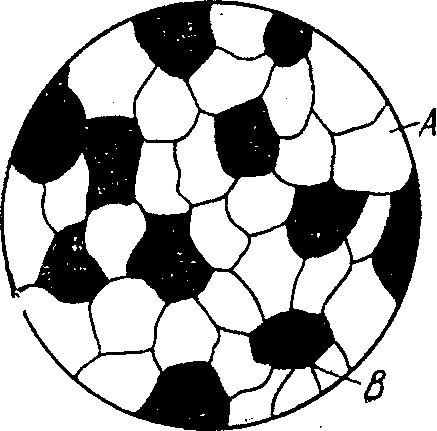
2. Твердый раствор образуется тогда, когда компоненты сплава обладают взаимной растворимостью друг в друге как в жидком, так и в твердом состоянии. Твердый раствор – однородное кристаллическое тело, имеющее один тип кристаллической решетки.
Различают следующие виды твердых растворов:
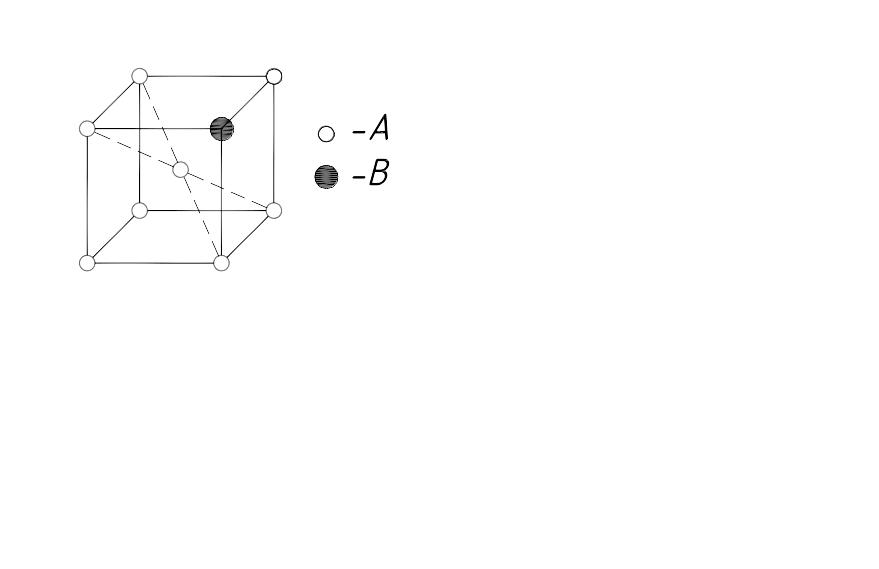
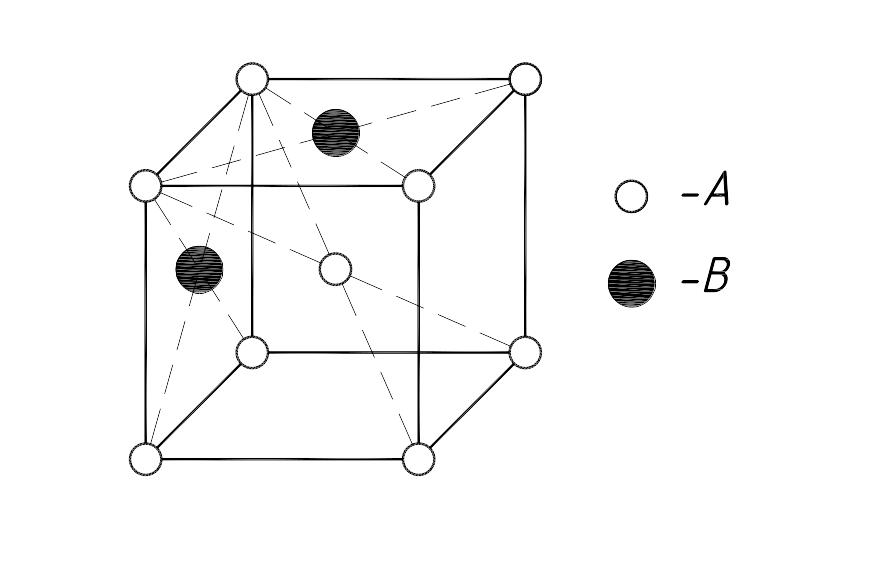
2.1. Твердый раствор замещения – когда атомы В растворенного элемента замещают атомы А растворителя в его кристаллической решетке (рис. 3.2,а).
2.2. Твердый раствор внедрения – когда атомы В растворенного элемента размещаются между атомами А растворителя в его кристаллической решетке (рис. 3.2,б).
2.3. Твердый раствор вычитания – образуется на базе химического соединения, когда атомы растворенного элемента замещают атомы растворителя в узлах кристаллической решетки, но отдельные узлы остаются не занятыми (пустыми). Примером может служить коррозия железа.
а)
б) |
|
Рис. 3.2. Кристаллическая решетка а – твердого раствора замещения; б – твердого раствора внедрения |
|
3. Химическое соединение образуется в том случае, когда составляющие его компоненты (металлы или неметаллы) вступают между собой в химическое взаимодействие (реакцию). В результате образуется сплав, имеющий новый вид кристаллической решетки и обладающий определенными специфическими свойствами, которые в значительной степени отличаются от решеток и свойств исходных компонентов. Пример: Fe- (ГЦК) + С (гексагональная кристаллическая решетка) = Fe3С (ромбическая кристаллическая решетка).
3.2. Диаграмма состояния двойных сплавов.
3.2.1. Основная информация о диаграмме состояния.
Диаграмма состояния представляет собой графическое изображение состояния сплава в зависимости от температуры и концентрации компонентов. Она позволяет определить температуру начала и конца кристаллизации (перекристаллизации) сплава, его структуру в различных интервалах температур и превращения, которые сплав претерпевает при охлаждении и нагревании.
Двойными называются сплавы, в состав которых входят два компонента.
Компоненты – это вещества, образующие систему, или другими словами, это химические составляющие сплавов.
Различные изменения системы, происходящие в зависимости от внешних условий (температуры, концентрации компонентов), подчиняются правилу фаз (закону Гиббса), которое устанавливает зависимость между числом компонентов, числом фаз и числом степеней свободы системы.
Фазой называется однородная часть системы, отделенная от других частей поверхностью раздела, при переходе через которую химический состав или структура сплава изменяются скачкообразно. Чаще всего, когда работают с металлами или сплавами, различают твердую или жидкую фазы.
Под числом степеней свободы (вариантность) системы понимают число внешних и внутренних факторов (температура, давление, концентрация), которое можно изменять без изменения числа фаз данной системы.
Правило фаз (закон Гиббса) для металлических систем при постоянном давлении выражается уравнением
С = К + 1 – Ф, (3.1)
где С – число степени свободы системы;
К – число компонентов, образующих систему;
Ф – число фаз, находящихся в равновесии.
В процессе затвердевания чистого металла (К = 1, Ф = 2) – система нонвариантная (безвариантная), так как, согласно формуле (3.1), С = 0. Т.е. в системе нельзя произвольно изменять внешний фактор (температуру), не изменяя числа фаз и равновесия системы.
Чистый расплавленный металл (К = 1, Ф = 1) представляет моновариантную (одновариантную) систему с одной степенью свободы (С = 1). Сохраняя металл в жидком виде, можно в определенных пределах (выше точки плавления) изменять температуру, не изменяя числа фаз и равновесия системы.
Если двухкомпонентная система (сплав) находится в расплавленном состоянии (К = 2, Ф = 1), то имеем две степени свободы(С = 2), т.е. систему бивариантную (двухвариантную). В этом случае существуют различные температуры и концентрации компонентов, при которых не изменяется число фаз и равновесие системы. Для этой же системы при наличии двух фаз (жидкой, и твердой) имеем К = 2, Ф = 2 и С = 1, т.е. с изменением температуры концентрация должна быть строго определенной.