
- •Химические загрязнения в биосфере и их определение
- •Глава 1. Вредные вещества биосферы
- •Загрязнение воздуха
- •1.1.1 Методы анализа и методы снижения поступления в атмосферу токсичных веществ
- •1.2 Загрязнение воды
- •1.2.1 Методы очистки и контроль сточных вод
- •Твердые отходы. Безотходное производство
- •1.4. Химические элементы и их влияние на организм человека
- •Глава 2 качественный анализ
- •Теоретическое введение
- •Дополнительные методы исследования
- •Экспериментальная часть
- •Опыт 1. Характерные реакции на отдельные катионы и анионы
- •Лабораторная работа 2 качественный функциональный анализ органических соединений Теоретическое введение
- •Экспериментальная часть
- •Опыт 1. Кислородсодержащие органические соединения
- •1) Качественные реакции на спирты
- •2) Качественные реакции на фенолы
- •3) Качественные реакции на альдегиды и кетоны
- •4) Качественные реакции на карбоновые кислоты
- •Опыт 2. Аминосодержащие органические соединения
- •1) Получение медной соли глицина
- •2) Осаждение белка солями тяжелых металлов
- •3) Денатурация белка
- •4) Цветные реакции белков
- •Глава 3 количественный анализ Принципы количественного анализа
- •3.1 Титриметрический анализ
- •3.1.1 Способы выражения концентрации растворов и расчеты в объемном анализе
- •3.1.2 Классификация методов объёмного анализа по типу реакции, лежащей в основе титрования
- •1. Метод нейтрализации (кислотно-основное титрование)
- •2. Окислительно-восстановительное титрование
- •А) Перманганатометрическое определение
- •Б) Иодометрическое определение
- •3. Метод комплексонометрии
- •Лабораторная работа 3 кислотно – основное титрование
- •Опыт 1. Определение концентрации гидроксида натрия в растворе
- •Опыт 2. Определение концентрации соляной кислоты в растворе
- •Лабораторная работа 4 окислительно – восстановительное титрование
- •Лабораторная работа 5 комплексометрическое титрование
- •Лабораторная работа 6 определение перманганатной окисляемости
- •Лабораторная работа 7 определение концентрации формальдегида в растворе
- •3.2 Физико-химические методы анализа
- •3.2.1 Фотоколориметрия
- •3.2.2 Визуальная колориметрия. Метод стандартных серий
- •3.2.3 Фотоколориметрия с использованием прибора кфк-2мп
- •3.2.4 Построение калибровочного графика данного вещества
- •Лабораторная работа 8 определение и очистка фенола в сточных водах
- •Лабораторная работа 9 фотоколориметрическое определение концентрации никеля в сточных водах
- •Лабораторная работа 10 фотоколориметрическое определение концентрации хрома (IV) в сточных водах
- •Лабораторная работа 11 фотоколориметрическое определение концентрации железа (II) и (III) в воде
- •Лабораторная работа 12 определение ионов аммония в сточных вода
- •Лабораторная работа 13 нефелонометрическое определение хлорид иона в сточных водах
- •Лабораторная работа 14 определение поверхностно – активных веществ (пав) в сточной воде
- •Лабораторная работа 15 определения нитрат ионов в почве
- •Лабораторная работа 16 определение аэрозоля серной кислоты и растворимых сульфатов
- •Заключение
- •Список литературы
- •Химические загрязнения биосферы и их определение
Экспериментальная часть
Цель работы: с помощью качественных реакций определить наличие функциональной группы и определить принадлежность к определенным классам органических веществ.
Опыт 1. Кислородсодержащие органические соединения
1) Качественные реакции на спирты
В пробирку поместите маленький кусочек металлического натрия, добавьте 3-5 капель изопропилового спирта и закройте отверстие пробирки пробкой. Начинается выделение водорода. По окончании реакции поднесите к пробирке горящую спичку, уберите пробку, водород воспламеняется, образуя колечко голубого цвета.
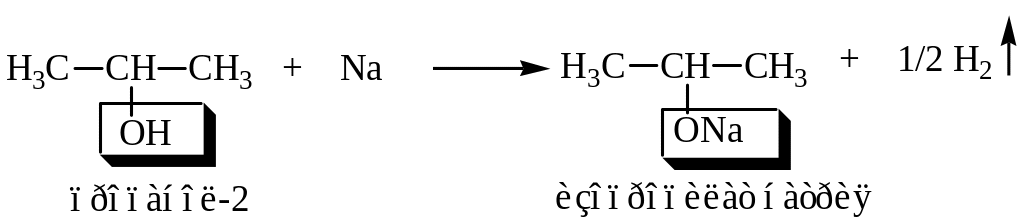
К изопропилату натрия добавьте немного воды и 2-3 капли фенолфталеина. Какая среда в полученном растворе?
2) Качественные реакции на фенолы
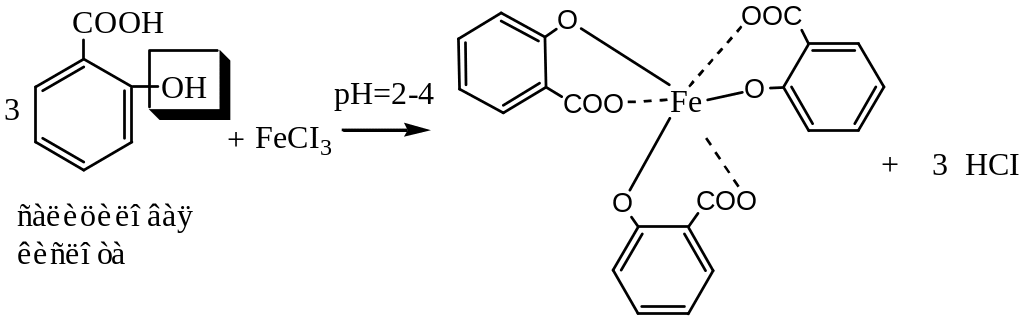
Поместите в пробирку 1 мл раствора салициловой кислоты (OHС6H4COOH) и добавьте 1-2 капли 2%-го раствора хлорида железа (III), появляется сине-фиолетовое окрашивание комплексного соединения железа при рН = 2-4.
3) Качественные реакции на альдегиды и кетоны
а) Обнаружение ацетона
Эта реакция обнаружение карбонильной группы связанной с метильным радикалом (-СОСН3)
Поместите в пробирку 1 каплю йода в растворе иодида калия и 5 капель 10% раствора NaOH, произойдет обесцвечивание раствора, затем добавьте 1 каплю раствора ацетона, появляется иодоформ –желтовато-белый осадок с характерным запахом.
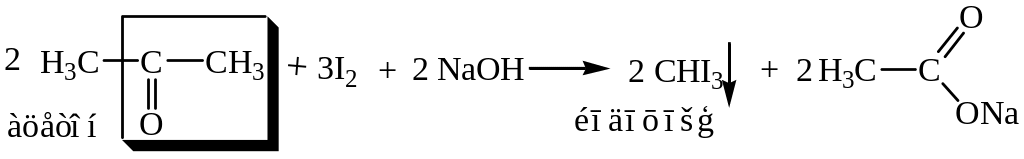
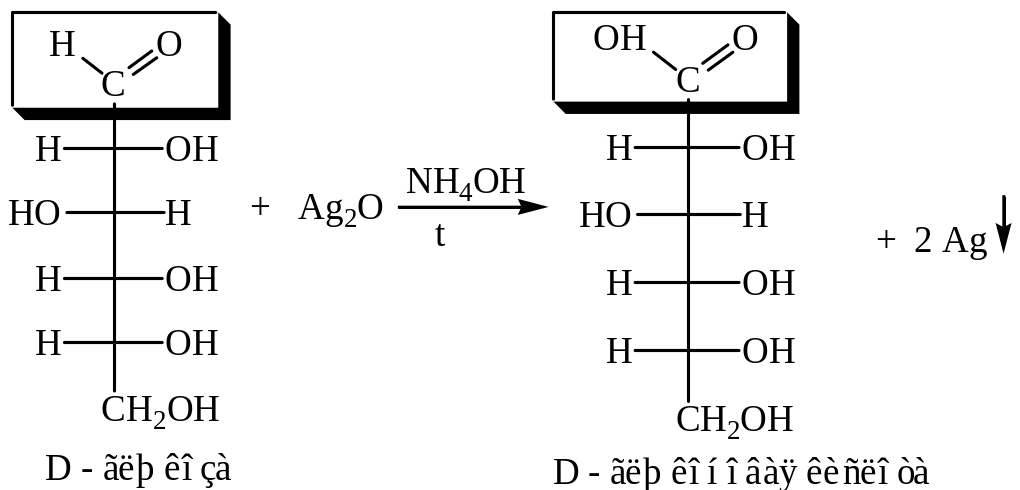
б) Восстановление аммиачного раствора оксида серебра глюкозой (реакция «серебряного зеркала»)
В пробирку поместите 4 капли 0,5%-го раствора глюкозы, добавьте 4-5 капель аммиачного раствора оксида серебра, пробирку слегка нагрейте, далее серебро выделяется на стенках в виде зеркального налета.
в) Качественное обнаружение гидроксильных групп в глюкозе
Поместите в пробирку 1 каплю 1%-го раствора глюкозы, 6 капель 10%-го раствора NaOH и 1 каплю 2%-го раствора медного купороса. Образующийся в начале осадок гидрата окиси меди (II) немедленно растворяется с образованием прозрачного раствора комплексного соединения синего цвета.

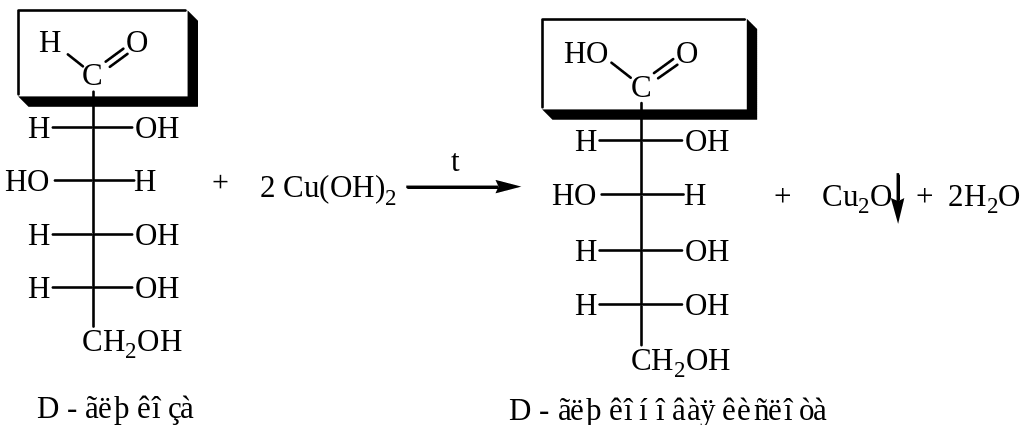
г) Восстановление гидрата окиси меди глюкозой
К полученному в предыдущем опыте раствору синего цвета добавьте несколько капель воды и нагрейте до кипения. Синий цвет раствора меняется на оранжево-красный, так как образуется осадок оксида меди (I).
4) Качественные реакции на карбоновые кислоты
а) Взаимодействие карбоновых кислот с металлами
В три пробирки приливают по 1 мл уксусной кислоты. В одну пробирку помещают стружки магния, в другую – цинка, в третью – железной или медной проволоки. Что наблюдается в каждой из пробирок? Какой газ выделяется? Напишите уравнения реакции.
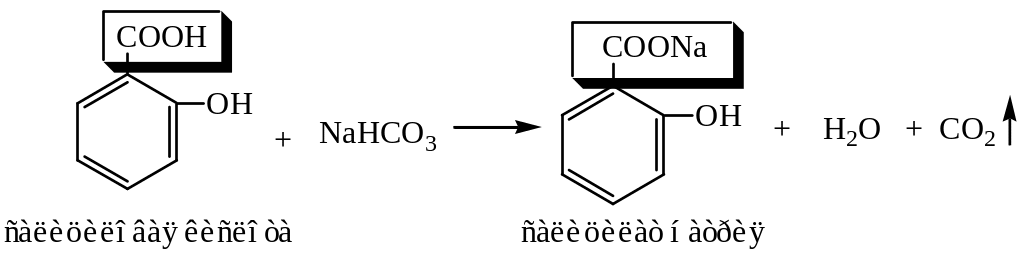
б) Реакция карбоновых кислот с гидрокарбонатом натрия (NaHCO3)
В пробирку поместите 1 мл раствора салициловой кислоты и добавьте 2 мл насыщенного раствора гидрокарбоната натрия. При наличии гидроксильной группы выделяются пузырьки CO2.
Опыт 2. Аминосодержащие органические соединения
К аминосодержащими органическим соединениям относят классы соединений: амины, α-аминокислот, пептиды, белки.
Проведем качественные реакции с α-аминокислотой (глицином) и яичным белком. В таблице 2.12 показано строение некоторых незаменимых α-аминокислот. Пептиды и белки представляют собой высокомолекулярные органические соединения, построенные из остатков α-аминокислот, соединенных между собой пептидными связями (-СО-NH-). Пептиды и белки различают в зависимости от величины молекулярной массы. Условно считают, что пептиды содержат в молекуле до 100 (соответствует молекулярной массе до 10000), а белки – свыше 100 аминокислотных остатков (молекулярная масса от 10000 до нескольких миллионов).
Таблица 2.12 – Строение некоторых α-аминокислот H2N-CH(R)-COOH
Аминокислота |
Сокращенное обозначение |
-R |
1 |
2 |
3 |
Глицин |
Gly |
-H |
Аланин |
Ala |
-CH3 |
Цистеин |
Cys |
-CH2-SH |
Серин |
Ser |
-CH2-OH |
Фенилаланин |
Phe |
-CH2-C6H5 |
1 |
2 |
3 |
Тирозин |
Tyr |
|
Глутаминовая кислота |
Glu |
-CH2-CH2-COOH |
Лизин |
Lys |
-(CH2)4-NH2 |
