
- •10. Теория переходного состояния
- •21. Ступенчатая диссоциация электронов
- •28. Комплексные соединения. Основные положения теории Вернера. Тип химической связи в комплексных соединениях.
- •29. Диссоциация комплексных соединений в водных растворах (типы диссоциации, ступени диссоциации). Привести примеры.
- •33. Электрохимические процессы. Механизм возникновения тока в гальваническом элементе. Устройство и принцип работы медно-цинкового гальванического элемента (Якоби-Даниэля).
- •34. Стандартный электродный потенциал. Уравнения Нернста. Эдс гальванического элемента.
- •37. Электрохимическая коррозия: классификация, условия протекания.
- •38. Атмосферная коррозия
- •Виды атмосферной коррозии
- •Особенности протекания атмосферной коррозии металлов
- •Уравнение атмосферной коррозии:
- •Свойства лакокрасочных материалов
- •Свойства лакокрасочных покрытий
- •Виды лакокрасочных материалов (лкм)
- •Состав лакокрасочных материалов
- •Классификация лакокрасочных материалов
- •42. Электролиз. Схема электролизной установки. Причины электролиза. Анод. Катод. Их заряды при электролизе.
- •54. Химическая связь.
- •Методы умягчения воды
- •70. Двенадцать принципов зелёной химии
- •Основные промышленные группы полимеров, синтезируемых поликонденсацией
33. Электрохимические процессы. Механизм возникновения тока в гальваническом элементе. Устройство и принцип работы медно-цинкового гальванического элемента (Якоби-Даниэля).
Электрохимические процессы – это процессы сопровождающиеся возникновением электрического тока, или сами вызываемые им.
Механизм возникновения тока в гальваническом элементе:
![]()
Действие любого гальванического элемента основано на протекании в нем окислительно-восстановительной реакции. В простейшем случае гальванический элемент состоит из двух пластин или стержней, изготовленных из различных металлов и погруженных в раствор электролита. Такая система делает возможным пространственное разделение окислительно-восстановительной реакции: окисление протекает на одном металле, а восстановление — на другом. Таким образом, электроны передаются от восстановителя к окислителю по внешней цепи.
Устройство и работа медно-цинкового гальванического элемента Якоби-Даниэля.
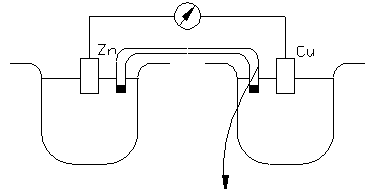
Внутренняя цепь гальв. элем.
(солевой мостик)
Медно-цинковый гальванический элемент работает за счет энергии реакции между цинком и сульфатом меди. Элемент Якоби — Даниэля состоит из медной пластины, погруженной в раствор сульфата меди (медный электрод), и цинковой пластины, погруженной в раствор сульфата цинка (цинковый электрод). Оба раствора соприкасаются друг с другом (солевой мостик).
При работе элемента, т. е. при замкнутой цепи, цинк окисляется: на поверхности его соприкосновения с раствором атомы цинка превращаются в ионы и, гидратируясь, переходят в раствор. Высвобождающиеся при этом электроны движутся по внешней цепи к медному электроду. Вся совокупность этих процессов схематически изображается уравнением полуреакции, или электрохимическим уравнением;
Zn = Zn2+ + 2e-
На медном электроде протекает восстановление ионов меди. Электроны, приходящие сюда от цинкового электрода, соединяются с выходящими из раствора дегидратирующимися ионами меди; образуются атомы меди, выделяющиеся в виде металла. Соответствующее электрохимическое уравнение имеет вид:
Си2+ + 2е- == Си
Гальванические элементы. Катод. Анод. Схема гальванического элемента. Процессы, протекающие на катоде и аноде.
Приборы и устройства которые используются для преобразования энергии хим. реакции в электрическую энергию называются гальваническими элементами или источниками электрической энергии.
В гальваническом элементе протекает ОВР разделенный на два процесса. На одном электроде процесс окисления, на другом – восстановление.
Анод – это электрод, на котором протекает процесс окисления (знак - )
Катод - – это электрод, на котором протекает процесс восстановления (знак + )
Гальванический элемент (Якоби-Даниэля) состоит из:
медной пластины, погруженной в раствор сульфата меди (медный электрод)
цинковой пластины, погруженной в раствор сульфата цинка (цинковый электрод)
оба раствора соприкасаются друг с другом (солевой мостик).
Процессы, протекающие на катоде и аноде:
На аноде протекает процесс окисления.
На катоде протекает процесс восстановления.
