
- •Министерство образования рф
- •Кафедра теоретической и экспериментальной физики
- •Законы геометрической оптики как следствия теории Максвелла. Интерференция волн и света. Расчет интерференционной картины от двух когерентных источников
- •Основы геометрической оптики
- •Законы геометрической оптики
- •Предварительные сведения
- •II пара или
- •Световая волна. Основные характеристики световой волны
- •Энергия электромагнитных волн
- •Давление света
- •Отражение и преломление плоской волны на границе двух диэлектриков
- •Интерференция света
- •Интерференция от двух волн
- •Пространственная и временная когерентность световых волн
- •Пространственная когерентность
- •Способы наблюдения интерференции. Интерференция в тонких пленках
- •Интерферометры
- •Кольца Ньютона
- •Дифракция волн и света
- •Зоны Френеля
- •Дифракция от круглого отверстия
- •Дифракция от круглого диска
- •Дифракция Фраунгофера
- •Дифракционная решетка
- •Характеристики дифракционной решетки
- •Дифракция рентгеновских лучей
- •Понятие о голографии
- •Дисперсия света
- •Элементы Фурье-оптики. Групповая скорость
- •Элементарная теория дисперсии
- •Поглощение света
- •Рассеяние света
- •Эффект Вавилова-Черенкова
- •Поляризация света. Естественный и поляризованный свет
- •Поляризация при отражении и преломлении
- •Интерференция поляризованных лучей
- •Искусственное двойное лучепреломление
- •Вращение плоскости поляризации
- •Магнитное вращение плоскости поляризации
- •Квантовая природа излучения
- •Элементы квантовой механики
- •Соотношение неопределенностей
- •Т ак как очень мало (1,05 10-34 Дж с), то соотношение неопределенностей проявляет себя ярко в микромире.
- •Волновая функция
- •Временное и стационарное уравнение Шрёдингера
- •Частица в одномерной яме с абсолютно непроницаемыми стенками
- •Элементы атомной физики
- •Модель атома водорода Бора
- •Квантовомеханическая модель атома водорода
- •Векторная модель атомов
- •Превращение атомных ядер Законы радиоактивного распада
- •Активность радиоактивного вещества
- •- Распад
- •- Распад
- •Искусственная радиоактивность, ядерные реакции
- •Законы сохранения ядерных реакций
- •Основные характеристики элементарных частиц
- •3. Изотопический спин
- •Библиографический список
Векторная модель атомов
Д вижение
электронов в других атомах (помимо H)
определяется теми же квантовыми числами
(можно и n, l,
j, mj).
Но влияние на движение электрона других
электронов приводит к тому. Что его
энергия зависит и от числа l
(кроме n).
вижение
электронов в других атомах (помимо H)
определяется теми же квантовыми числами
(можно и n, l,
j, mj).
Но влияние на движение электрона других
электронов приводит к тому. Что его
энергия зависит и от числа l
(кроме n).
Механические и магнитные моменты атомов складываются из орбитальных и спиновых моментов отдельных электронов.
Возможны два случая:
1. Если орбитальные
моменты
![]() связаны между собой сильнее, чем с
связаны между собой сильнее, чем с
![]() и
наоборот (такая связь называется
LS-связью), то все
моменты
складываются в суммарный орбитальный
момент атома
и
наоборот (такая связь называется
LS-связью), то все
моменты
складываются в суммарный орбитальный
момент атома
![]() ,
а все
в
суммарный спиновый момент
,
а все
в
суммарный спиновый момент
![]() .
А потом находится полный момент атома
.
А потом находится полный момент атома
![]() .
.
Результирующий орбитальный момент импульса для SL-связи
![]()
где L – орбитальное квантовое число атома.
Для двух
электронов
![]()
Проекция момента импульса атома на некоторое напр-е
![]()
![]()
Также и для полного спинового момента
![]()
S – в зависимости от четного или нечетного числа электронов
![]()
Тогда полный орбитальный момент атома
![]()
![]()
![]()
Векторная
модель строится по следующим правилам.
Пусть известен модель момента импульса
и его одна проекция М и Мz
(Мx и
Мy – не
определены). Следовательно,
![]() может
иметь направление одной из образующих
конуса (совершает прецессию).
может
иметь направление одной из образующих
конуса (совершает прецессию).
То, что проекция полного момента атома квантуется, было доказано опытами в 1922 году Штерном и Герлихом.
Состояние
электронов в атомах позволяет объяснить
принцип Паули (1925 г.): в одном и том же
атоме (или другой квантовой системе) не
может быть двух электронов (либо других
частиц со спином
![]() ),
обладающих одинаковой совокупностью
квантовых чисел. (В одном и том же
состоянии не могут находится 2 электрона).
),
обладающих одинаковой совокупностью
квантовых чисел. (В одном и том же
состоянии не могут находится 2 электрона).
Тогда кратность
выражения уровня будет определяться
![]()
|
|
|
Оболочка |
На уровне с энергией |
n = 1 |
2 эл. |
K |
|
n = 2 |
8 эл. |
L |
|
n = 3 |
18 эл. |
M |
|
n = 4 |
32 эл. |
N |
|
n = 5 |
50 эл. |
O |
|
|
|
P |
Принцип Паули дает объяснение периодической повторяемости свойств атомов.
Принцип запрета Паули
Состояние электронов в атомах позволяет объяснить принцип Паули (1925 г.): в одном и том же атоме (или другой квантовой системе) не может быть двух электронов (либо других частиц со спином ), обладающих одинаковой совокупностью квантовых чисел. (В одном и том же состоянии не могут находится 2 электрона).
В
таблице все возможные квантовые состояния
атома водорода и соответствующие им
ориентации орбитального
![]() и спинового
и спинового
![]() моментов электрона. Стрелками обозначены
направления векторов. Учет приводит к
тому, что уровни энергий, описываемые
формулой (
моментов электрона. Стрелками обозначены
направления векторов. Учет приводит к
тому, что уровни энергий, описываемые
формулой (![]() ),
расщепляются на несколько уровней,
соответствует нескольким значениям
),
расщепляются на несколько уровней,
соответствует нескольким значениям
![]() и
и
![]() .
.
Распределение
электронной плотности для состояний с
заданным главным числом
![]() ,
но с разными значениями орбитального
и магнитного
,
но с разными значениями орбитального
и магнитного
![]() - квантовых чисел, существенно отличаются.
Хотя, согласно формуле (
- квантовых чисел, существенно отличаются.
Хотя, согласно формуле (![]() ),
им соответствует одна и та же энергия
(
),
им соответствует одна и та же энергия
(![]() ).
).
Такая
ситуация, когда одному и тому же
энергетическому уровню
![]() соответствует
несколько различных квантовых состояний
систем (волновые функции
соответствует
несколько различных квантовых состояний
систем (волновые функции
![]() отличаются значениями
и
),
называется вырождением уровня энергии.
отличаются значениями
и
),
называется вырождением уровня энергии.
Уровень
энергии называется невырожденным, если
ему отвечает лишь одно состояние
и
![]() ,
кратно вырожденным, если система в
различных состояниях имеет одинаковую
энергию.
,
кратно вырожденным, если система в
различных состояниях имеет одинаковую
энергию.
В
атоме водорода при заданном числе
орбитальное квантовое число
может принимать
значений
![]() ,
а магнитное квантовое число
изменяется в пределах:
,
а магнитное квантовое число
изменяется в пределах:
![]() и следовательно принимает
и следовательно принимает
![]() значений.
значений.
Поэтому кратность вырождения - уровня энергии определяется суммой арифметической прогрессии.
![]()
если
учесть наличие спина у электрона, то
![]() .
.
Элементы физики твердого тела ЛЕКЦИЯ № 12
1.Тепловые свойства твердого тела
При сближении атомов до расстояния, когда начинают действовать молекулярные силы, энергетические уровни отдельных атомов расщепляются (двухатомная молекула).
Из графика следует, что спектры молекул должны быть сложнее одиночных атомов. Молекулярные спектры ”полосатые”.
В первом приближении атомы кристаллической решетки можно рассматривать как систему шариков, соединенные невесомыми пружинками и способных колебаться в 3-х направлениях.
Гармонический
осциллятор
![]() ,
,
![]() .
.
Изменение
энергии
![]() .
.
Фонон
– это квант тепловой энергии кристаллической
решетки, равной
![]() .
Фонон как частица не существует. Такого
рода частицы называют квазичастицами.
.
Фонон как частица не существует. Такого
рода частицы называют квазичастицами.
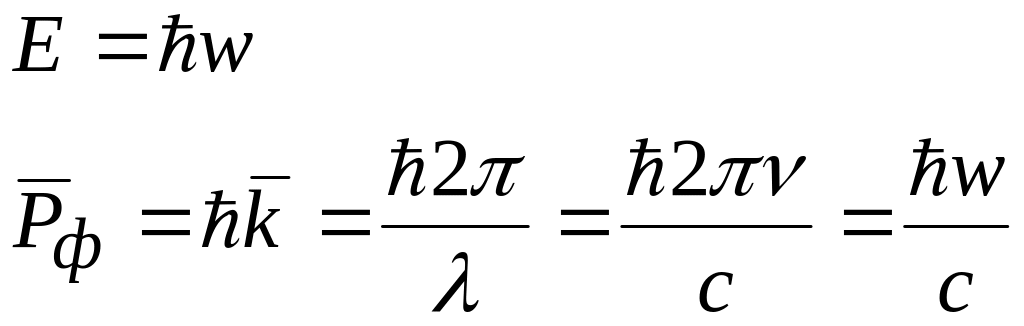
Поскольку фононы – это квазичастицы, то они не могут существовать в вакууме, а существуют только в твердом теле.
Фононы можно рассматривать как фононный газ. Можно говорить, что теплоемкость кристалла определяется фононным газом.
Среднее число фононов при заданной энергии:
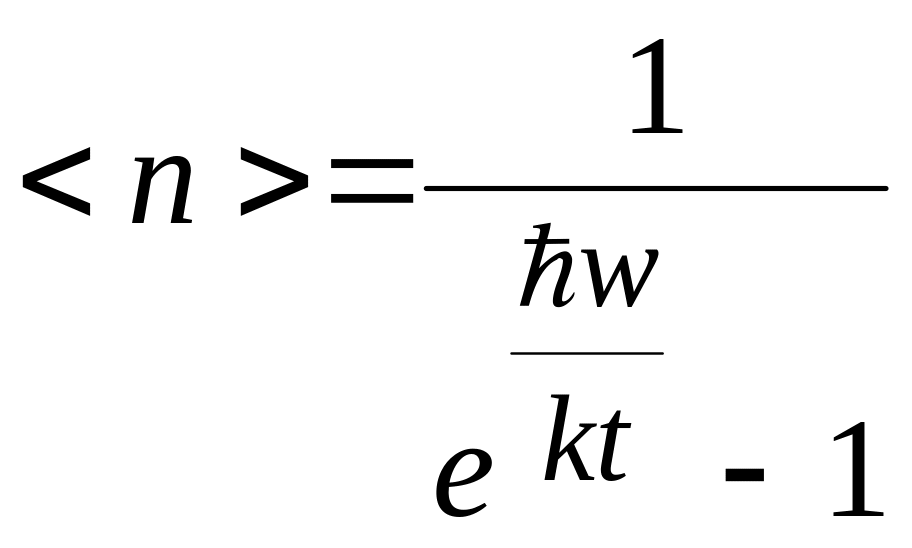 .
.
Отсюда следует, что число фононов не ограничено. Оно растет с ростом температуры. Принцип запрета Паули не работает для фононов. Фононы взаимодействуют друг с другом, с деффектами кристаллической решетки, с электронами, фотонами. Взаимодействие фононов с электронами при низких температурах. Электроны притягиваются друг к другу, появляется сверхпроводимость.
Количество
фононов:
![]() ,
,
![]() -
количество существующих фононов, т.е.
фононы любят накапливаться.
-
количество существующих фононов, т.е.
фононы любят накапливаться.
По характеру поведения в коллективе все микрочастицы можно разделить на 2 группы: фермионы и бозоны.
К
фермионам относятся электроны, протоны,
нейтроны и другие частицы с полуцелым
спином -
![]() .
.
К
бозонам относятся фотоны, фононы и
другие частицы, обладающие целочисленным
спином -
![]() .
В коллективе фермионы проявляют ярко
выраженное стремление к ”уединению”.
Если данное квантовое состояние уже
занято фермионом, то никакой другой
фермион данного типа не может находиться
в этом состоянии.
.
В коллективе фермионы проявляют ярко
выраженное стремление к ”уединению”.
Если данное квантовое состояние уже
занято фермионом, то никакой другой
фермион данного типа не может находиться
в этом состоянии.
В этом заключается известный принцип Паули, которому подчиняются фермионы. Бозоны, напротив, обладают стремлением к ”объединению”. Они могут неограниченно заселять одно и то же состояние, при чем делают это тем охотнее, чем их больше в этом состоянии.
Фермионы подчиняются статистике Ферми–Дирака, а бозоны – Бозе-Эйнштейна.
3.Теория теплоемкости твердых тел
А. Эйнштейна (1907г.)
Согласно
классическим представлениям,
кристаллическую решетку можно
рассматривать, как состоящую из
![]() -осцилляторов,
где
-осцилляторов,
где
![]() - число атомов твердого тела. Можно
считать, что энергия одного осциллятора
- число атомов твердого тела. Можно
считать, что энергия одного осциллятора
![]() .
.
Предполагается, что энергия может принимать непрерывные значения. Приняв, что распределение энергии осциллятора подчиняется больцмановскому распределению по энергиям
![]() .
.
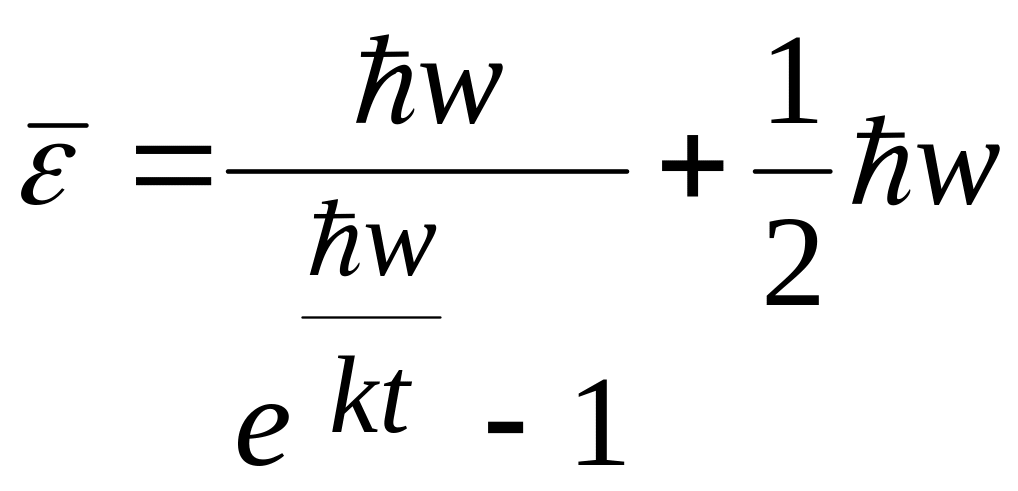 .
.
Эйнштейн не учел нулевой энергии.
 ,
,
![]()
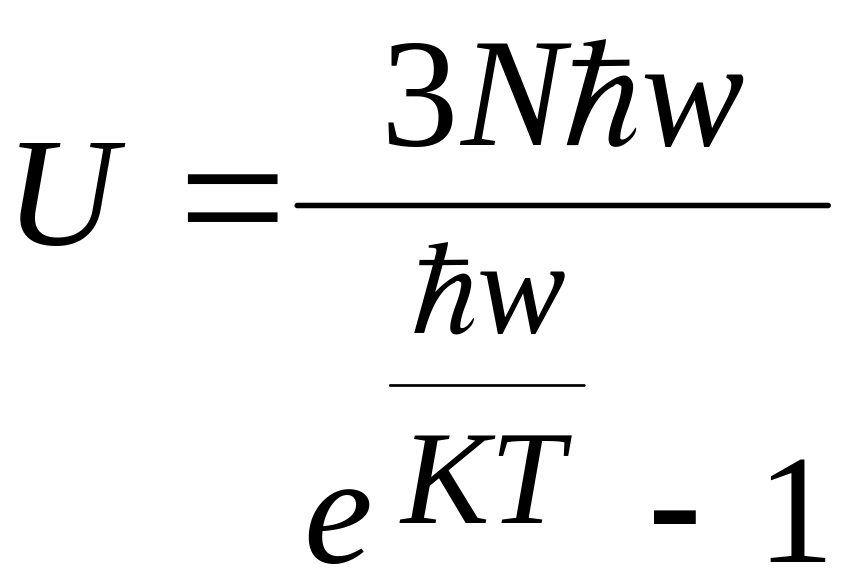
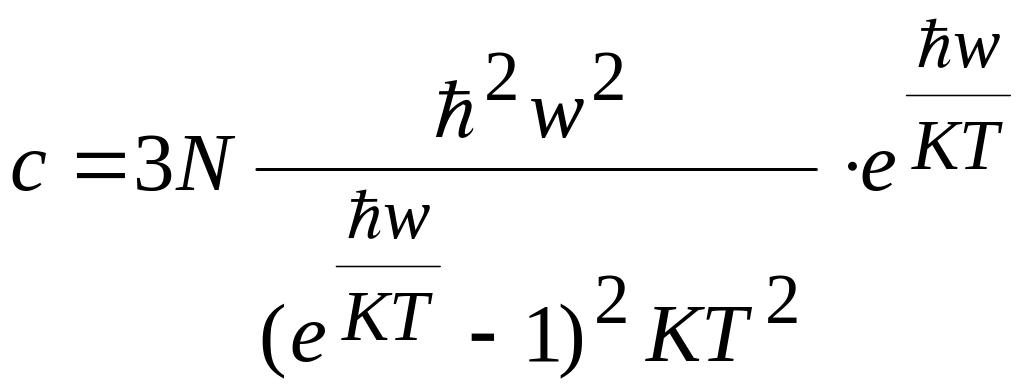 .
.
В
1819г. Дюлонг (1785-1838) и Пти (1791-1820) установили
закон:
![]() .
.
Рассмотрим 2 предельных случая:
Случай высоких температур.
![]() ,
то
,
то
![]() ;
;
![]() ,
то
,
то
![]() ,
то
,
то
![]() - а такого быть не может.
- а такого быть не может.
Разложим
 ;
;
![]() ;
;
![]() .
.
Если
подставим, то получим:
![]() - закон Дюлонга - Пти.
- закон Дюлонга - Пти.
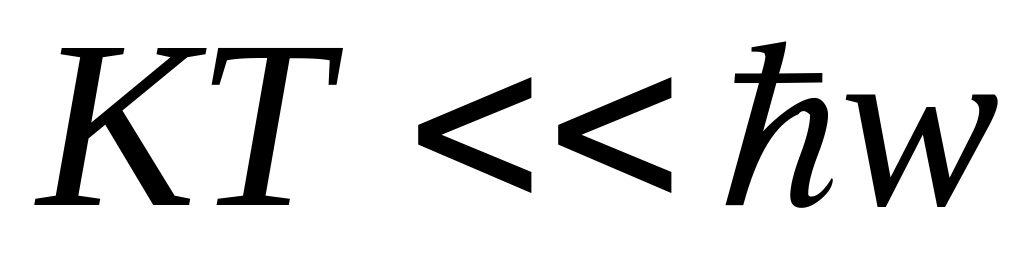 ,
то в формуле теплоемкости единицей
можно пренебречь.
,
то в формуле теплоемкости единицей
можно пренебречь.
 .
.
Экспоненциальный
множитель изменяется быстрее, и по
Эйнштейну получается теплоемкость
твердого тела к 0 должна подходить по
экспоненте. На самом же деле теплоемкость
к 0 приближается, как
![]() .
Т.е. в области низких давлений Эйнштейн
не прав.
.
Т.е. в области низких давлений Эйнштейн
не прав.
4.Теория теплоемкости Дебая
Теплоемкость,
рассчитанная по Эйнштейну, падает с
температурой быстрее, чем это в
действительности. Эксперимент показал,
что диэлектрики имеют теплоемкость
(при
![]() ),
изменяющуюся как
.
Расхождение эксперимента с теорией
связано с тем, что в модели твердого
тела предполагалось, что каждый атом
совершает колебания с частотой
),
изменяющуюся как
.
Расхождение эксперимента с теорией
связано с тем, что в модели твердого
тела предполагалось, что каждый атом
совершает колебания с частотой
![]() независимо от других атомов. На самом
деле атомы в твердом теле не могут
колебаться с одной и той же частотой,
поскольку они сильно связаны между
собой.
независимо от других атомов. На самом
деле атомы в твердом теле не могут
колебаться с одной и той же частотой,
поскольку они сильно связаны между
собой.
Дебай (1884-1966) в 1912г. сделал шаг в развитии теории теплоемкости. Он рассматривал твердое тело, состоящее из одинаковых атомов, как сплошную упругую среду, тепловое движение в которой сводится к аккустическим колебаниям всевозможных частот, распространяющихся упругих волн.
Основную идею Эйнштейна Дебай сохранил, дополнив ее предложением о том, что гармонические осцилляторы колеблются с различными частотами, а их энергия квантуется по Планку.
Пусть
из слоя
![]() выбит один электрон, который покидает
атом, т.е. появляется энергетическая
вакансия, которая может быть заполнена
разными способами, например, либо из
выбит один электрон, который покидает
атом, т.е. появляется энергетическая
вакансия, которая может быть заполнена
разными способами, например, либо из
![]() -слоя,
либо из
-слоя,
либо из
![]() -слоя,
либо из
-слоя.
Тогда, если имеется множество атомов с
вакансией в
-слое,
то возможны серии переходов:
-слоя,
либо из
-слоя.
Тогда, если имеется множество атомов с
вакансией в
-слое,
то возможны серии переходов:
![]() ,
,
![]() и т.д.;
и т.д.;
![]() ,
,
![]() и т.д. Переходы на место в
-слое
из дальних слоев сопровождаются
излучением спектральных линий:
и т.д. Переходы на место в
-слое
из дальних слоев сопровождаются
излучением спектральных линий:
![]() ;
;
![]() и т.д.;
и т.д.;
![]() ;
;
![]() .
.
Эти спектры используют при микрорентгеноспектральном анализе.
( Квантовые источники излучения - лазеры самостоятельно).
Основы теории ядра ЛЕКЦИЯ № 13
Согласно современным представлениям атомное ядро состоит из протонов и нейтронов, которые объединяются общим названием нуклонами.
1.Протон (от греч. Protos)
термин был введен Резерфордом. Обозначается
![]() .
Является стабильной частицей с временем
жизни
.
Является стабильной частицей с временем
жизни
![]() лет
лет
![]() кг
кг
Однако чаще всего масса элементарных
частиц указывается в
![]()
![]()
Таким образом,
![]() считается больше, а масса е
считается больше, а масса е
![]()
Протон имеет собственный спин
![]()
2. Нейтрон (от латин. Neuter – ни тот, ни другой)
![]() -
нейтральная частица. Был предсказан
теоретически, а затем обнаружен
экспериментально в 1932 году английским
физиком Чедвиком.
-
нейтральная частица. Был предсказан
теоретически, а затем обнаружен
экспериментально в 1932 году английским
физиком Чедвиком.
![]() (в энергетических единицах)
(в энергетических единицах)
![]()
![]()
3. Основные характеристики ядра.
Заряд ядра определяется количеством p в ядре и характеризуется зарядовым числом Z (порядковый номер элемента в таблице Мнделеева)
Число нуклонов протеинов и нейтронов численно равна массовому числу А.
Массовым числом называется ближайшее к массе атома целое число и выражается в а.е.м., которое определяется
![]()
![]()
Таким образом, любой элемент таблицы Менделеева отображается в следующем виде:
![]()
n = количество нейтронов.
4. Радиус-вектор зависит от числа содержащихся в нем нуклонов. Опыты показали, сто средняя плотность нуклонов для всех ядер приблизительно одинаковы, следовательно, объем ядра ~ массовому числу, а следовательно
![]()
![]() см.
см.
В настоящее время принято
![]() см
см
![]()
![]()
Проведенные опыты по рассеиванию -частиц на ядрах показали,. Что радиус действия ядерных сил больше радиуса. В котором распределены нуклоны.
Последняя формула для радиуса ядер имеет вид:
![]()
5. Масса ядра.
В настоящее время существует множество моделей атомных ядер, а следовательно множество формул, связывающих массы ядер с их составом. Однако в первом приближении все модели приводят к выводу, что масса ядра ~ массовому числу
![]()
- постоянная
отсюда следует, что плотность ядерного вещества приблизительно одинакова для всех ядер.
Если ядро состоит из p и n, то масса ядра должна быть связана с их массами. Измерение масс ядер показывает, что масса ядра всегда меньше суммы масс исходных нуклонов. Разность между массой всех исходных частиц и массой ядра называется дефектом масс:
![]()
Это означает, что при образовании ядра часть массы исходных частиц должна передаваться окружающей среде в виде энергии, которая согласно Эйнштейну
![]() - называется энергией связи.
- называется энергией связи.
и показывает, какую энергию необходимо затратить для расщепления ядра на составные части.
Более важной характеристикой ядра называется удельная энергия связи, то есть энергия связи, приходящаяся на 1 нуклон
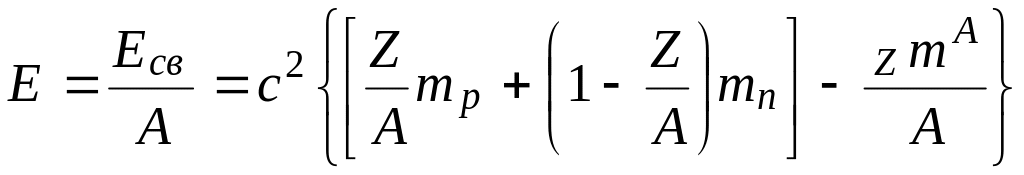
О казалось,
что Е зависит от массового числа
А.
казалось,
что Е зависит от массового числа
А.
То есть существуют ядра химических
элементов, в которых
![]() велика. Это ядра с массовыми числами
50-60, для которых энергия связи около 9
Мэв.
велика. Это ядра с массовыми числами
50-60, для которых энергия связи около 9
Мэв.
а)
![]()
В таких ядрах р и п-ны наиболее плотно упакованы, поэтому больше, чем в среднем.
б) Все точки для средней энергии связи на нуклон ложатся на гладкую кривую, за исключением ядер с магическими числами.
Они, как правило, с зарядовым числом
![]()
rколичество протонов
Либо с числом нейтронов
![]()
Но существует ядра, у которого Z и N входят в ряд магических чисел, тогда ядро мы назовем дважды магическим.
Это
![]()
![]()
![]()
![]()
![]()
