
- •Содержание
- •1. Теоретическая часть
- •1.1. Открытие углеродных нанотрубок и распространённость нанотрубок в природных и технологических средах
- •1.2. Основные типы и структура углеродных нанотрубок
- •1.3. Основные способы получения углеродных нанотрубок
- •1.4. Свойства и применение углеродных нанотрубок
- •1.4.1. Механические свойства
- •1.4.2. Баллистический транспорт в наноразмерных системах
- •1.4.3. Полупроводниковые нанотрубки
- •1.4.5. Использование асм для работы с нанотрубками
- •1.4.7. Топливные элементы на основе углеродных нанотрубок
- •1.5. Методы расчетов электронной структуры
- •1.6. Зонная структура углеродных нанотрубок
- •1.6.1. Метод сильной связи
- •1.6.2. Расчеты зонной структуры углеродных нанотрубок методом сильной связи
- •1.6.3. Другие методы расчета углеродных нанотрубок
- •1.6.4. Экспериментальные данные по зонной структуре нанотрубок
- •1.7. Метод функционала плотности
- •1.7.1. Принцип минимума функционала энергии в терминах волновых функций уравнения Шредингера
- •1.7.2. Плотность электронных состояний
- •1.7.3. Теоремы Хоэнберга – Кона
- •1.7.4. Самосогласованные уравнения Кона – Шэма и обменно-корреляционная энергия
- •1.7.5. Приближение lda
- •2. Практическая часть
- •2.1. Программное обеспечение, используемое в работе
- •2.1.1. Программный комплекс Gaussian
- •2.1.2. Базисные наборы в Gaussian
- •2.1.3. Программное обеспечение TubeGen
- •2.1.4. Файлы заданий в Gaussian
- •2.1.5. Этапы расчета
- •2.2. Задания
- •2.3. Задания для самостоятельной работы
- •2.4. Вопросы
- •2.4. Рекомендуемая форма отчётности
- •3. Рекомендуемая литература
1.4.7. Топливные элементы на основе углеродных нанотрубок
Углеродные нанотрубки могут быть использованы в изготовлении батареек. Литий, являющийся носителем заряда в некоторых батарейках, можно помещать внутрь нанотрубок. По оценкам, в трубке можно разместить один атом лития на каждые шесть атомов углерода. Другим возможным использованием нанотрубок является хранение в них водорода, что может быть использовано при конструировании топливных элементов как источников электрической энергии в будущих автомобилях. Топливный элемент состоит из двух электродов и специального электролита, пропускающего ионы водорода между ними, но не пропускающего электроны. Водород направляется на анод, где он ионизируется. Свободные электроны движутся к катоду по внешней цепи, а ионы водорода диффундируют к катоду через электролит, где из этих ионов, электронов и кислорода образуются молекулы воды. Такой системе необходим источник водорода. Одна из возможностей состоит в хранении водорода внутри углеродных нанотрубок. По существующим оценкам, для эффективного использования в этом качестве трубка должна поглощать 6,5% водорода по весу. В настоящее время в трубку удалось поместить только 4% водорода по весу.
1.5. Методы расчетов электронной структуры
Наиболее удобным, с точки зрения квантовой химии, является такой метод расчета структуры и свойств молекул, который использовал бы информацию только о конфигурации электронных оболочек атомов, составляющих систему. Реализация такого метода позволила бы исследователям предсказывать существование и свойства новых материалов, еще не полученных в эксперименте, например, сверхтвердых материалов и др.
Ab initio, т. е. первопринципные методы, используют вышеописанный принцип, однако из-за высокой сложности расчета в них применяются некоторые приближения, которые не позволяют применить эти методы к любым системам. При этом точность расчета в большинстве случаев довольно высока.
К основным методам расчета из первых принципов можно отнести следующие:
– метод Хартри – Фока и его дальнейшие развития;
– метод функционала электронной плотности.
Метод
Хартри – Фока, или метод самосогласованного
поля, является одним из эффективных
методов решения задач квантовой химии.
Его идея состоит в том, что взаимодействие
электрона с его окружением заменяется
взаимодействием с неким усредненным
полем
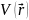 .
Таким образом, не решаемая квантовомеханическая
задача многих тел сводится к решению
одночастичного уравнения
.
Таким образом, не решаемая квантовомеханическая
задача многих тел сводится к решению
одночастичного уравнения
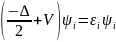 (где Δ – оператор Лапласа).
(где Δ – оператор Лапласа).![]()
В
методе функционала плотности вместо
волновых функций электронов
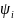 используется электронная плотность –
функция трех пространственных переменных
используется электронная плотность –
функция трех пространственных переменных
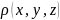 .
Затем находится минимум энергии,
являющейся функционалом от электронной
плотности. Это позволяет существенно
упростить задачу и рассчитывать системы
из десятков и сотен электронов.
.
Затем находится минимум энергии,
являющейся функционалом от электронной
плотности. Это позволяет существенно
упростить задачу и рассчитывать системы
из десятков и сотен электронов.
Решения уравнения Хартри – Фока без использования каких-либо других приближений лежат в основе неэмпирических методов расчета, которые отличаются используемым базисом атомных орбиталей. При использовании этих методов основные затраты машинного времени (около 70 %) направлены на вычисление интегралов межэлектронного взаимодействия оператора Фока. По мере увеличения размеров молекулы число таких интегралов возрастает примерно пропорционально N4, где N – число базисных функций. Соответственно этому растут время и стоимость расчета.
Наиболее перспективными являются методы, основанные на замене большей части интегралов параметрами, вычисленными с помощью данных, взятых из эксперимента (потенциалами ионизации атомов в орбитальных валентных состояниях и др.), и использовании различных приближенных выражений для оценки интегралов. Основанные на этом подходе методы называются полуэмпирическими.
Среди полуэмпирических методов расчета можно выделить следующие:
– метод молекулярных орбиталей Хюккеля;
– расширенный метод Хюккеля;
– метод сильной связи.
Даже после появления таких быстрых алгоритмов, как семейство O(N)–алгоритмов, время счета в которых пропорционально количеству атомов в системе, системы, насчитывающие 104 – 106 атомов, невозможно просчитать на уровне решения уравнения Шредингера или его аналогов (уравнения Хартри – Фока, Кона – Шэма) для волновых функций электрона. Решение таких уравнений требует проведения огромного количества вычислений для матричной диагонализации и поэтому практически нереально для систем вышеперечисленных размеров. Современные же технологии, особенно нанотехнологии, фармацевтика и микробиология, требуют возможности рассчитывать системы, насчитывающие десятки тысяч атомов и выше, пусть даже и с минимумом получаемой информации, например – полной энергии системы. При этом часто возникает потребность выполнения молекулярно-динамических расчетов, где поведение системы моделируется в дискретном времени с шагом порядка 1.0 фемтосекунды (10–15 с) и в течение времени, много большего обратной частоты фононных колебаний, обычно 10–6 – 10–9 с, что на несколько порядков замедляет проведение расчетов. Зато при этом моделируется поведение системы при любой заданной температуре с минимальными погрешностями.
Из вышесказанного следует, что огромные системы практически невозможно просчитать на уровне вычисления волновых функций электронов, и поэтому для них применяются методы, базирующиеся на эмпирическом знании потенциалов взаимодействия атомов или ионов, без вычисления электронных волновых функций или плотностей.
Основными эмпирическими методами расчета электронной структуры являются:
– метод парных потенциалов;
– метод многочастичных потенциалов;
– метод молекулярной динамики.
