
- •Третичный вторичный первичный.
- •Задачи (алканы)
- •Задачи (алкены)
- •2. С какими из приведенных соединений реагируют бутен-1 в указанных условиях?
- •H2o, 20c; 7) Br2 / 20c (в темноте); 8) hBr. 9) Na . Напишите уравнения реакций.
- •Задачи (алкины)
- •Задачи (диены)
- •Лабораторная работа № 2
- •Задачи (арены)
- •Галогенопроизводные
- •Лабораторная работа № 3
- •Задачи (галогенопроизводные)
- •Спирты и фенолы
- •Лабораторная работа № 4
- •Задачи (спирты, фенолы)
- •Задачи (амины)
- •Альдегиды и кетоны
- •Лабораторная работа № 5
- •Задачи (альдегиды и кетоны)
- •Карбоновые кислоты
- •Лабораторная работа №6
- •Задачи (карбоновые кислоты)
- •Задачи (оксикислоты)
- •Аминокислоты
- •Задачи (аминокислоты)
- •Углеводы
- •Лабораторная работа №7
- •Задачи (углеводы)
Лабораторная работа № 2
Опыт 1. Свойства толуола: растворимость в воде, взаимодействие с бромной водой и раствором перманганата калия.
А) Налейте в пробирку 2 мл толуола и 2 мл воды. Встряхните пробирку. Смесь расслаивается. Толуол в воде не растворяется. Обратите внимание на то, что толуол легче воды.
Б) В две пробирки налейте по 2 мл толуола и добавьте в одну 2 мл бромной воды, а в другую – 2 мл раствора перманганата калия. Обе пробирки встряхните.
Наблюдения и выводы запишите в лабораторный журнал.
Опыт 2. Бромирование толуола.
А) Налейте в пробирку 2 мл толуола и 2 мл бромной воды. Смесь нагрейте на водяной бане в течение 5 минут (до полного обесцвечивания бромной воды). Опустите полоску фильтровальной бумаги в раствор. Затем выньте ее и подсушите. Образовавшийся бромистый бензил можно обнаружить по резкому запаху. Наблюдения и выводы запишите в лабораторный журнал.
Б) Налейте в пробирку 2 мл толуола, 2 мл бромной воды и прибавьте на кончике шпателя немного железных опилок. Смесь нагрейте на водяной бане в течение 5 минут (до полного обесцвечивания бромной воды). Опустите полоску фильтровальной бумаги в раствор. Затем выньте ее и подсушите. Образовавшиеся орто- и пара-бромтолуол обнаруживается по характерному ароматическому запаху.
Наблюдения и выводы запишите в лабораторный журнал.
Опыт 3. Нитрование толуола.
В плоскодонную колбу на 10 мл налейте 2 мл концентрированной серной кислоты и 1 мл концентрированной азотной кислоты. Полученную нитрующую смесь охладите до комнатной температуры. Прилейте к ней 1 мл толуола. Закройте пробкой и энергично встряхивайте в течение 5-6 минут. Затем вылейте смесь в стакан с холодной водой. Образовавшая смесь орто- и пара-нитротолуолов собирается на дне стакана в виде желтоватых маслянистых капель. Наблюдения и выводы запишите в лабораторный журнал.
Опыт 4. Горение толуола.
В фарфоровую чашку налейте 2 мл толуола и подожгите его (опыт проводить под тягой!). Отметьте характер пламени.
Наблюдения и выводы запишите в лабораторный журнал.
Задачи (арены)
Определите, являются ли изображенные соединения ароматическими или нет, дайте объяснения:

Назовите следующие соединения по тривиальной номенклатуре и IUPAC:
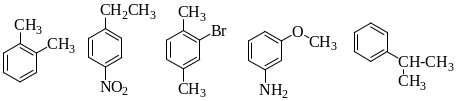
3. Напишите и назовите структурные формулы всех углеводородов ряда бензола, имеющие состав С9Н12 (восемь изомеров).
4. Напишите механизм электрофильного замещения в ароматическом ядре на примере бромирования этилбензола в присутствии AlBr3.
5. Напишите схему синтеза п-крезола из толуола через стадию образования п-толуолсульфокислоты.
6. Закончите уравнения реакций:

7. Какие из перечисленных соединений реагируют с бромом: стирол, этилбензол, метилфенилацетилен, п-метилэтилбензол, 1-фенилбутен-2? Напишите уравнения реакций.
8. Какие производные образуются при нитровании бензойной кислоты, кумола, нитробензола, бромбензола, анизола.
9. Какие гомологи бензола могут образоваться при каталитической дегидроциклизации гексана, гептана, октана, 2-метилгексана, 4-метилгептана?
10. Напишите реакции взаимодействия толуола с пропиленом, этилбромидом, этанолом, ацетилхлоридом. В каких условиях протекают эти реакции? Какие катализаторы используются в каждом случае?
11. Ароматический углеводород состава С9Н10 легко обесцвечивает раствор перманганата калия в воде. При окислении в серной кислоте образуется фталевая кислота. Установите строение этого вещества, напишите схемы указанных реакций.
