
- •Микробиологические основы
- •Введение
- •1. Противомикробные мероприятия
- •Физические методы:
- •2. Химические методы:
- •1.1. Стерилизация
- •1.1.1. Физические методы стерилизации.
- •1.1.2. Химический метод стерилизации.
- •Сравнительная характеристика некоторых методов низкотемпературной стерилизации
- •1.1.3. Контроль стерильности изделий медицинского назначения.
- •1.2. Дезинфекция
- •1.2.2. Контроль качества дезинфекции.
- •1.3. Антисептика
- •1.3.1. Химические антисептические средства.
- •1.3.2. Биологические антисептические средства.
- •1.4. Механизмы антимикробного действия дезинфектантов и антисептиков
- •1.5. Резистентность микроорганизмов к антисептикам и дезинфектантам
- •1.6. Контроль за распространением устойчивых к антибиотикам,антисептикам и дезинфектантам вариантов бактерий и грибов
- •1.7. Микробиологический контроль за присутствием микроорганизмов в глф антибиотиков, антисептиков и дезинфектантов
- •1.7.1. Методика контроля стерильности противомикробных препаратов.
- •2. Методические рекомендации к самостоятельному выполнению заданий по контролю качества противомикробных мероприятий
- •2.1. Стерилизация изделий из стекла и контроль ее качества
- •2.2. Стерилизация медицинского инструментария и контроль ее качества
- •2.3. Контроль качества дезинфекции поверхностей в очагах капельных инфекций
- •2.4. Контроль качества дезинфекции поверхностей в очагах кишечных инфекций
- •2.5. Методика испытания противомикробной активности антисептика профилактического назначения. Гигиеническая антисептика.
- •I этап:
- •II этап:
- •2.6. Методика испытания противомикробной активности антисептика профилактического назначения. Хирургическая антисептика.
- •I этап:
- •II этап:
- •2.7. Контроль стерильности готовых лекарственных форм антибиотиков и антисептиков
- •14 Дней 14 дней
- •2.8. Определение общего микробного числа в готовых лекарственных формах дезинфектантов
2.3. Контроль качества дезинфекции поверхностей в очагах капельных инфекций
Цель: освоить методику контроля качества дезинфекции в очагах капельных инфекций.
Задания:
Провести дезинфекцию поверхностей 0,5% раствором хлорамина;
Проконтролировать качество дезинфекции.
Материалы: 0,5% раствор хлорамина; трафарет 10×10 см, поверхность лабораторного стола, взвесь суточной 1 млрд. культуры S. aureus, ватные тампоны для контаминации, стерильные тампоны, смонтированные в пробирке с 1 мл 1% тиосульфата натрия, среды: 6,5% солевой бульон, чашки с ЖСА, скошенный МПА, плазма кроличья, реактивы для окраски по Граму.
Методика:
Ограничить площадь лабораторного стола или иной поверхности трафаретом 10х10 см;
Контаминировать её тампоном, смоченным взвесью стафилококка (дважды по 1 мин); дать высохнуть;
Тщательно в течение 10 минут протереть тампоном, смоченным раствором хлорамина (не ниже 20оС), ограниченную трафаретом и контаминированную стафилококком поверхность.
Методика контроля качества дезинфекции:
Проводится не позднее 30-45 минут после дезинфекции;
Смыть стерильным ватным тампоном, смоченным в растворе тиосульфата натрия, продезинфицированную площадь (не выходя за границы трафарета);
Тампон опустить в пробирку с солевым бульоном;
Через 24 часа инкубации в термостате при 37оС из бульона сделать высев на ЖСА;
После 48-часовой инкубации в при 37оС подозрительные колонии высеять из ЖСА на скошенный МПА, поместить МПА в термостат на 24 часа при 37оС;
Сделать мазки с окраской по Граму из культуры на МПА и поставить пробу на плазмокоагулазу;
Ответ об обнаружении золотистого стафилококка дают на основании характера роста на питательных средах, характерной морфологии и положительного теста на плазмокоагулазу;
Заключение: дезинфекция считается качественной, если в посевах смывов не выделен золотистый стафилококк.
Рекомендации по выполнению задания:
В первый день провести дезинфекцию, сделать смыв и посеять его в солевой бульон; на второй день из солевого бульона сделать высев на среду ЖСА; на четвёртый день отсеять подозрительные колонии на скошенный МПА; на пятый день определить морфологию, поставить тест на плазмокоагулазу и дать заключение.
Выполнение задания оформляется в виде протокола в альбоме.
Контаминация поверхности стола 10×10 см 1 млрд. взвесью стафилококка |
|
Дезинфекция поверхности стола 0,5% раствором хлорамина |
|
К |


по Граму
![]()
![]()
плазма МПА ЖСА солевой бульон
37оС – 24 ч. 37оС – 48 ч. 37оС – 24 ч.
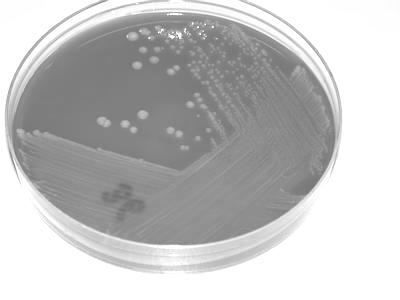
Рис. 6. Общая схема исследования по контролю качества дезинфекции поверхностей в очаге капельных инфекций
2.4. Контроль качества дезинфекции поверхностей в очагах кишечных инфекций
Цель: освоить методику контроля качества дезинфекции в очагах кишечных инфекций.
Задания:
Провести дезинфекцию посуды 0,5% раствором хлорамина;
Проконтролировать качество дезинфекции.
Материалы: 0,5% раствор хлорамина; взвесь суточной 1 млрд. агаровой культуры E. coli, ватные тампоны для контаминации чашек, стерильные тампоны, смонтированные в пробирках с 1 мл 1% тиосульфата натрия, среды: Кесслера, Эндо и ГПС; реактивы для окраски по Граму, кастрюля на 1-2 л., чашки Петри.
Методика:
Тампонами, увлажненными взвесью тест-микроба контаминировать внутреннюю поверхность чашки Петри.
Контаминированные E. coli и высушенные чашки Петри опускают в раствор хлорамина (температура не ниже 20оС);
После 15-минутной экспозиции чашки вынимают из дезраствора.
Методика контроля дезинфекции (не позднее 30-45 минут после дезинфекции):
Всю внутреннюю поверхность чашки протереть тампоном, смоченным раствором тиосульфата натрия;
Тампон опустить в среду Кесслера, которую поставить в термостат при 37оС на одни сутки;
Сделать высев со среды Кесслера на среду Эндо петлёй и выдержать среду в термостате при 37оС - 48 часов;
Подозрительные колонии (красного и розового цвета гладкой формы), содержащие грамотрицательные палочки, пересеять на ГПС;
После суточной инкубации при 43оС учесть образование кислоты и газа;
Ответ об обнаружении кишечной палочки дают на основании характера роста на средах Кесслера и Эндо, грамотрицательной окраски бактерий, ферментации глюкозы с образованием кислоты и газа;
Заключение: дезинфекция считается качественной, если из смывов продезинфицированного объекта не выделена кишечная палочка.
Рекомендации по выполнению задания:
Ход выполнения: в первый день провести дезинфекцию, сделать смыв с продезинфицированных чашек и посеять смыв на среду Кесслера; на второй день - из среды Кесслера сделать высев на среду Эндо; на четвертый день - отобрать подозрительные колонии, сделать мазок и в случае обнаружения грамотрицательных палочек остаток колонии пересеять на полужидкую ГПС; на пятый день - учесть ферментацию глюкозы и сделать заключение.
Выполнение задания оформляется в виде протокола в альбоме.
Контаминация чашки Петри 1 млрд. взвесью E. coli |
|
Дезинфекция чашки Петри 0,5% раствором хлорамина |
|
К (смыв поверхности чашки) |
по Граму
ГПС Cреда Эндо Cреда Кесслера
43оС – 24 ч. 37оС – 24 ч. 37оС – 24 ч.
![]()

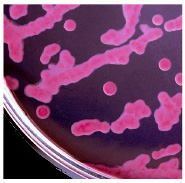
Рис. 7. Общая схема исследования по контролю качества дезинфекции поверхностей в очаге кишечных инфекций


 онтроль
качества дезинфекции (смыв с поверхности
стола)
онтроль
качества дезинфекции (смыв с поверхности
стола) онтроль
качества дезинфекции
онтроль
качества дезинфекции