
- •Введение
- •Электронное строение элементов-органогенов. Химическая связь в органических молекулах
- •Химическая связь в органических молекулах
- •Классификация химических реакций. Химические свойства алканов, алкенов и алкадиенов
- •Реакционная способность алканов
- •Реакционная способность алкенов
- •Химические свойства алкенов
- •Общий механизм реакций электрофильного присоединения
- •Реакции электрофильного присоединения к несимметричным алкенам
- •Реакции присоединения к алкадиенам
- •Сопряжённые системы. Ароматичность. Электронные эффекты. Реакции электрофильного замещения в бензоле и его производных
- •Химические свойства бензола
- •Взаимное влияние атомов в молекулах органических соединений. Электронные эффекты
- •Реакции электрофильного замещения в нафталине
- •Реакции окисления гомологов бензола
- •Химические свойства галогеналканов, спиртов и фенолов
- •Медико-биологическое значение галогеналканов
- •Спирты и фенолы
- •Медико-биологическое значение спиртов и фенолов
- •Кислотные и основные свойства органических соединений. Реакционная способность аминов
- •Кислоты Бренстеда
- •Основания Бренстеда
- •Реакционная способность оксосоединений
- •Классификация и номенклатура оксосоединений
- •Названия алифатических альдегидов
- •Реакционные центры в молекулах оксосоединений
- •Примеры реакций нуклеофильного присоединения
- •Медико-биологическое значение альдегидов и кетонов
- •Химические свойства карбоновых кислот и их функциональных производных
- •Названия предельных алифатических монокарбоновых кислот
- •Реакционные центры в молекулах карбоновых кислот
- •Кислотные свойства карбоновых кислот
- •Реакции нуклеофильного замещения
- •Реакции карбоновых кислот по радикалу
- •Названия насыщенных алифатических дикарбоновых кислот
- •Медико-биологическое значение карбоновых кислот и их производных
- •Гетерофункциональные соединения алифатического ряда – метаболиты и биорегуляторы
- •Аминоспирты
- •Аминокислоты
- •Гидроксикислоты (оксикислоты)
- •Оксокислоты
- •Медико-биологическое значение гетерофункциональных производных карбоновых кислот
- •Оптическая изомерия
- •Стереоизомерия молекул с несколькими центрами хиральности
- •Стереоизомерия и биологическая активность
- •Гетерофункциональные производные бензольного ряда
- •Производные сульфаниловой кислоты
- •Сульфаниламидные препараты
- •Салициловая кислота и ее производные
- •Гетероциклические соединения. Производные пятичленных гетероциклов
- •Пятичленные гетероциклы с одним гетероатомом
- •Свойства пиррола и его производных
- •Свойства фурана и его производных
- •Пятичленные гетероциклы с двумя гетероатомами
- •Шестичленные гетероциклические соединения
- •Шестичленные гетероциклы с двумя гетероатомами
- •Углеводы. Моносахариды
- •Цикло-оксо-таутомерия моносахаридов
- •Углеводы. Ди- и полисахариды
- •Природные α-аминокислоты. Пептиды, белки
- •Строение и классификация природных α-аминокислот
- •Стереоизомерия α-аминокислот
- •Химические свойства
- •Реакции α-аминокислот in vivo
- •Нуклеиновые кислоты
- •Нуклеиновые основания
- •Нуклеозиды
- •Названия нуклеозидов
- •Нуклеотиды
- •Нуклеиновые кислоты
- •Омыляемые липиды
- •Фосфолипиды
- •Неомыляемые липиды
- •Алкалоиды
- •Литература
- •Оглавление
- •305041, Г. Курск, ул. К. Маркса, 3.
- •305041, Г. Курск, ул. К. Маркса, 3. Заказ № 313.
Названия нуклеозидов
|
Нуклеиновое основание |
Моносахарид |
Название нуклеозида |
|
Урацил Тимин Цитозин Цитозин Аденин Аденин Гуанин Гуанин |
рибоза дезоксирибоза рибоза дезоксирибоза рибоза дезоксирибоза рибоза дезоксирибоза |
уридин тимидин цитидин дезоксицитидин аденозин дезоксиаденозин гуанозин дезоксиаденозин |
Как для N-гликозидов, для нуклеозидов характерен кислотный гидролиз, который протекает сравнительно легко, особенно для пуриновых нуклеозидов.
Например, при кислотном гидролизе тимидина образуется тимин и дезоксирибоза (тимидин – нуклеозид ДНК):

Некоторые нуклеозиды не входят в структуру нуклеиновых кислот, а присутствуют в растительных и животных клетках в свободном виде. Они обладают антибиотической и противоопухолевой активностью. Некоторые из них применяются в медицине.
Нуклезиды-антибиотики отличаются от обычных нуклеозидов природой пентозы или строением гетероциклического основания. Например, кордицепин отличается от аденозина только отсутствием гидроксильной группы в положении 3’ моносахаридного остатка.
Т акое
подобие кордицепина аденозину,
по-видимому, делает его антагонистом
аденозина, что и приводит к антибиотической
активности.
акое
подобие кордицепина аденозину,
по-видимому, делает его антагонистом
аденозина, что и приводит к антибиотической
активности.

Метод аналогии был использован в синтезе некоторых новых антивирусных препаратов, например, арабинозида аденина (ингибирует синтез ДНК вируса):
Одним из первых препаратов, применяемых для лечения ВИЧ-инфекцированных больных, был азидотимидин (антагонист тимидина).
А зидотимидин
снижает скорость размножения вируса
СПИД.
зидотимидин
снижает скорость размножения вируса
СПИД.
Нуклеотиды
Нуклеотиды – это сложные эфиры нуклеозидов и фосфорной кислоты (фосфаты нуклеозидов). В зависимости от природы нуклеозидов выделяют рибонуклеотиды и дезоксирибонуклеотиды.
Фосфатная группа связана с пентозным циклом обычно в положениях 3’ или 5’.

Нуклеотиды называют как сложные эфиры фосфорной кислоты – фосфаты, например, уридин-5’-фосфат, дезоксигуанозин-3’-фосфат. С другой стороны, нуклеотиды можно рассматривать как двухосновные кислоты. Тогда их называют 5’-уридиловая кислота, 3’-дезоксигуаниловая кислота и т.д.

Фосфорная кислота может этерифицировать одновременно две гидроксильные группы углеводного остатка, образуя циклофосфаты. Практически во всех клетках присутствуют аденозин-3’,5’-циклофосфат (3’,5’-циклоадениловая кислота) и гуанозин-3’,5’-циклофосфат (3’,5’-циклогуаниловая кислота):

Циклические нуклеотиды играют в клетке важную роль: они являются посредниками между некоторыми гормонами (например, адреналин) и клеточными процессами.
Так как в молекулах нуклеотидов присутствуют и N-гликозидные, и сложноэфирные связи, в зависимости от условий гидролиза образуются различные продукты. N-гликозидная связь гидролизуется только в кислой среде, а сложноэфирная – и в кислой, и в щелочной:

Нуклеотиды имеют большое значение не только как мономеры для строительства нуклеиновых кислот. Они участвуют в биохимических процессах и особенно важны в роли коферментов, т.е. веществ, необходимых для проявления активности ферментов.
Во всех тканях организма содержатся моно-, ди- и трифосфаты нуклеотидов. Особенно широко известны аденозинмонофосфат (АМФ), аденозиндифосфат (АДФ) и аденозинтрифосфат (АТФ). Нуклеотиды, фосфорилированные в разной степени, способны к взаимным преврашениям путем отщепления остатка фосфорной кислоты или наращиванием его:
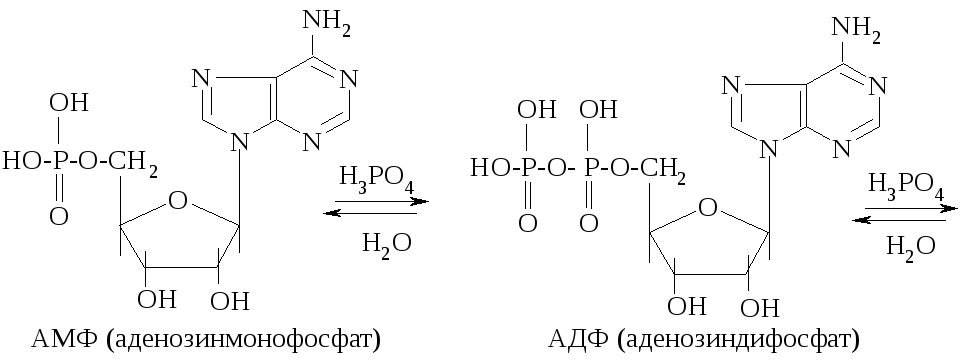

Ангидридные связи между остатками фосфорной кислоты обладают большим запасом энергии (~32 кДж/моль), поэтому их называют макроэргическими. При гидролизе АТФ до АДФ и АМФ эта энергия выделяется. Важнейшая роль АТФ – поставщик энергии во всех живых клетках.
 С
участием АТФ и АДФ в организме
осуществляется важнейший биохимический
процесс – перенос фосфатных групп.
Образование фосфатов – типичная реакция
в метаболизме углеводов:
С
участием АТФ и АДФ в организме
осуществляется важнейший биохимический
процесс – перенос фосфатных групп.
Образование фосфатов – типичная реакция
в метаболизме углеводов:
АТФ активирует α-аминокислоты в биосинтезе белков:


При взаимодействии α-аминокислоты с молекулой АТФ образуется смешанный ангидрид аминокислоты и АМФ – аминоациладенилат. Ангидриды кислот являются более активными ацилирующими средствами, чем сами кислоты. Активированная аминокислота затем взаимодействует с аминогруппой следующей аминокислоты в синтезе пептидов.
Нуклеотидную природу имеет никотинамидадениндинуклеотид (НАД+) – кофермент дегидрогеназ, который является участником окислительно-восстановительных реакций (см. стр. 148). С участием НАД+ протекают реакции окисления спиртов в альдегиды (ретинол – ретиналь и др.).
Флавинадениндинуклеотид (ФАД) является метаболически активной формой рибофлавина (витамина B2).

В структуре рибофлавина присутствует остаток D-рибитола (многоатомный спирт – продукт восстановления рибозы) и гетероциклическая система изоаллоксазина (флавина). В структуре же ФАД присутствует ещё и остаток адениндинуклеотида.
Флавинадениндинуклеотид является коферментом окислительно-восстановительных процессов с участием ферментов оксидаз и дегидрогеназ. С участием ФАД происходит, например, окислительное дезаминирование α-аминокислот в организме.
Ответственной за окислительно-восстановительный процесс является остаток изоаллоксазина, способный присоединять два атома водорода с образованием восстановленной формы ФАДH2:

