
- •Введение
- •Электронное строение элементов-органогенов. Химическая связь в органических молекулах
- •Химическая связь в органических молекулах
- •Классификация химических реакций. Химические свойства алканов, алкенов и алкадиенов
- •Реакционная способность алканов
- •Реакционная способность алкенов
- •Химические свойства алкенов
- •Общий механизм реакций электрофильного присоединения
- •Реакции электрофильного присоединения к несимметричным алкенам
- •Реакции присоединения к алкадиенам
- •Сопряжённые системы. Ароматичность. Электронные эффекты. Реакции электрофильного замещения в бензоле и его производных
- •Химические свойства бензола
- •Взаимное влияние атомов в молекулах органических соединений. Электронные эффекты
- •Реакции электрофильного замещения в нафталине
- •Реакции окисления гомологов бензола
- •Химические свойства галогеналканов, спиртов и фенолов
- •Медико-биологическое значение галогеналканов
- •Спирты и фенолы
- •Медико-биологическое значение спиртов и фенолов
- •Кислотные и основные свойства органических соединений. Реакционная способность аминов
- •Кислоты Бренстеда
- •Основания Бренстеда
- •Реакционная способность оксосоединений
- •Классификация и номенклатура оксосоединений
- •Названия алифатических альдегидов
- •Реакционные центры в молекулах оксосоединений
- •Примеры реакций нуклеофильного присоединения
- •Медико-биологическое значение альдегидов и кетонов
- •Химические свойства карбоновых кислот и их функциональных производных
- •Названия предельных алифатических монокарбоновых кислот
- •Реакционные центры в молекулах карбоновых кислот
- •Кислотные свойства карбоновых кислот
- •Реакции нуклеофильного замещения
- •Реакции карбоновых кислот по радикалу
- •Названия насыщенных алифатических дикарбоновых кислот
- •Медико-биологическое значение карбоновых кислот и их производных
- •Гетерофункциональные соединения алифатического ряда – метаболиты и биорегуляторы
- •Аминоспирты
- •Аминокислоты
- •Гидроксикислоты (оксикислоты)
- •Оксокислоты
- •Медико-биологическое значение гетерофункциональных производных карбоновых кислот
- •Оптическая изомерия
- •Стереоизомерия молекул с несколькими центрами хиральности
- •Стереоизомерия и биологическая активность
- •Гетерофункциональные производные бензольного ряда
- •Производные сульфаниловой кислоты
- •Сульфаниламидные препараты
- •Салициловая кислота и ее производные
- •Гетероциклические соединения. Производные пятичленных гетероциклов
- •Пятичленные гетероциклы с одним гетероатомом
- •Свойства пиррола и его производных
- •Свойства фурана и его производных
- •Пятичленные гетероциклы с двумя гетероатомами
- •Шестичленные гетероциклические соединения
- •Шестичленные гетероциклы с двумя гетероатомами
- •Углеводы. Моносахариды
- •Цикло-оксо-таутомерия моносахаридов
- •Углеводы. Ди- и полисахариды
- •Природные α-аминокислоты. Пептиды, белки
- •Строение и классификация природных α-аминокислот
- •Стереоизомерия α-аминокислот
- •Химические свойства
- •Реакции α-аминокислот in vivo
- •Нуклеиновые кислоты
- •Нуклеиновые основания
- •Нуклеозиды
- •Названия нуклеозидов
- •Нуклеотиды
- •Нуклеиновые кислоты
- •Омыляемые липиды
- •Фосфолипиды
- •Неомыляемые липиды
- •Алкалоиды
- •Литература
- •Оглавление
- •305041, Г. Курск, ул. К. Маркса, 3.
- •305041, Г. Курск, ул. К. Маркса, 3. Заказ № 313.
Шестичленные гетероциклы с двумя гетероатомами
Пиридазин, пиримидин и пиразин являются изомерными шестичленными гетероциклами с двумя гетероатомами азота. Они носят общее название азины:

Диазины являются ароматическими соединениями (это замкнутые π,π-сопряженные системы, в которых делокализовано 6 электронов).
Подробнее остановимся на свойствах пиримидина.
Реакционная способность пиримидина в реакциях электрофильного замещения понижена из-за электроноакцепторного влияния двух пиридиновых атомов азота, поэтому реакции SE практически не протекают.
В связи с тем, что пиримидин является ещё
более π-недостаточной системой, чем
пиридин, для него характерны реакции
нуклеофильного
замещения,
например, реакция Чичибабина. Аминирование
протекает в положениях 2, 4 или 6, в которых
электронная плотность особенно понижена:
связи с тем, что пиримидин является ещё
более π-недостаточной системой, чем
пиридин, для него характерны реакции
нуклеофильного
замещения,
например, реакция Чичибабина. Аминирование
протекает в положениях 2, 4 или 6, в которых
электронная плотность особенно понижена:
О сновные
свойства
пиримидина ниже, чем пиридина, также
из-за электроноакцепторного влияния
второго атома азота. В отличие от пиридина
пиримидин не образует соли с водой, он
реагирует с сильными минеральными
кислотами:
сновные
свойства
пиримидина ниже, чем пиридина, также
из-за электроноакцепторного влияния
второго атома азота. В отличие от пиридина
пиримидин не образует соли с водой, он
реагирует с сильными минеральными
кислотами:
Особенно важны гидрокси- и амино-производные пиримидина – урацил, тимин и цитозин, являющиеся компонентами нуклеиновых кислот (см. стр.204).
К производным пиримидина относится также барбитуровая кислота и барбитураты.
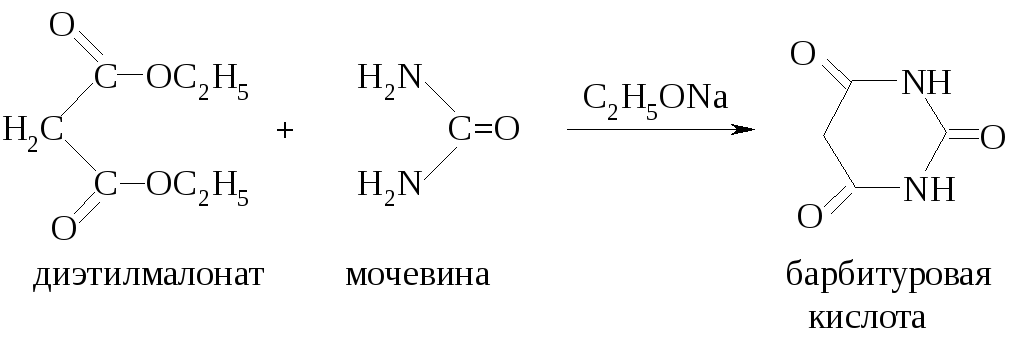
Барбитуровая кислота является циклическим уреидом малоновой кислоты. Она может быть получена при взаимодействии мочевины с диэтиловым эфиром малоновой кислоты:
Для барбитуровой кислоты характерны два вида таутомерии – лактам-лактимная и кето-енольная:

Наиболее стабильной является триоксоформа, т.е. лактамная кето-форма. За счет существования в енольной таутомерной форме барбитуровая кислота проявляет сильные кислотные свойства (она сильнее, чем уксусная).
М ногие
5,5-дизамещенные производные барбитуровой
кислоты, так называемые барбитураты,
применяются в медицине как снотворные
и противосудорожные препараты.
ногие
5,5-дизамещенные производные барбитуровой
кислоты, так называемые барбитураты,
применяются в медицине как снотворные
и противосудорожные препараты.
Для барбитуратов возможна только лактам-лактимная таутомерия. Они проявляют кислотные свойства за счет лактимной формы, образуя соли с одним эквивалентом щелочи:

Примерами барбитуратов являются барбитал (5,5-диэтилбарбитуровая кислота), фенобарбитал (5-фенил-5-этилбарбитуровая кислота).
Пиримидиновое кольцо входит также в структуру витамина В1 (тиамина) и кокарбоксилазы (см. стр. 143,144).
Из конденсированных гетероциклических систем в природе наиболее распространены соединения пуринового ряда.
П урин
образован конденсированными ядрами
пиримидина и имидазола. Пурин является
ароматическим соединением. Это замкнутая
p,π-сопряженная
система, в которой делокализовано 10
электронов (пиридиновые атомы азота в
положениях 1, 3 и 7 отдают в сопряжение
по одному электрону, пиррольный азот в
положении 9 – неподеленную электронную
пару).
урин
образован конденсированными ядрами
пиримидина и имидазола. Пурин является
ароматическим соединением. Это замкнутая
p,π-сопряженная
система, в которой делокализовано 10
электронов (пиридиновые атомы азота в
положениях 1, 3 и 7 отдают в сопряжение
по одному электрону, пиррольный азот в
положении 9 – неподеленную электронную
пару).
П урин
проявляет амфотерные свойства: пиридиновый
азот в положении 7 отвечает за основные
свойства, а пиррольный азот – за
кислотные:
урин
проявляет амфотерные свойства: пиридиновый
азот в положении 7 отвечает за основные
свойства, а пиррольный азот – за
кислотные:
П урин
образует соли с минеральными кислотами
и со щелочными металлами:
урин
образует соли с минеральными кислотами
и со щелочными металлами:
Для пурина характерна протропная таутомерия за счет переноса протона водорода от кислотного центра к основному, поэтому положения 7 и 9 в молекуле равноценны:

Гидроксипурины. Гипоксантин (6-гидроксипурин), ксантин (2,6-дигидроксипурин) и мочевая кислота (2,6,8-тригидроксипурин) образуются в организме в процессе метаболизма нуклеиновых кислот.

Д ля
гидроксипуринов характерна лактам-лактимная
таутомерия,
за счет лактимной формы они проявляют
кислотные свойства. Более стабильной
является лактамная форма.
ля
гидроксипуринов характерна лактам-лактимная
таутомерия,
за счет лактимной формы они проявляют
кислотные свойства. Более стабильной
является лактамная форма.
Важными производными ксантина являются алкалоиды (так называемые метилированные ксантины) – теофилин (1,3-диметилксантин), теобромин (3,7-диметилксантин) и кофеин (1,3,7-триметилксантин):

Их природными источниками являются листья чая, зерна кофе, какао-бобы. Кофеин возбуждает центральную нервную систему. Теофиллин и теобромин также стимулируют ЦНС, но в меньшей степени. Они проявляют диуретический эффект.
Мочевая кислота – конечный продукт метаболизма пуриновых соединений в организме. Мочевая кислота образует два ряда солей, т.е. является двух-, а не трехосновной кислотой, как можно было бы предположить.

Дело в том, что один из лактамных фрагментов мочевой кислоты является «закрепленным», т.е. не может перейти в лактимную форму из-за наличия водородной связи.
Соли мочевой кислоты называют уратами. Кислые ураты (кроме литиевых) нерастворимы в воде, средние ураты растворимы. Нерастворимые ураты могут откладываться в суставах при подагре, а также в виде почечных камней.
Производными пурина являются также аденин и гуанин – нуклеиновые основания (см. стр. 204).
