
muravev_a_g_rukovodstvo_po_opredeleniyu_pokazatelei_kachestv
.pdf
«свободный активный хлор», и относительно менее слабые окислители – хлорамины – «связанный активный хлор». Благодаря сильным окислительным свойствам соединения, имеющие активный хлор, используются для обеззараживания (дезинфекции) питьевой воды и воды в бассейнах, а также для химической очистки некоторых сточных вод. Кроме того, некоторые содержащие активный хлор соединения (например, хлорная известь) широко используются для ликвидации очагов распространения инфекционных загрязнений.
Наиболее широко для дезинфекции питьевой воды используется свободный хлор, который при растворении в воде диспропорционирует по реакции:
Cl2+H2O=H++Cl–+HOCl
В природной воде содержание активного хлора не допускается; в питьевой воде его содержание установлено в пересчете на хлор на уровне 0,3–0,5 мг/л в свободном виде и на уровне 0,8–1,2 мг/л в связанном виде . Активный хлор в указанных концентрациях присутствует в питьевой воде непродолжительное время (не более нескольких десятков минут) и нацело удаляется даже при кратковременном кипячении воды. По этой причине анализ отобранной пробы на содержание активного хлора следует проводить немедленно.
Интерес к контролю содержания хлора в воде, особенно в питьевой, возрос после осознания того факта, что хлорирование воды приводит к образованию заметных количеств хлоруглеводородов, вредных для здоровья населения. Особую опасность представляет хлорирование питьевой воды, загрязненной фенолом. ПДК для фенолов в питьевой воде при отсутствии хлорирования питьевой воды установлена 0,1 мг/л, а в условиях хлорирования (при этом образуются гораздо более токсичные и имеющие резкий характерный запах хлорфенолы) – 0,001 мг/л. Аналогичные химические реакции могут протекать с участием органических соединений природного или техногенного происхождения, приводя к различным токсичным хлорорганическим соединениям – ксенобиотикам.
Предлагаемый йодометрический метод (метод йодометрического титрования) определения активного хлора является адаптированным стандартным методом для анализа питьевой воды (ГОСТ 18190). Метод основан на свойстве всех содержащих активный хлор соединений в кислой среде выделять из йодида калия свободный йод:
Для питьевой воды приведены диапазоны концентраций активного хлора, т.к. при меньших его концентрациях возможна неблагоприятная ситуация по микробиологическим показателям, а при больших – превышение непосредственно по активному хлору.
151
Cl2+2I–=I2+2Cl–
ClO–+2H++2I–=I2+Cl–+H20
HClO+H++2I–=I2+Cl–+H20
NH2Cl+2H++2I–=I2+NH4++Cl–
Свободный йод оттитровывают тиосульфатом натрия в присутствии крахмала, как описано при определении растворенного кислорода. Реакцию проводят в буферном растворе при рН 4,5, и тогда определению не мешают нитриты, озон и другие соединения. Однако мешающими определению веществами являются другие сильные окислители, которые также выделяют йод из йодида калия, – хроматы, хлораты и др. Концентрации, в которых указанные окислители оказывают мешающее действие, могут присутствовать в сточных водах, но маловероятны в питьевой и природной воде. Метод может также использоваться для анализа мутных и окрашенных вод.
Концентрацию активного хлора (САХ) в мг/л рассчитывают по результатам титрования, для которого обычно используется раствор тиосульфата натрия с концентрацией 0,005 моль/л экв. Расчет проводят по формуле:
САХ |
VТ К 0,177 1000 |
, |
|
VА |
|||
|
|
где: VТ – количество раствора тиосульфата натрия с концентрацией 0,005 моль/л экв., израсходованного на титрование, мл; К – поправочный коэффициент, учитывающий отклонение точной
фактической концентрации тиосульфата от значения 0,005 моль/л экв. (для большинства случаев значение К принимается равным 1); 0,177 – содержание активного хлора в мг, соответствующее 1 мл рас-
твора тиосульфата с концентрацией 0,005 моль/л экв.; VА – объем пробы воды, взятой для анализа, мл;
1000 – коэффициент пересчета единиц измерения из миллилитров в литры.
Чувствительность метода – 0,3 мг/л при объеме пробы 250 мл, однако при использовании растворов тиосульфата с различной концентрацией объем пробы может составлять, в зависимости от требуемой чувствительности определения, от 500 до 50 мл воды и менее.
Лимитирующий показатель вредности для активного хлора – общесанитарный.
152
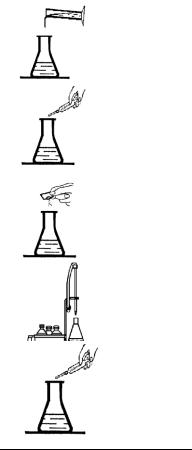
Оборудование и реактивы
Колба коническая на 250–500 мл с градуировкой по объему (если колба не отградуирована, тогда необходим также мерный цилиндр), бюретка или пипетка градуированная на 2–5 мл со шприцем и соединительной трубкой, шприц-дозатор (пипетка) на 1 мл (2 шт.), ножницы.
Калий йодистый в капсулах по 0,5 г, раствор буферный ацетатный (рН 4,5), раствор тиосульфата натрия титрованный (0,005 моль/л экв.), раствор крахмала (0,5%).
Приготовление растворов см. приложение 3.
Выполнение определения
1. Налейте в коническую колбу анализируемую воду до метки (например, 50 мл) либо с помощью мерного цилиндра. Колбу предварительно ополосните анализируемой водой.
2. Поместите в колбу при помощи шприца-дозатора или пипетки 1,0 мл ацетатного буферного раствора, содержимое колбы перемешайте.
3. Добавьте в коническую колбу содержимое одной капсулы (около 0,5 г) йодида калия. Перемешайте содержимое колбы до растворения соли.
4. Оттитровывайте выделившийся йод раствором тиосульфата. Для этого в бюретку (пипетку), закрепленную в штативе и соединенную через трубку со шприцем, наберите 2–5 мл раствора тиосульфата и титруйте пробу до слабо желтой окраски.
5. Добавьте другим шприцем-дозатором (пипеткой) 1 мл раствора крахмала (раствор в колбе синеет) и продолжайте титрование до полного обесцвечивания раствора.
Калий йодистый не должен выделять йода при подкислении раствора.
153
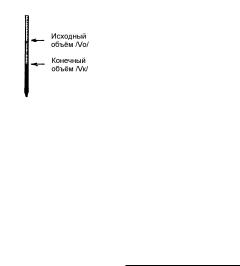
Примечание. После изменения окраски пробу необходимо выдержать еще 0,5 мин. для полного протекания реакции. В случае восстановления окраски необходимо добавить еще некоторое количество раствора титранта.
6. Определите общий объем раствора тиосульфата, израсходованный на титрование (как до, так и после добавления раствора крахмала).
7. Рассчитайте концентрацию суммарного остаточного активного хлора (САХ) в мг/л по формуле,
приведенной на стр. 152.
При необходимости анализ повторите, уменьшив (увеличив) объем пробы.
В качестве экспрессной портативной полевой модификации ме-
тода с чувствительностью не менее 0,3–0,5 мг/л для определения активного хлора в питьевой, водопроводной и природной воде может быть рекомендовано использование раствора тиосульфата с концентрацией 0,0025 моль/л экв., при отборе пробы 50 мл и титрованием с помощью калиброванной пипетки-капельницы. В этом случае концентрация активного хлора (САХ) в мг/л рассчитывается по формуле:
СAX VK N 0,089 1000 N 0,0712 , где
Vnp
где: N – количество капель раствора тиосульфата натрия, израсходованного на титрование; 0,089 – количество эквивалентов тиосульфата натрия в 1 мл раствора
с концентрацией 0,0025 моль/л экв., моль; VK – объем капли, равный 0,040 мл;
Vnp – объем пробы, взятой для анализа, 50 мл.
Пример расчета. При анализе водопроводной воды в результате титрования пробы объемом 50 мл раствором тиосульфата с концентрацией 0,0025 моль/л экв. с помощью калиброванной пипетки-капельницы (объем капли 0,040 мл) на титрование израсходовано 11 капель раствора тиосульфата. Следовательно, содержание активного хлора в воде составляет:
САХ=11 0,0712=0,78 мг/л.
6.6.3. Нефтепродукты
Нефтепродукты относятся к числу наиболее распространенных и опасных веществ, загрязняющих поверхностные воды. Большие количества нефтепродуктов поступают в поверхностные воды при перевозке
154
нефти водным путем, транспортировке по трубопроводам, со сточными водами предприятий нефтедобывающей, нефтеперерабатывающей, химической, металлургической и других отраслей промышленности, с хо- зяйственно-бытовыми водами.
Нефть и продукты ее переработки представляют собой чрезвычайно сложную, непостоянную по составу и разнообразную смесь веществ. В ее состав входят низко- и высокомолекулярные предельные, непредельные алифатические, нафтеновые, ароматические углеводороды; кислород-, азот- и серосодержащие соединения; ненасыщенные гетероциклические соединения типа смол, асфальтенов, ангидридов, асфальтеновых кислот и др.
В результате протекающих в водоеме процессов (испарения, сорбции, биохимического и химического окисления и др.) концентрация нефтепродуктов может существенно снижаться, при этом значительным изменениям может подвергаться их химический состав. Нефтепродукты находятся в различных миграционных формах: растворенной, эмульгированной, сорбированной на твердых частицах взвесей и донных отложений, в виде пленки на поверхности воды. Обычно в момент поступления в водоем масса нефтепродуктов сосредоточена в пленке. По мере удаления от источника загрязнения либо с течением времени происходит перераспределение нефтепродуктов между основными формами, проходящее стадии перехода с последовательным повышением доли растворенных, эмульгированных, сорбированных нефтепродуктов. Наличие нефтепродуктов в виде пленки отрицательно сказывается как на качестве воды, так и на состоянии водоема в целом, на флоре и фауне. В присутствии нефтепродуктов вода приобретает специфический вкус и запах, изменяется ее цвет, рН, ухудшается газообмен с атмосферой, нарушаются процессы самоочищения водоема.
При санитарно-химическом контроле при анализе нефтепродуктов определяют суммарную их концентрацию во всех формах, существующих в отобранной пробе, – растворе, эмульсии, а также в виде, сорбированном как на взвешенных частицах, так и на стенках сосуда для отбора пробы.
При анализе предлагаемым методом в качестве нефтепродуктов определяются неполярные и малополярные углеводороды (суммарное содержание алифатических, олефиновых, нафтеновых, ароматических соединений), составляющие обычно основную и наиболее характерную часть нефти и продуктов ее переработки. Именно такие соединения специалисты подразумевают под термином «нефтепродукты» при анализе вод согласно определению, впервые принятому Комиссией по унификации методов анализа природных и сточных вод стран-членов СЭВ (1968 г.).
155
Метод определения содержания масла и нефтепродуктов в воде основан на их предварительной концентрации путем экстрагирования из водной среды неполярным растворителем – четыреххлористым углеродом в кислой среде при рН 3–4 с последующим анализом экстракта.
Анализ экстракта на содержание нефтепродуктов выполняется полуколичественным методом бумажной хроматографии, который основан на использовании различия коэффициентов распределения (сорбируемости) компонентов анализируемого раствора. Различные величины коэффициентов распределения обеспечивают разделение смеси в экстракте.
Чувствительность обнаружения нефтепродуктов составляет 1 мг/л. Диапазон определяемых концентраций нефтепродуктов в воде – от
1 до 20 мг/л, продолжительность выполнения анализа – не более 3 часов (включая стадию экстракции пробы).
Оборудование
Бумага индикаторная универсальная, полоски для хроматографирования (длина 60 мм, ширина 6 мм).
Воронка делительная на 100 мл, воронка делительная на 1 л или сосуд для экстракции с пробкой (плоскодонная колба, стеклянная бутыль), склянки для хранения экстрактов, стаканчики для хроматографирования (2 шт.), пипетка мерная градуированная на 10 мл, пипетка-капельница на 1 мл (2 шт.), шприц медицинский с соединительной трубкой, шкала миллиметровая.
Углерод четыреххлористый, раствор соляной кислоты (1:1).
Выполнение анализа
Отбор проб
Количество отбираемой пробы воды определяется величиной ожидаемой концентрации нефтепродуктов в воде. В зависимости от ожидаемой концентрации нефтепродуктов в воде рекомендуется отбирать пробы в количествах согласно табл. 13.
|
Таблица 13 |
|
|
Величина ожидаемой концентрации |
Количество |
нефтепродуктов в воде, мг/л |
отбираемой пробы, л |
1–5 |
0,5 |
5–20 |
0,2 |
Проведение экстракции
Экстракцию проводите в делительной воронке либо в сосуде достаточной вместимости (плоскодонной колбе, стеклянной бутыли).
156
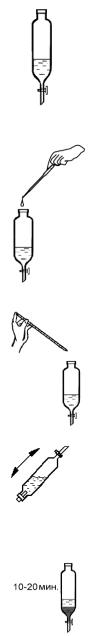
1. В сосуд с пробкой (делительную воронку, плоскодонную колбу, стеклянную бутыль) поместите в соответствии с табл. 13 пробу анализируемой воды. Проба должна занимать не более ⅓ объема сосуда.
2. К пробе добавьте 2–3 капли раствора соляной кислоты до рН 3–4 (значение рН контролируйте по универсальной индикаторной бумаге).
2-3 капли HCl до рН 3-4
3. Добавьте к пробе с помощью пипетки 10 мл четыреххлористого углерода.
10 мл ЧХУ
|
4. Проведите экстракцию, для чего интенсивно пере- |
3-5 мин. |
мешивайте содержимое сосуда в течение 3–5 мин. |
|
5. Оставьте сосуд в вертикальном положении на
10–20 минут для расслоения жидкости.
157
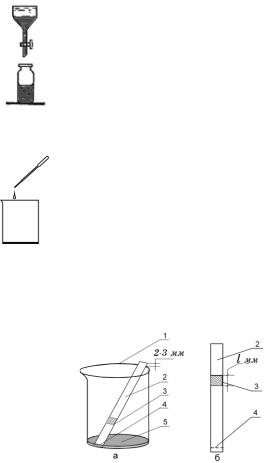
6. Нижний слой с небольшим количеством воды перенесите в делительную воронку из набора (верхний водный слой отбрасывают). Воронку оставьте в вертикальном положении на 10–20 минут.
7. Отделите экстракт от остатков воды, слив его в склянку для хранения экстракта.
Примечание. Экстракты можно хранить в герметично закрытых склянках в прохладном месте в вертикальном положении до 2 месяцев.
Анализ экстракта
1. Из склянки с экстрактом пипеткой-капельницей отберите 1 мл экстракта и перенесите в стаканчик для хроматографирования.
2. В стаканчик с экстрактом поместите полоску хроматографической бумаги под углом таким образом, чтобы нижний конец полоски упирался в противоположную стенку стаканчика, а верхний край полоски выступал выше края стаканчика на 2–3 мм (рис. 11, а).
Рис. 11. Определение содержания нефтепродуктов методом бумажной хроматографии: а – положение полоски в стаканчике при хроматографировании; б – расположение пятна нефтепродуктов на полоске после хроматографирования. 1 – стаканчик; 2 – полоска; 3 – пятно нефтепродуктов; 4 – граница погружения плоски; 5 – экстракт.
Примечание. 1. Наклоны и тряска (качание основы) в период хроматографирования могут привести к неправильному результату при анализе! 2. Для повышения надежности результатов целесообразно выполнять анализ 2 проб воды одновременно. При этом следует обеспечивать одинаковые условия при хроматографировании экстракта (температуру, скорость обдува стаканчика воздухом).
158
3. Выдержите полоску бумаги до полного испарения растворителя (около 3 часов).
4. Линейкой измерьте ширину пятна нефтепродуктов на полоске
(рис. 11, б).
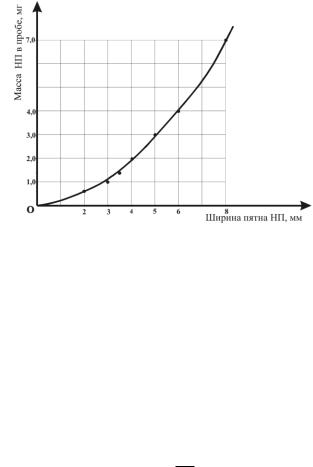
5. С помощью градуировочного графика (рис. 12) определите массу нефтепродуктов в пробе.
Рис. 12. Зависимость ширины пятна (l) от массы нефтепродуктов в пробе (градуировочный график).
6. Концентрацию нефтепродуктов в пробе воды (СНП, мг/л) рассчитайте по формуле:
C НР C ПР ,
V
где: V – объем воды, взятый на анализ, мл; СПР – масса нефтепродуктов в пробе, мг.
Пример. На анализ взято 200 мл анализируемой воды. После экстракции нефтепродуктов и анализа экстракта на полоске после испарения ЧХУ осталось масляное пятно шириной 5,5 мм. Пользуясь графиком (рис. 12), нашли соответствующее содержание нефтепродуктов в пробе – 3,5 мг. Рассчитали концентрацию:
CНП C ПР 3,5 17,5
V 0,2
Следовательно, содержание нефтепродуктов в анализируемой воде составляет 17,5 мг/л.
159
Контроль точности анализа
Контроль точности анализа осуществляется с помощью тестирования специально приготовленных растворов с известной концентрацией нефтепродуктов (например, приготовленных из ГСО).
6.6.4.Поверхностно-активные вещества, анионоактивные
Поверхостно-активные вещества (ПАВ) представляют собой обширную группу, как правило, синтетических соединений, различных по своей структуре, относящихся к разным классам. Эти вещества способны адсорбироваться на поверхности раздела фаз и понижать вследствие этого поверхностную энергию (поверхностное натяжение). В зависимости от свойств, проявляемых ПАВ при растворении в воде, их делят на анионоактивные вещества (активной частью является анион), катионоактивные (активной частью молекул является катион), амфолитные и неионогенные, которые совсем не ионизируются.
Анионоактивные ПАВ в водном растворе ионизируются с образованием отрицательно заряженных органических ионов. Из анионоактивных ПАВ широкое применение нашли соли сернокислых эфиров (сульфаты) и соли сульфокислот (сульфонаты). Радикал R может быть алкильным, алкиларильным, алкилнафтильным, иметь двойные связи и функциональные группы.
Катионоактивные ПАВ – вещества, которые ионизируются в водном растворе с образованием положительно заряженных органических ионов. К ним относятся четвертичные аммониевые соли, состоящие из: углеводородного радикала с прямой цепью, содержащей 12–18 атомов углерода; метильного, этильного или бензильного радикала; хлора, брома, йода или остатка метилили этилсульфата.
Амфолитные ПАВ ионизируются в водном растворе различным образом в зависимости от условий среды: в кислом растворе проявляют катионоактивные свойства, а в щелочном – анионоактивные.
Неионогенные ПАВ представляют собой высокомолекулярные соединения, которые в водном растворе не образуют ионов. К неионогенным ПАВ относятся препараты ОП-7, ОП-10, ОС-20, оксанол КШ-9, оксанол Л-7, проксамин 385, проксанол 186, синтамид, синтанолы, ВН-7 и др.
В водные объекты ПАВ поступают в значительных количествах с хозяйственно-бытовыми (использование синтетических моющих средств в быту) и промышленными сточными водами (текстильная, нефтяная, химическая промышленность, производство синтетических каучуков), а так-
160
