
Радиобиология с основами радиоэкологии
.pdf
2. Типы ионизирующих излучений, их характеристика и дозиметрия |
41 |
|
|
как бы размазаны в пространстве, и один электрон может пребывать на различном удалении от ядра. Стало принятым говорить о так называемом «электронном облаке» в атоме (рис. 2.1), подразумевая при этом именно место нахождения электрона.
Радиус атома составляет около 10–8, а ядра всего 10–12–10–13 см. Но в ядре сосредоточено до 99.8% массы атома. Оно состоит из нуклонов – протонов и нейтронов.
Протон (р+) – это элементарная частица, имеющая одинаковый с электроном электрический заряд, но положительный. Масса протона в 1836 раз больше массы электрона, т.е. составляет 1.67×10–24 г. Протон – ядро самого простого по физическому строению элемента – атома водорода, положительный заряд которого нейтрализуется отрицательным зарядом единственного электрона.
Нейтрон (n) – электрически нейтральная частица массой, близкой массе протона. Поскольку нейтрон не имеет заряда, он не взаимодействует с электрически заряженными частицами, не отклоняется в магнитном поле, поэтому проникающая способность нейтронов в вещество весьма значительна.
Считается, что и протон, и нейтрон являются одними и теми же частицами, только находящимися в различных «зарядовых» состояниях, которые при определенных условиях могут переходить одна в другую.
Атомное ядро включает в себя множество других элементарных частиц, в том числе электроны, позитроны, нейтрино, антинейтрино, мезоны.
С радиобиологической точки зрения кроме электронов интерес представляют позитроны как возможный тип ионизирующих излучений. Позитрон (е+) – частица, идентичная по своим физическим свойствам электрону, но имеющая эквивалентный положительный заряд.
Несмотря на то, что эти частицы как бы дополнительно, кроме нуклонов, входят в состав ядра, масса его в свободном состоянии меньше суммы масс его протонов и нейтронов. Это
1Н
12С
23Na
Рис. 2.1. Схематическое изображение электронных оболочек атомов водорода, углерода и натрия.
42 |
Радиобиология с основами радиоэкологии |
|
|
не совсем понятное с обычной точки зрения явление получило название дефекта массы. Оно объясняется тем, что при объ единении нуклонов в атомное ядро часть массы не исчезает бесследно, а уносится с излучением, испускаемым при образовании системы.
Плотность ядра необычайно велика и достигает огромнейших, трудно представляемых значений – 214 г/см3, или 200 млн. т/см3.
Число протонов определяет электрический заряд и место атома в периодической системе элементов Д.И. Менделеева.
Атомные ядра с одинаковым количеством протонов, но раз ным количеством нейтронов называются изотопами. А ядра с одинаковым количеством нуклонов, но разным количеством протонов – изобарами.
Существуют атомы с устойчивыми (стабильными) и не устойчивыми (радиоактивными) ядрами. У изотопов элементов, расположенных в периодической системе после висмута, все ядра атомов радиоактивны.
Что же такое радиоактивность?
2.2. Явление радиоактивности. Закон радиоактивного распада
Нуклоны удерживаются в ядре за счет ядерных сил, природа которых изучена пока недостаточно. Они в тысячи раз сильнее электромагнитных и действуют на небольших расстояниях, не превышающих диаметр ядра. Согласно уже упомянутому принципу эквивалентности А. Эйнштейна, масса ядра меньше суммарной массы составляющих его нуклонов именно на величину энергии связи между ними. И разные ядра даже одного элемента с одинаковым количеством нейтронов, но с разным количеством протонов (изотопы) имеют разные энергии связи.
Атомные ядра большинства изотопов естественных элементов стабильны. Эта стабильность обусловлена балансом количества протонов и нейтронов в ядре. Так, в ядрах атомов изотопов легких элементов соотношение протонов и нейтронов составляет 1:1. Чем дальше от начала (водорода) располагается элемент в периодической системе, т.е. чем большей атомной массой он обладает, тем больше в нем количество нейтронов и у самых тяжелых примерно в 1.6 раз выше количества протонов. Именно они – 70 изотопов 25 элементов нестабильны. Предполагается, что они находятся еще в состоянии формирования. Данный процесс состоит во всевозможных ядерных превращениях, сопровождаемых ионизирующими излучениями.
2. Типы ионизирующих излучений, их характеристика и дозиметрия |
43 |
|
|
Ядерные превращения – это переход ядер атомов из одного состояния в другое с меньшей энергией, сопровождаемый испусканием высокоэнергетических частиц и (или) γ-квантов.
При поглощении ядром атома энергии извне стабильный изотоп может превращаться в радиоактивный и при последующем его распаде также выделять элементарные частицы и кванты. Именно поэтому наряду с естественной радиоактив ностью выделяют искусственную радиоактивность. К настоящему времени известно около 1880 искусственных радиоактивных изотопов практически всех химических элементов, полученных путем специального их облучения (бомбардировки) высокоэнергетическими частицами или в ядерных реакторах.
Таким образом, радиоактивность – это самопроизвольное или искусственное превращение ядер атома нестойкого изо топа химического элемента из основного состояния в другой изотоп этого или другого элемента, которое сопровождает ся выделением энергии путем испускания элементарных ча стиц или продуктов деления ядер. Такие ядра и соответствующие атомы называются радиоактивными. Определенный избыток энергии радиоактивных ядер при этом выделяется в виде γ-квантов. Именно γ-излучение сопровождает все типы радиоактивных распадов.
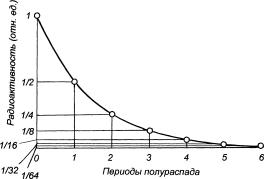
В связи с тем, что радиоактивное излучение является следст вием распада радиоактивного изотопа, оно ведет к постепенному уменьшению числа его атомов. Основной закон радиоактивного распада утверждает, что за единицу времени распадается одинаковая доля имеющихся в наличии ядер. Поэтому количество ядер радиоактивного изотопа со временем изменяется по экспоненциальной зависимости, т.е. графически закон радиоактивного распада описывается экспоненциальной кривой (рис. 2.2).
Для характеристики скорости распада радиоактивных изотопов на практике пользуются величиной, которая получила название периода полураспада. Период полураспада – это вре мя, в течение кото рого количество ато мов радиоактивного изотопа уменьшает ся в два раза.
Для различных радиоактивных изотопов период полураспада составляет от долей секунды до миллиардов лет. В связи с этим они подразделяются на короткоживущие (доли секунды,
44 |
Радиобиология с основами радиоэкологии |
|
|
секунды, минуты, часы, дни), среднеживущие (недели, месяцы, несколько лет), долгоживущие (десятки и тысячи лет) и сверхдолгоживущие (миллионы и миллиарды лет) изотопы.
Здесь, однако, следует кратко остановиться на некоторых очень важных терминологических особенностях.
В радиобиологической литературе, как научной, так и учебной (и это учебное пособие – не исключение), в отношении названия источников ионизирующих излучений нередко как равнозначные понятия используются термины «радиоактивный изотоп», «радиоактивный элемент», «радиоактивное вещество», «радионуклид». В некоторых случаях это оправдано и не является большой ошибкой. Тем не менее, их следует различать.
Изотопы, как уже отмечалось, – разновидности атомов одного элемента, обладающие одинаковым электрическим зарядом, но различными массовыми числами, т.е. имеющие разное количество нуклонов при одинаковом количестве протонов. Общеизвестно, что большинство химических элементов в природе представлено несколькими изотопами. Некоторые из них могут быть радиоактивными.
Радиоактивный изотоп – это неустойчивый, т.е. распадающийся изотоп химического элемента. Например, элемент калий представлен тремя изотопами: 39К, 40К и 41К. Первый и последний из них – устойчивые, стабильные, а 40К – радиоактивный. Термины «изотоп», «радиоактивный изотоп» используются обычно в тех случаях, когда говорится об атомах одного и того же элемента.
Радиоактивный элемент – это химический элемент, все изотопы которого радиоактивны. Например, уран, состоящий из трех вышеупомянутых радиоактивных изотопов, торий – из пяти, радон – из трех, радий – из четырех, полоний – из восьми изотопов и другие, в состав которых входят исключительно радиоактивные изотопы. Калий не является радиоактивным элементом, так как в его состав кроме радиоактивного изотопа входят и нерадиоактивные изотопы.
Радиоактивное вещество – это химическое вещество, в со став которого входит хотя бы один радиоактивный изотоп. При этом понимают химическое соединение, т.е. такое вещество, где элементы, как радиоактивные, так и нерадиоактивные, объединены с помощью химических связей, например, 40КНСО3, К3НСО3, КН14СО3. Радиоактивные изотопы, радиоактивные нуклиды и радиоактивные элементы в природе представлены обычно в составе радиоактивных веществ и очень редко встречаются в свободном состоянии.
Понятие «нуклид» объединяет понятия «изотоп» и «изобар», т.е. это атомы элемента, имеющие различное количество нуклонов в ядре или состоящие из различного числа протонов и нейтронов при одинаковом количестве нуклонов.
2. Типы ионизирующих излучений, их характеристика и дозиметрия |
45 |
|
|
Радионуклид, или радиоактивный нуклид, – неустойчивый, распадающийся нуклид. Термин «радионуклид» обычно используют для определения радиоактивных атомов радиоактивных веществ, потому что, как правило, радиоактивные изотопы и изобары бывают в составе соединений и очень редко – в свободном состоянии. Например, говорят о радионуклидах 89Sr и 90Sr, 131I и 133I, 134Сs и 137Сs, 95Nb и 95mNb, 137mBa и 140Ba. Значок «m» отличает изобар от изотопа, подчеркивая, что атом имеет ту же массу, но другое количество протонов.
2.3. Типы ядерных превращений
Хотя в начале этой главы говорилось о потоках электронов, которые возникают при действии ионизирующих излучений и приводят к различным повреждениям веществ, следует подчеркнуть, что первичным источником излучений являются ядра атомов, а не их электронные оболочки. Это совершенно очевидно, например, для альфа-радиации (α-радиации), так как
воболочке нет протонов и нейтронов, образующих α-частицу, но не совсем понятно для бета-частиц (β-частиц), которые не входят
всостав ядра. Они возникают в ядре в процессе его распада при превращениях нейтронов в протоны. И α-, и β-распады сопровождаются излучением γ-квантов. Именно поэтому ионизирующие излучения еще называют ядерными излучениями.
Основными типами ядерных превращений, или радиоактивного распада, являются α-распад, β-распад (электронный и
позитронный), электронный захват и внутренняя конверсия. α-распад. Этот тип радиоактивного распада состоит в испу-
скании ядром радиоактивного изотопа частицы, представляю-
щей собой ядро атома гелия, которое включает два протона и два нейтрона – α-частицу. Таким образом, ядро теряет два протона и два нейтрона и превращается в другое ядро, в котором
заряд ядра уменьшен на два, а массовое число – на четыре. Следовательно, при α-распаде образующийся дочерний изотоп смещается влево или вверх относительно исходного материнского на две клетки периодической системы элементов, т.е. превращается в изотоп другого элемента, естественно, с меньшей атомной массой и электрическим зарядом. Например:
23892U → 24He + 23490Th + Q,
где Q – выделяющаяся энергия.
α-распад характерен для большинства радиоактивных ядер тяжелых элементов с атомной массой более 82.
β-распад. Выделяют электронный β–-распад и позитронный β+-распад. Если нестабильность ядра обусловлена избыт-
46 |
Радиобиология с основами радиоэкологии |
|
|
ком нейтронов, то происходит электронный β-распад, при котором нейтрон превращается в протон, а ядро испускает электрон и антинейтрино. При этом заряд ядра, а следовательно, атомный номер изотопа увеличивается на единицу, и дочерний изотоп сдвигается на один номер вправо от материнского, становясь изотопом другого элемента, но массовое число остается без изменения. Типичным примером электронного β-распада является распад естественного радиоактивного изотопа 40К с превращением его в стабильный изотоп 40Са, которое сопровождается γ-излучением:
4019К → β– + 4020Са + γ.
Если нестабильность ядра обусловлена излишком протонов, то происходит позитронный распад, при котором испускается позитрон – частица такой же массы, что и электрон, но с положительным электрическим зарядом, и нейтрино. При этом один из протонов превращается в нейтрон. Заряд ядра и соответственно атомный номер изотопа уменьшается на единицу, а дочерний изотоп сдвигается влево от материнского, тоже становясь изотопом другого элемента. Массовое число остается без изменения. Примером такого распада может быть превращение радиоактивного изотопа фосфора 30P в стабильный изотоп кремния 30Si, составляющего 3.05% всего имеющегося на планете кремния:
1530P → β+ + 1430Si + γ + Q.
Вылетевший из ядра позитрон взаимодействует с электроном оболочки, образуя пару позитрон-электрон, которая превращается в два γ-кванта. Этот процесс называется аннигиляцией (превращением), а возникающее γ-излучение – аннигиляционным. В итоге при позитронном распаде за пределы атома вылетают не ядерные частицы, а γ-кванты и β-распадающийся изотоп фактически оказывается источником γ-радиации.
Электронный захват. Этот тип ядерного превращения состоит в захвате одним из протонов ядра электрона с орбиты, обычно ближайшей. При этом протон превращается в нейтрон, а порядковый номер ядра становится на единицу меньше порядкового номера материнского ядра, хотя массовое число не меняется. Изотоп нового элемента занимает место в периодической системе на одну клетку влево.
Типичный пример электронного захвата – поглощение электрона ядром 40К, следствием которого является возникновение 40Аr:
2. Типы ионизирующих излучений, их характеристика и дозиметрия |
47 |
|
|
Избыток энергии, высвободившейся при реакции, испускается в виде γ-излучения.
Таким образом, естественный радиоактивный изотоп 40К одновременно может подвергаться электронному β-распаду (88%)
собразованием β- и γ-излучения и электронному захвату (12%)
собразованием γ-излучения.
Внутренняя конверсия. В результате тех или иных превращений ядро атома переходит в возбужденное состояние. Возврат к нормальному состоянию всегда сопровождается либо выбрасыванием ядерной частицы, либо излучением γ-кванта. Но нередко при этом избыточная энергия возбуждения передается электрону одной из ближайших орбит. В результате такой передачи электрон вырывается за пределы атома. Это и порождает конверсионное электронное излучение, которое, по сути, представляет собой поток электронов. Однако в отличие от электронов β-распада, дающих электроны сплошного энергетического спектра, конверсионные электроны имеют линейчатый спектр, т.е. занимают в нем определенные достаточно узкие диапазоны.
Ядерная физика рассматривает и некоторые другие типы и разновидности ядерных превращений, но в общем количестве ядерных распадов им отводится относительно небольшая роль.
2.4. Типы ионизирующих излучений
Ионизирующие излучения всех естественных и искусственных источников подразделяются на два типа: электромагнитное и корпускулярное.
2.4.1. Электромагнитное ионизирующее излучение Электромагнитное, или фотонное ионизирующее излуче-
ние представляет собой поток периодических электрических и магнитных колебаний, которые отличаются от радиоволн, видимого и ультрафиолетового света более короткой длиной волны и более высокой энергией, находящихся между собой в обратной зависимости. К ним в первую очередь относятся самые используемые в радиобиологических исследованиях и практике рентгеновское и γ-излучение радиоактивных изотопов, а также тормозное излучение, возникающее при прохождении через вещество ускоренных заряженных частиц.
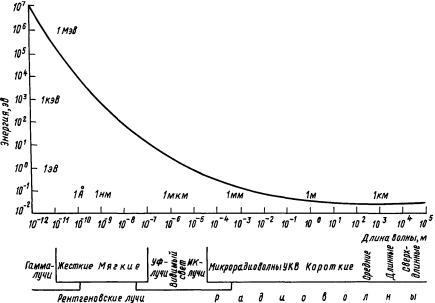
Рентгеновское излучение (Х) – это электромагнитное излучение, занимающее спектральную область между γ- и ультрафиолетовым излучениями в диапазоне длин волн от 10–11 до 10–7 м. Иногда выделяют рентгеновское излучение и с более короткой длиной волны – до 10–14 м. Условно рентгеновское излучение с длинами волн менее 2 ангстрем (2×10–10 м) называют жестким, а с длинами волн свыше 2 ангстрем – мягким (рис. 2.3). Иногда выделяют сверхжесткое рентгеновское излучение с еще бо-
48 |
Радиобиология с основами радиоэкологии |
|
|
Рис. 2.3. Зависимость энергии электромагнитных излучений от длины волны.
лее короткой длиной волны и соответственно более высоких энергий – до 1 МэВ. Данные названия широко используются в практической радиобиологии, в первую очередь – в радиационной медицине.
γ-излучение – один из видов ионизирующих излучений, испускаемых ядрами атомов многих естественных (226Rа) и искусственных (60Со, 137Сs) радиоактивных изотопов; представляет собой электромагнитное излучение с чрезвычайно малой длиной волны – 10–12–10–11 м и даже короче. На шкале электромагнитных волн, приведенной на рис. 2.3, оно граничит с жестким рентгеновским излучением и несколько перекрывая его, занимает область самых коротких волн.
Соответственно энергия рентгеновских излучений составляет от нескольких десятков сотен до сотен тысяч, а γ-излучений – от десятков тысяч до миллионов электронвольт.
Тормозное излучение – тоже рентгеновское и γ-излучение, которое возникает при прохождении через вещество и торможении заряженных ядерных частиц или продуктов деления ядер, образующихся при самопроизвольном и искусственном расщеплении ядер урана и плутония и других ядерных реакциях. Иногда в понятие тормозного излучения включают излучение заряженных частиц, движущихся в магнитном поле ускорителя, в космическом пространстве. В данном случае его еще называют магнитотормозным. Хотя чаще используется термин
2. Типы ионизирующих излучений, их характеристика и дозиметрия |
49 |
|
|
«синхротронное излучение». Классическим примером тормозного излучения является рентгеновское излучение рентгеновской трубки, возникающее при резком торможении потока электронов, ускоренных до энергий выше 12 кэВ, при их столкновении с атомами вольфрама, из которого изготавливается анод.
2.4.2. Корпускулярное ионизирующее излучение Корпускулярное ионизирующее излучение представляет
собой поток частиц (корпускул), характеризующихся в отличие от электромагнитного излучения не только энергией, но еще массой и электрическим зарядом, о котором уже говорилось в первом разделе этой главы. В зависимости от последних двух свойств частицы подразделяются на легкие и тяжелые, заря женные и нейтральные.
α-частицы – поток ядер атомов гелия. Относятся к тяжелым частицам, состоящим из двух протонов и двух нейтронов и имеющим, соответственно, два элементарных положительных заряда.
β-частицы (е–) – поток электронов – легчайших отрицательно заряженных элементарных частиц, испускаемых атомным ядром.
Вещество может стать источником электронов, если к нему будет подведено достаточное количество энергии. Так, если в вакууме создать электрическое поле и нагреть вольфрамовый катод до белого каления, он начинает испускать электроны оболочек атомов. Это будет поток электронов, но не β-частиц. Хотя при одинаковых энергиях их действие на вещество будет одинаковым.
Позитроны (е+) – легкие элементарные частицы, испускаемые ядром, идентичные по своим свойствам электрону, но имеющие не отрицательный, а положительный электрический заряд. В отличие от β-частицы, которую называют еще бета-ми- нус-частица, позитрон именуют бета-плюс-частица.
Протоны (р) – тяжелые положительно заряженные элементарные частицы, ядра атомов водорода, входящие в состав атомных ядер всех химических элементов. Протон несет одинаковый с электроном и позитроном электрический заряд, но имеет массу в 1836 раз большую. При поглощении ядром атома энергии извне и последующем распаде протон внутри ядра может превратиться в нейтрон. Процесс сопровождается рождением позитрона и нейтрино – электрически незаряженной элементарной частицы с массой покоя, много меньшей электрона.
Нейтроны (n) – тяжелые, не обладающие электрическим зарядом, т.е. нейтральные элементарные частицы с массой, близкой массе протона. Нейтроны относятся к классу сильно взаимодействующих с веществом частиц и в отличие от тяжелых заряженных частиц (α-частиц, протонов, дейтронов) легко про-
50 |
Радиобиология с основами радиоэкологии |
|
|
никают вглубь атомов и, достигая атомных ядер, поглощаются либо рассеиваются на них. Именно при поглощении нейтронов атомные ядра становятся неустойчивыми и в последующем распадаясь, испускают протоны, α-частицы, γ-излучение – приобретают искусственную, или как еще называют, наведенную ра диоактивность.
В зависимости от энергии принята следующая условная классификация нейтронов: ультрахолодные нейтроны (до 10–7 эВ), очень холодные (10–7–10–4 эВ), холодные (10–4–5×10–3 эВ), тепловые (5×10–3–0.5 эВ), резонансные (0.5–104 эВ), промежуточные (104–105 эВ), быстрые (105–108 эВ), высокоэнергетические (108– 1010 эВ) и релятивистские (более 1010 эВ). Все нейтроны с энергией до 105 эВ объединяют под общим названием – медленные нейтроны. Наибольшее практическое значение в радиобиологических работах имеют быстрые нейтроны.
Дейтроны (d) – ядра атомов изотопа водорода дейтерия, или тяжелого водорода, тяжелые положительно заряженные частицы. Дейтроны – простейшая в природе ядерная система, состоящая всего из двух частиц – протона и нейтрона, связанных между собой внутриядерными силами.
В табл. 2.1 приведены главные физические характеристики рассмотренных основных типов ионизирующих излучений, широко применяемых в радиобиологических работах. Они свидетельствуют о разной природе излучений и однозначно указывают на то, что в зависимости от энергии, массы и заряда различным будет и их взаимодействие с веществом.
Физические характеристики основных типов |
Таблица 2.1 |
|||||
|
|
|||||
|
ионизирующих излучений |
|
|
|
||
|
|
|
|
|
|
|
Тип |
Символ |
Энергия, эВ |
Длина волны, м |
Заряд, Кл |
|
Масса, г |
|
|
Электромагнитное |
|
|
|
|
Рентгеновское |
Х |
5.101–5.105 |
10–11–10–7 |
– |
|
– |
Гамма |
γ |
5.105–5.106 |
10–12–10–11 |
– |
|
– |
Тормозное |
Х + γ |
104–106 |
10–11–10–9 |
– |
|
– |
|
|
Корпускулярное |
|
|
|
|
Электроны (бета) |
е– (β)– |
103–1.7.106 |
– |
–1.6.10–19 |
|
9.31.10–28 |
Позитроны |
е+ |
|
– |
+1.6.10–19 |
|
9.31.10–28 |
Протоны |
p |
|
– |
+1.6.10–19 |
|
1.67.10–24 |
Нейтроны |
n |
|
– |
0 |
|
1.67.10–24 |
Дейтроны |
d |
|
– |
+1.6.10–19 |
|
3.34.10–24 |
Альфа |
α |
5.29.106 |
– |
+3.2.10–19 |
|
6.68.10–24 |
