
Основы физической химии_Ерёмин
.pdf

170 |
|
Г л а в а |
2. Приложения химической термодинамики |
|
|||||||||||
|
|
При p = 100 Торр степень заполнения |
|
|
|
||||||||||
|
|
|
|
θ = |
|
|
K L p |
= |
|
|
0.0046 100 |
= 0.315 . |
|
|
|
|
|
|
|
1 |
+ K L p |
1 |
+ 0.0046 100 |
|
|||||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
Пример 10-2. При исследовании адсорбции азота на 1 г активиро- |
|||||||||||||
|
|
ванного угля при 273 К получены следующие результаты (объем по- |
|||||||||||||
|
|
глощенного газа пересчитан к н. у.): |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
p, Торр |
|
|
4.5 |
|
|
|
9.2 |
|
18.6 |
|
40.2 |
||
|
|
V, см3 г–1 |
|
|
1.12 |
|
|
|
2.22 |
|
4.22 |
|
8.02 |
||
Выясните, описываются ли эти данные изотермой Ленгмюра и определите площадь поверхности адсорбента, если в плотном монослое молекула азота занимает площадь 0.162 нм2.
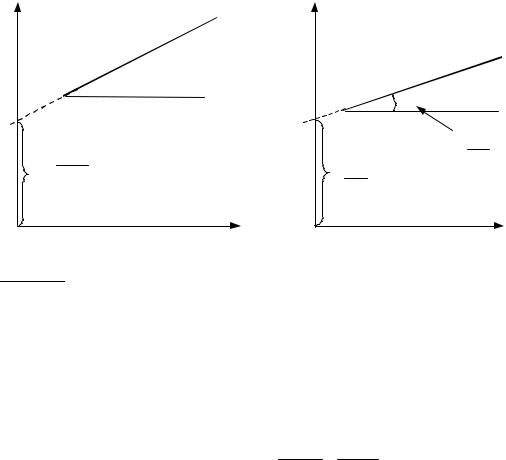
Решение. Воспользуемся линейной формой уравнения Ленгмюра в виде:
|
|
p |
= |
1 |
+ |
1 |
p . |
|
||
|
|
|
Vm K L |
|
|
|||||
|
V |
Vm |
|
|
|
|||||
Составляем вспомогательную таблицу: |
|
|
|
|||||||
|
|
|
|
|
9.2 |
|
|
|
||
p, Торр |
4.5 |
|
|
|
18.6 |
40.2 |
||||
p/V, Торр см–3 г |
4.0179 |
|
4.1441 |
|
4.4076 |
5.0125 |
||||
Данные таблицы можно представить в виде графика; угловой коэффициент равен 1/Vm, а по отрезку, отсекаемому на оси ординат, рассчитывается величина 1/VmKL. Более точные значения параметров Vm и KL получаются при статистической обработке данных, например, методом наименьших квадратов:
p |
= 3.89 + 2.787 10−2 p , т.е. |
1 |
= 2.787 10−2 , Vm =35.9 см3 г−1 . |
V |
|
||
|
Vm |
||
При н. у. объем, занимаемый 1 молем газа, Vo = 22.4 л; площадь, занимаемая 1 молекулой – 16.2 10–20 м2. Тогда
Ω = s NA Vm/Vo = 16.2 10–20 м2 6.02 1023 моль–1 35.9 10–3 л г–1 / 22.4 л моль–1 = 156.3 м2г–1.
Пример 10-3. При 312 К и давлении 1.21 Торр на поверхности микропористого глинистого адсорбента сорбируется 1.37 моль кг–1 паров метилового спирта. Такая же адсорбция достигается при повышении температуры до 320 К и увеличении давления до 3.16 Торр. Вычислите энтальпию адсорбции метилового спирта при данной степени заполнения поверхности.
Решение. Энтальпия адсорбции равна
∆адсH = |
RT1T2 |
ln |
p2 |
= |
8.314 312 320 |
ln |
3.16 |
= –99603 Дж моль–1. |
|
T1 −T2 |
p1 |
−8 |
1.21 |
||||||
|
|
|
|
|

Г л а в а 2. Приложения химической термодинамики |
171 |
Пример 10-4. Для водных растворов фенола при 20 °С измерены значения поверхностного натяжения (см. таблицу). Рассчитайте адсорбцию фенола Г2 при концентрации 0.2 моль л–1.
с, моль л–1 |
0.05 |
0.127 |
0.268 |
0.496 |
σ103, Н м–1 |
67.88 |
60.10 |
54.58 |
44.97 |
Решение. Для определения адсорбции нам понадобятся вспомогательные данные ln c:
ln с |
–2.9957 |
–2.0636 |
–1.3168 |
–0.7012 |
σ103, Н м–1 |
67.88 |
60.10 |
54.58 |
44.97 |
Строим график зависимости σ = f(ln c).
7.00E–02
6.00E–02
|
σ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5.00E–02 |
|
|
σ = – 0.0009(lnc)2 – 0.0136(lnc) + 0.0357 |
|
|||||
|
|
|
|
|
|
|
|
4.00E–02 |
|
– 4 |
|
–3 |
|
–2 |
–1 |
0 |
|
|
|
|
|
|
|
– lnc |
|
|
Графическим или аналитическим дифференцированием находим |
||||||||
|
|
|
|
∂σ |
|
= −0.0107 Н м−1 . |
||
|
|
∂ ln c2 |
|
|||||
|
|
T ,c=0.2 |
|
|
||||
Соответственно, |
|
|
|
|
|
|
||
Г21 = − |
|
∂σ |
|
= − |
|
−0.0107 |
= 4.39 10−6 |
моль м−2 = 4.39 10−10 моль cм−2 . |
1 |
|
|
||||||
|
RT |
∂ ln p2 T |
8.314 293 |
|
|
|||
ЗАДАЧИ
10-1. Сколько литров аммиака при 273 К и 1 атм может адсорбироваться на поверхности 25 г активированного угля, если образуется мономолекулярный слой? Поверхность 1 г угля примите равной 950 м2. Диаметр молекулы 3 Å.
172 |
Г л а в а 2. Приложения химической термодинамики |
10-2. Вычислите площадь поверхности катализатора, 1 г которого при образовании монослоя адсорбирует при н. у. 83 г азота. Примите, что эффективная площадь, занятая молекулой азота, равна 16.2 10–20 м2.
10-3. Удельная поверхность активированного угля 400 м2 г–1. Плотность метанола при 288 К 0.7958 г см–3. Определите максимальное количество метанола, которое может адсорбировать 1 г угля при 288 К при образовании мономолекулярного слоя.
10-4. Объем бутадиена, адсорбированного на 1 г катализатора при 15 °С, зависит от давления следующим образом
p, Торр |
50 |
150 |
250 |
350 |
450 |
Va, см3 |
9.6 |
25.6 |
40.3 |
54.4 |
68.1 |
Какое уравнение – Ленгмюра или Фрейндлиха – позволяет получить адекватное описание экспериментальных данных? Определите параметры уравнения.
10-5. При адсорбции доксициклина на высокодисперсном кремнеземе при pH = 6 (фосфатный буфер, навеска кремнезема 0.2 г, объем 20 мл) получены следующие значения адсорбции:
с 104 моль л–1 |
0.5 |
1 |
2 |
4 |
8 |
a 105 моль г–1 |
0.68 |
1.08 |
1.53 |
1.9 |
2.26 |
С помощью какого уравнения лучше описывать экспериментальные данные? Определите параметры этого уравнения.
10-6. В результате исследования сорбции натриевой соли бензилпенициллина из водных растворов на поверхности высокодисперсного пирогенного аминокремнезема ([NH2] = 0.3 ммоль г–1) получены следующие значения адсорбции:
с 103 моль л–1 |
0.25 |
0.5 |
2 |
6 |
a 102 моль г–1 |
1.88 |
2.80 |
4.98 |
6.20 |
Рассчитайте константу адсорбционного равновесия и предельную величину адсорбции, если процесс сорбции описывается уравнением Ленгмюра.
10-7. Найдите степень заполнения поверхности аэросила при адсорбции натриевой соли бензилпенициллина из растворов концентрации 0.004, 0.0075 и 0.011 М, если адсорбция описывается уравнением Ленгмюра с константой адсорбционного равновесия 790 М–1.
10-8. Оцените изменение степени заполнения поверхности кальцита при адсорбции комплексона-А из 0.00002 М раствора при разных зна-

Г л а в а 2. Приложения химической термодинамики |
173 |
чениях pH. Концентрация фонового электролита 0.02 М NaCl. Константы адсорбционного равновесия приведены в таблице:
pH |
8.7 |
9.5 |
10.5 |
K 10–5, л моль–1 |
3.5 |
3.4 |
3.3 |
10-9. При 15 °С из водно-спиртового раствора (0.6 : 0.4) концентрации 5 мкмоль л–1 на поверхности сорбента Separon BD адсорбируется 44.1 мкмоль г–1 антрацена и 22.0 мкмоль г–1 пирена. При увеличении их содержания в растворе до 10 мкмоль л–1 количество адсорбированных веществ увеличивается до 54.7 и 46.8 мкмоль г–1 соответственно. Рассчитайте степень заполнения поверхности в каждом случае.
10-10. При адсорбции паров метилового спирта на микропористом глинистом адсорбенте получены следующие величины адсорбции:
p/ps |
0.01 |
0.07 |
0.25 |
0.44 |
0.64 |
0.90 |
a, моль кг–1 |
0.70 |
1.00 |
1.28 |
1.55 |
1.85 |
2.55 |
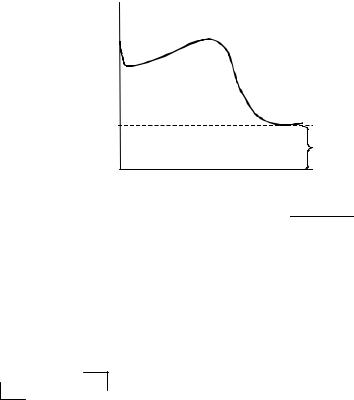
Постройте изотерму адсорбции, предложите ее аналитическое описание и рассчитайте значение am.
10-11. Давление при адсорбции некоторого количества СH4 1 г древесного угля равно 42 Торр при 313 К и 261 Торр при 363 К. Вычислите теплоту адсорбции при данной степени заполнения.
10-12. При адсорбции этана на поверхности графитированной сажи степень заполнения θ = 0.5 достигается при следующих значениях температуры и давления: 173 К, 2.15 Торр и 188 К, 7.49 Торр. Найдите изостерическую теплоту адсорбции.
10-13. Определите энтальпию адсорбции окиси азота на фториде бария, если для адсорбции 4 см3 газа при 233 К необходимо создать давление
40.7 Торр, а при 273 K – 206.5 Торр.
10-14. Исследуя адсорбцию СО на древесном угле обнаружили, что для того, чтобы при разных температурах адсорбировалось 10 см3 газа (объемы приведены к н. у.), необходимо задать следующие равновесные давления
T, K |
200 |
220 |
230 |
250 |
p, торр |
30.0 |
45.2 |
54.0 |
73.9 |
Определите изостерическую теплоту, соответствующую данной величине адсорбции.
10-15. Для адсорбции N2 на 1 г кремнеземных материалов с различным размером пор при 77 K получены приведенные в таблице зависимости объемов адсорбированного газа (Vадс, измерены в см3) от давления. Объемы приведены к стандартному давлению. Одна молекула N2 зани-

Глава
3 Электрохимия
§ 11. Термодинамика растворов электролитов
Электролитами называют вещества или системы, содержащие в заметных количествах ионы и обладающие ионной проводимостью. Со-
ответственно, различают твердые электролиты, расплавы и растворы электролитов. В более узком смысле электролитами называют вещества, молекулы которых в растворе способны распадаться на ионы в результате процесса электролитической диссоциации. Растворы электролитов также часто называют электролитами.
По способности к электролитической диссоциации электролиты условно разделяют на сильные и слабые. Сильные электролиты в разбавленных растворах практически полностью диссоциированы на ионы. Слабые электролиты в растворах диссоциированы лишь частично. Доля диссоциированных молекул электролита называется степенью диссоциации. Степень диссоциации α электролита связана с константой диссоциации K законом разведения Оствальда, который для бинарного электролита записывается следующим образом:
K = |
α 2c |
= |
|
α 2 |
|
1 |
, |
(11.1) |
|
1 − α |
1 − α |
V |
|||||||
|
|
|
|
|
|||||
где c – молярность электролита, V = 1/c – разведение (или разбавление) раствора, т.е. объем, в котором содержится 1 моль электролита.
Поскольку при диссоциации число частиц в растворе возрастает, растворы электролитов обладают аномальными коллигативными свойствами. Уравнения, описывающие коллигативные свойства растворов неэлектролитов, можно применить и для описания свойств растворов электролитов, если ввести поправочный изотонический коэффициент Вант-Гоффа i, например:
π = icRT или ∆Tзам. = iKm. |
(11.2) |
