
- •«Башкирский государственный аграрный университет»
- •Контрольные вопросы
- •2 Лабораторная работа
- •3 Лабораторная работа
- •4 Лабораторная работа
- •5 Лабораторная работа
- •5.4 Анализ одиночного сокращения скелетной мышцы (оссм)
- •6 Лабораторная работа
- •7 Лабораторная работа
- •8 Лабораторная работа
- •8.2 Иррадиация, суммация возбуждения нервных центрах
- •9 Лабораторная работа
- •10 Лабораторная работа
- •11 Лабораторная работа
- •12 Лабораторная работа
- •13 Лабораторная работа
- •14 Лабораторная работа
- •15 Лабораторная работа
- •16 Лабораторная работа
- •17. Лабораторная работа
- •18 Лабораторная работа
- •19 Лабораторная работа
- •20 Лабораторная работа
- •21 Лабораторная работа
- •22.Лабораторная работа
- •22.2 Оборудование, приборы: водяной спирометр, вата, спирт.
- •22.3 Ход работы.
- •23 Лабораторная работа
- •24. Лабораторная работа
- •24.3 Перечень контрольных вопросов по разделу «Физиология крови,
- •25 Лабораторная работа
- •26 Лабораторная работа
- •27 Лабораторная работа
- •28 Лабораторная работа
- •28.4 Вопросы к контрольной по физиологии пищеварения и
- •29 Лабораторная работа
- •30 Лабораторная работа
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ
Ф ЕДЕРАЛЬНОЕ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ
УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО
ОБРАЗОВАНИЯ
ЕДЕРАЛЬНОЕ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ
УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО
ОБРАЗОВАНИЯ
«Башкирский государственный аграрный университет»
Кафедра кормления
животных и физиологии
С. 2. Б. 9 ФИЗИОЛОГИЯ И ЭТОЛОГИЯ ЖИВОТНЫХ
Методические указания
к выполнению лабораторных работ по
направлению подготовки дипломированного специалиста
Специальность 111801 Ветеринария
Уфа 2012
УДК 636
ББК 45/46
М 54
Рекомендовано к изданию методической комиссией факультета ветеринарной медицины (протокол № 1 от 3 сентября 2012 г.)
Составитель: доцент Ганиев С.Б.
Рецензент: профессор Дементьев Е.В.
Ответственный за выпуск - заведующий кафедрой кормления животных и физиологии Хабиров А.Ф.
1 Лабораторная работа
Введение в предмет. Техника безопасности при проведений занятий. Методы исследований. Приборы и инструменты используемые в физиологии. Фиксация, успокоение, наркоз и обезболивание животных
1.1 Введение.
Практический курс по физиологии ставит целью ознакомить студентов с основными процессами жизнедеятельности здорового животного организма, функциями составляющих его частей (органов, тканей, клеток и субклеточных структур), механизмами проявления функций и их регуляцией.
Работая с животными следует постоянно руководствоваться указанием И. П. Павлова о том, что при изучении каких-либо процессов организма можно использовать любой метод (наблюдение или эксперимент), лишь бы он позволял не нарушая целостности связей наблюдать и количественно учитывать происходящие в нем изменения.
Кроме того, работая с животными, следует соблюдать гуманное отношение к ним. Если же и проводятся болевые опыты, их необходимо выполнять с применением анестезии или общего наркоза.
При выполнении заданий необходимо строго соблюдать основные положения по охране труда и технике безопасности. Для предотвращения травм все манипуляции, связанные с проведением учебных занятий, следует выполнять на фиксированных животных.
При многообразии лабораторных и сельскохозяйственных животных им всем присущи общие закономерности функций организма.
1.2 Техника безопасности при выполнении лабораторных работ по физиологии и этологии
При изучении дисциплины – физиология применяют методы наблюдения, постановки острого и хронического опыта с использованием хирургических инструментов разнообразных приборов и оборудования в том числе питаемых от электрической сети.
Для обеспечения безопасности при проведении занятий студенты должны выполнять основные правила безопасной работы.
1. На занятия приходить в халатах.
2. Лабораторные работы выполняются после ознакомления с методикой постановки опыта и ознакомления с прибором при его использовании по соответствующей теме.
3. Работа со сложными и ценными приборами выполняется только под наблюдением и при участии преподавателя.
4. Приборы и оборудование, питаемые от сети не должны иметь оголенных проводов по которым проходит электрический ток выше 24 вольт, все приборы должны иметь заземление.
5. Для безопасной работы с животными и получения достоверных результатов необходимо уметь обездвиживать и обезболивать лабораторных и с.х. животных.
6. Студенты обязаны относится бережно к оборудованию и приборам. О нарушителях учебной дисциплины сообщается в деканат.
1.3 Методы исследований.
Проведение исследований физиологических функций организма животных проводится в специализированной лаборатории или в производственных условиях: животноводческих помещениях, пастбище и др.
В производственных условиях применяют методы наблюдения с использованием отдельных приборов и оборудованиях (стетфонендоскопы, набор для получения крови, исследование рефлексов имеющих клиническое значение с комплексом дистанционной регистрации функций и др.).
В специализированной лаборатории проводят исследования по форме хронического опыта на сложно – оперированных животных, либо с использованием сложного стационарного диагностического оборудования и приборов.
Методика применения острого опыта практикуется только в экспериментах на мелких лабораторных животных при исследованиях на тканевом или клеточном уровнях.
1.4 Приборы и инструменты используемые в физиологии
Сложные процессы и функции организма не могут быть изучены только путем визуального наблюдения за животными. Для получения глубоких знаний и достоверных результатов необходимо проведение опытов, выполнение которых возможно с использованием различных инструментов, приборов и аппаратов.
Весь обширный набор разнообразного лабораторного оборудования можно условно разделить, в зависимости от назначения, на отдельные группы.
Приборы показывающие величины измерения. В эту группу входят приборы, имеющие шкалу измерения (например, спирометр, тонометр и др.).
Приборы для графической регистрации функций (например: кимограф, миограф, ЭКГ, ЭЭГ, руминограф и др.).
Вспомогательные приборы, инструменты и приспособления (например: центрифуги, микроскопы, хирургические инструменты, штативы и др.).
При выполнении физиологических опытов для поддержания осмотического равновесия и влажности тканей применяют различные растворы (таблица 1.1).
Таблица 1.1 Состав растворов для физиологических исследований, %
|
Растворы |
NaCl |
KCl |
CaCl2 |
NaHCO3 |
Глюкоза |
MgCl2 |
NaH2PO4 |
|
Для тканей лягушек | |||||||
|
Физиологический |
0,65 |
- |
- |
- |
- |
- |
- |
|
Рингера |
0,6 |
0,0075 |
0,01 |
0,01 |
- |
- |
- |
|
Для тканей млекопитающих | |||||||
|
Физиологический |
0,85 - 0,9 |
- |
- |
- |
- |
- |
- |
|
Рингера |
0,9 |
0,042 |
0,024 |
0,02 |
- |
- |
- |
|
Локка |
0,9 |
0,042 |
0,024 |
0,015 |
0,1 |
- |
- |
|
Тироде |
0,8 |
0,02 |
0,02 |
0,1 |
0,1 |
0,01 |
0,005 |
1.5 Фиксация, успокоение, наркоз, обезболивание животных
1.5.1 Фиксация лошади. Лошадь может укусить, ударить передней конечностью, чаще задней конечностью.

Рисунок 1.5.1 Способы фиксации спокойных лошадей
Спокойных лошадей держат за уздечку или коротко привязывают к столбу. При исследовании задних участков туловища у лошадей поднимают переднюю конечность, сгибая ее в запястном суставе, или одевают на конечности «случную шлею».
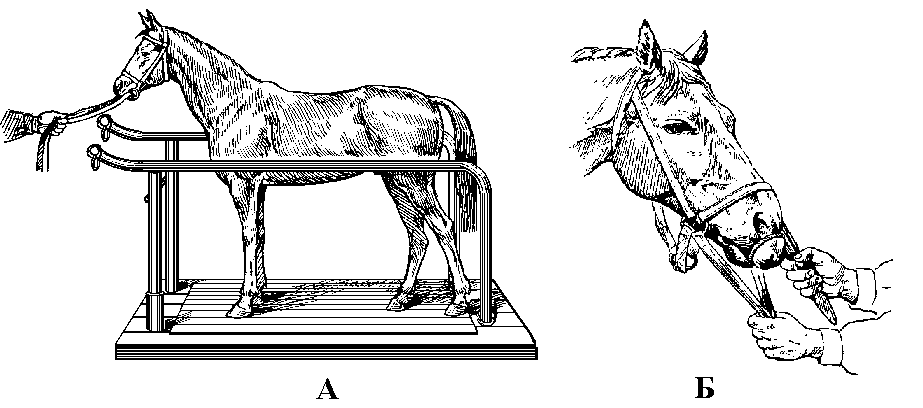
Рисунок 1.5.2 Фиксация строптивых лошадей
Строптивых животных фиксируют в деннике или станке
Как отвлекающее средство пользуются закруткой, которую накладывают на верхнюю губу или основание уха на 5 – 10 минут. При физиологических исследованиях закруткой пользоваться нежелательно.
При хирургических операциях лошадей наркотизируют и фиксируют на операционных столах (стол Юравичуса, стол-станок Виноградова ОСБ-240).
1.5.2 Фиксация крупного рогатого скота. Спокойных животных привязывают за рога к столбу или удерживают с помощью недоуздка.

Рисунок 1.5.3 Разборный фиксационный станок Виноградова
Удобным является фиксация в станке С. П. Виноградова (рисунок 1.5.3)

Рисунок 1.5.4Способы фиксация крупного рогатого скота
При необходимости прибегают к помощи отвлекающих средств – сдавливанию носогубного зеркальца пальцами (А), носовыми щипцами (Б) или носовым зажимом Кумсиева (В). При удерживании животного за рога необходимо большим пальцем прикрыть верхушку рога. Быков удерживают с помощью носового кольца и водила.
Для проведения хирургических операций животное фиксируют в стоячем положении, прижимая к стене манежа железной трубой, специально смонтированной на подвижной муфте или в лежачем положении на операционном столе.
1.5. 3.Фиксация мелкого рогатого скота. Овец и коз фиксируют в станках, клетках и операционных столах для мелких животных.
1.5.4 Фиксация свиньи. При фиксации в стоячем положении свиней используют узкие станки или специальные железные клетки, стенки которых при необходимости можно сблизить. При бесстаночной фиксации можно привязать свинью веревочной петлей за верхнюю челюсть к столбу, удерживать за верхнюю челюсть закруткой на длинной палке или специальными щипцами за верхнюю челюсть или за шею.
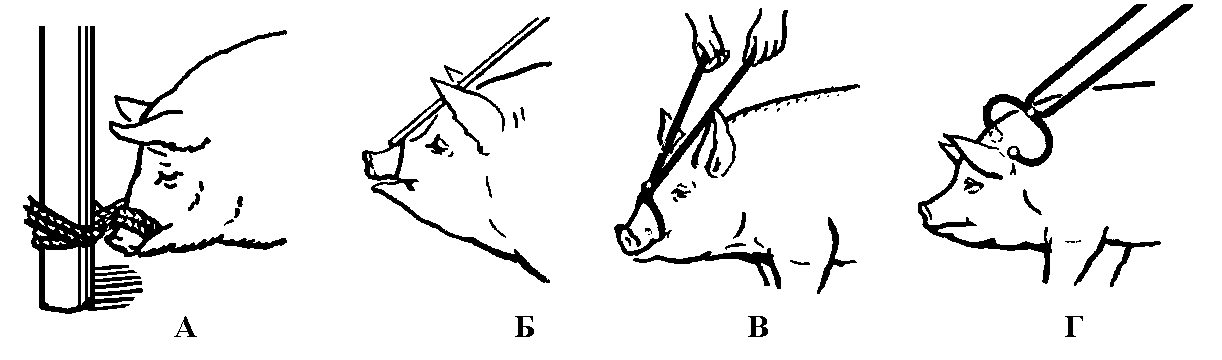
Рисунок 1.5.5 Способы фиксации свиней: А – веревочной петлей; Б – закруткой; В – щипцами за челюсть; Г – щипцами за шею
При операциях и острых опытах свиней фиксируют на операционных столах желобоватой формы или в корыте.
1.5.5 Фиксация птиц. Птицу одной рукой удерживают за основание крыльев, сжимая их, а другой рукой фиксируют лапки и голову.
1.5.6 Фиксация собаки. При проведении исследований во избежание укусов собаке надевают намордник или связывают челюсти тесьмой или бинтом. Для этого делают петлю, надевают ее на морду и завязывают одним простым узлом под подбородком и, проведя за ушами, бантиком на затылке. Фиксировать в этих случаях должен их владелец.
При проведении операций используют операционные столы для мелких животных.
1.5.7 Фиксация кошки. Кошку удерживают одной рукой за кожу на затылке, а другой – за кожную складку в поясничной области, или задние конечности.
На время операции кошку можно завернуть в кусок плотной ткани, оставляя открытым необходимый для операции участок. В спинном положении кошек фиксируют в специальном станке с головодержателем.
1.5.8 Фиксация кролика аналогично фиксации кошки.
1.5.9 Фиксация крыс и мышей. Крыс и мышей захватывают анатомическим пинцетом (рукой) за кожу на затылке и рукой за хвост.
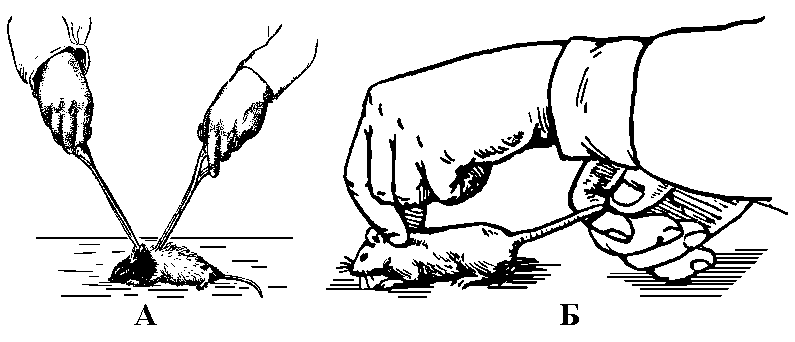
Рисунок 1.5.6 Фиксация крысы (А) и мыши (Б)
Острые опыты выполняют на мелких операционных столах.
1.5.10 Фиксация лягушки. Обездвиживают лягушек эфирным наркозом или разрушением центральной нервной системы препаровальной иглой. Для этого лягушку, завернув в салфетку, берут в левую руку так, чтобы указательный палец сгибал ее голову под углом к позвоночнику. За затылочной костью находят атланто-окципитальную ямку, покрытую мембраной, которую легко прокалывают иглой и, введя последнюю в спинномозговой канал, разрушают мозг.
После обездвиживания лягушку фиксируют булавками на препаровальной дощечке.
Успокоение животных в ветеринарной практике осуществляется миорелаксантами (веществами, вызывающими расслабление скелетной мускулатуры) и нейролептиками (веществами, понижающими возбудимость нервной системы). Они обладают слабыми обезболивающими, наркотическими свойствами.
Эти препараты применяются в следующих целях:
для успокоения строптивых, возбудимых животных при профилактических и экспериментальных процедурах (прививках, зондировании, взятии крови, перевозках, некоторых опытах, связанных с болевыми воздействиями);
для облегчения повала и последующей фиксации животных на операционных столах;
для продления и усиления действия наркотиков или анестетиков и ослабления побочных эффектов ("премедикация" наркоза).
Следует помнить, что высокие дозировки миорелаксантом (релаксин Г, диплацин, ромпун, рометар, стреснил и др.) могут вызывать резкое нарушение дыхания вплоть до его остановки.
Под влиянием нейролептических средств у животных наступает "сонливое" состояние, снижается болевая чувствительность, ослабляется мышечный тонус. Наиболее употребительными нейролептиками являются аминазин, дроперидол, галоперидол, калипсовет, комбелен.
Общее обезболивание, или наркоз – это воздействие на весь организм наркотическим веществом с целью потери болевой чувствительности.
По способу введения наркотика различают:
Ингаляционный наркоз – наркотик вводится путем ингаляции через дыхательные пути (например, эфир, хлороформ). Ингаляционный наркоз противопоказан крупному и мелкому рогатому скоту.
Неингаляционный наркоз – наркотик вводится подкожно, внутримышечно, внутрибрюшинно, внутривенно, внутрь или ректально (морфин, хлоралгидрат, этиловый алкоголь).
По количеству используемых наркотиков различают:
Чистый наркоз – вводится один наркотик (применяется редко). Например, алкогольный наркоз жвачных животных. Вводят внутривенно 33%-ный этиловый спирт в изотоническом растворе NaCl с добавлением 5% глюкозы. Доза для крупного рогатого скота 120 – 140 мл на 100 кг массы, овцам - 7-10 мл/кг массы.
Смешанный наркоз – вводится смесь наркотиков (например, хлороформ - эфир в соотношение 1:2 свинье путем ингаляции).
Комбинированный наркоз – вводятся два или три наркотика последовательно, но разными путями. Например, морфин – хлоралгидратный наркоз лошади. Морфин в дозе 0,2 – 0,5 г вводят подкожно за 15 минут до внутривенного введения снотворной дозы хлоралгидрата.
Сочетанный наркоз – введение наркотика сочетают с местной анестезией.
Потенцированный наркоз – вводится наркотик после обработки животного нейролептиком, миорелаксантом или анальгетиком, которые усиливают действие наркотиков.
Местное обезболивание (анестезия) – это выключение болевой чувствительности на определенном участке тела животного при сохранении всех других функций организма. Для поверхностной анестезии конъюнктива, слизистая, серозная, синовиальные оболочки орошаются 5 – 10% растворами новокаина или лучше 0,5 – 1% растворами дикаина.
Для анестезии кожи распыляют на ее участок быстро испаряющейся и охлаждающейся жидкости – хлорэтила в количестве 10 – 20 мл.
Для инфильтрационной анестезии применяют 0,25 – 1% растворы новокаина. Путем инъекции ими пропитывают ткани по линии намечаемого разреза.
Для проводникового обезболивания (блокады) используют 2 – 3%-ные растворы новокаина, которые вводят в места прохождения нервных стволов вдали от места операции.
