
Неорганическая химия / Астахов М.В. Теория химической связи
.pdf1.потенциалу ионизации электрона с атомарной орбитали данного атома молекулы
2.энергии перехода электрона с заданной молекулярной орбитали на следующую молекулярную орбиталь
3.потенциальной энергии взаимодействия электрона с другими атомами молекулы
4.потенциалу ионизации электрона с заданной орбиты
5.кинетической энергии электрона на данной молекулярной орбитали
ТЕСТ 10
1. Исходя из теории молекулярных орбиталей какая из связей будет прочнее в случае атомов второго периода?
1.σ2s
2.σ2рz
3.π2рy
4.σ*2sσ
5.π2рy
2.Какая из молекул, состоящая из двух одинаковых атомов второго периода, будет более устойчивой?
1.Которая имеет большее число электронов на молекулярных орбиталях
2.У которой больше число валентных электронов
3.У которой больше электронов находится на связывающих молекулярных орбиталях
4.У которой больше электронов находится на разрыхляющих молекулярных орбита-
лях
5.У которой число электронов, находящихся на связывающих молекулярных орбиталях, равно число электронов, находящихся на разрыхляющих молекулярных орбиталях
3.Какие из энергий связи равны в молекуле, образованных двумя одинаковыми атома-
ми?
1.σ1s и σ*1s
2.σ2s и σ*2s
3.σ2рz и π2рy
4.π2рy и π2рх
5.π2рх и π*2рy
4.Какая из приведенных ниже электронных конфигураций обеспечивает наиболее прочную связь атомов в двухатомной молекуле?
1.КК(σs)2(σs*)2(πy)2(πх)2(σz)2
2.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)(π*х)
3.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)2(π*х)2(σ*z)2
4.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)
5.КК(σs)2(σs*)2(πy)2(πх)2(σz)2
141
5. Какая из приведенных ниже электронных конфигураций соответствует молекуле B2?
1.КК(σs)2(σs*)2(πy)(πх)( σ z)]
2.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)2(π*х)2
3.КК(σ2s)2
4.КК(σs)2(σs*)2
5.(σ1s)2 (σ*1s)
6.Исходя из электронных конфигураций молекул, определите, у какой из этих структур будет наиболее прочная связь между атомами.
1.КК(σs)2(σs*)2(πy)(πх)( σ z)
2.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)2(π*х)2(σ*z)2
3.КК(σs)2(σs*)2(πy)(πх)
4.КК(σs)2(σs*)2(πy)2(πх)2(σz)2
5.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)(π*х)
7.Какая из приведенных ниже электронных конфигураций молекул обеспечивает наименьшее расстояние между атомами в этой молекуле?
1.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)2(π*х)2(σ*z)2
2.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)2(π*х)2(σ*z)2
3.КК(σs)2(σs*)2(πy)(πх)( σ z)
4.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)(π*х)
5.КК(σs)2(σs*)2(πy)2(πх)2(σz)2
8.Какая из приведенных ниже электронных конфигураций не приведет к образованию двухатомной молекулы?
1.КК(σs)2(σs*)2(πy)(πх)
2.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)2(π*х)2(σ*z)2
3.КК(σs)2(σs*)2(πy)(πх)( σ z)
4.КК(σs)2(σs*)2(σz)2(πy)2(πх)2(π*y)(π*х)
5.КК(σs)2(σs*)2(πy)2(πх)2(σz)2
ТЕСТ 11
1. Какие интегралы в ММО называют кулоновскими интегралами?
1. ∫ψiHψidτ
2. ∫ψiHψjdτ
3. ∫ψi ψidτ
4. ∫ψiψjdτ
5. β
142
2. Какие интегралы в ММО называют резонансными интегралами?
1. ∫ψiHψidτ
2. ∫ψiHψjdτ
3. ∫ψi ψidτ
4. ∫ψiψjdτ
5. α
3. Какие интегралы в ММО называют интегралами перекрывания?
1. ∫ψiHψidτ
2. ∫ψiHψjdτ
3. ∫ψi ψidτ
4. ∫ψiψjdτ
5. β
4. Какой величине равны в ММО интегралы типа ∫ψiψjdτ?
1.1
2.0
3.2
4.бесконечности
5.α
5. Какой величине равны интегралы типа ∫ψiψidτв ММО?
1.1
2.0
3.2
4.бесконечности
5.α
6. |
Чему равна полная электронная энергия молекулы в методе ММО ЛКАО? |
1. |
Сумме энергий всех электронов, находящихся на молекулярных орбитальных. |
2. |
Сумме энергий всех электронов в молекуле. |
3. |
Сумме кинетической энергии электронов в молекуле |
4. |
Сумме потенциальной энергии электронов в молекуле |
5. |
Сумме энергии электронов в каждом атоме, образующих молекулу. |
7. |
Каким выражением описывается молекулярная орбиталь в методе МОХ |
1.Ψ=C1ψ1+C2ψ2+C3ψ3+…..+Chψh =ΣCrψr |
|
2. |
ψa(1)ψb(2)+ ψa(2)ψb(1)+ ψa(1)ψa(2) + ψb(1)ψb(2) |
143
3.ϕ1sa (1)ϕ1sb (2) +ϕ1sa (2)ϕ1sb (1)
4.φа φb
5.a1ΨI + a2 ΨII
8. Какое величине равен порядок σ-связи между атомами углерода в органической молекуле?
1.1
2.4,73
3.1,73
4.½
5.0
ТЕСТ 12
1. С помощью какого уравнения может быть рассчитан индекс свободной валентности атома?
1. Nmax-Σ Prs
j=m
2.∑n j c jr c js
j=1
3.1-qr
4. Σnjcjr2
5. -mβ
2. С помощью какого уравнения может быть рассчитан порядок связи между атомами в молекуле (Рrs) валентности атома?
1. Nmax-Nr
j=m
2.∑n j c jr c js
j=1
3.1-qr
4.Σnjcjr2
5.-mβ
3. С помощью какого уравнения может быть рассчитан избыточный заряд на атоме в молекуле (qr)?
1. Nmax-Nr
j=m
2.∑n j c jr c js
j=1
3.1-qr
4.Σnjcjr2
5.–mβ
144
4.Какая из приведенных ниже величин соответствует максимально возможному порядку π-связи атома углерода в органической молекуле?
1.4,73
2.2
3.1.
4.1,73
5.2,23
5. Какое из уравнений описывает связывающую молекулярную орбиталь в молекуле бутадиена?
1.Ψ = 0,6ϕ1 −0,37ϕ2 −0,37ϕ3 +0,6ϕ4
2.Ψ = 0,6ϕ1 +0,37ϕ2 −0,37ϕ3 −0,6ϕ4
3. |
Ψ = 0,372 ϕ1 |
+ 0,602 ϕ2 + 0,602 ϕ3 + 0,372 ϕ4 |
4. |
Ψ = 0,37ϕ1 −0,6ϕ2 + 0,6ϕ3 −0,37ϕ4 |
|
5. |
Ψ = −0,372 ϕ |
1 + 0,602 ϕ2 + 0,602 ϕ3 + 0,372 ϕ4 |
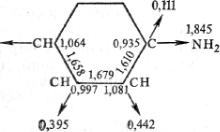
6. Какую характеристику атома в молекуле, молекулярная диаграмма которой приведена на рисунке, передает число 0,395?
Порядок связи индекс свободной валентности
избыточный заряд на атоме заряд на атоме энергию ионизации
Какая из приведенных ниже молекулярных орбиталей будет иметь наименьшую энер-
гию?
1.Ψ = 0,6ϕ1 −0,37ϕ2 −0,37ϕ3 +0,6ϕ4
2.Ψ = 0,6ϕ1 +0,37ϕ2 −0,37ϕ3 −0,6ϕ4
3. |
Ψ = −0,372 ϕ1 + 0,602 ϕ2 + 0,602 ϕ3 + 0,372 ϕ4 |
4. |
Ψ = 0,37ϕ1 −0,6ϕ2 + 0,6ϕ3 −0,37ϕ4 |
145
5. Ψ = 0,372 ϕ + 0,602 ϕ2 + 0,602 ϕ3 + 0,372 ϕ4
1
7.В результате расчета энергии молекулярных уровней были получены значения, приведенные ниже. Какое из этих значений будет соответствовать наименьшей энергии электронов в молекуле?
1.3α-2β
2.3α-β
3.3α+2β
4.3α+β
5.3α+1,47β
8.Какое из приведенных ниже значений характеризует наименьшую реакционную способность атома в молекуле?
1.F=0,3
2.F=0,45
3.F=0,67
4.F=0,5
5.F=0,9
ТЕСТ 13.
1. Какое уравнение описывает усредненную энергию ориентационного взаимодействия (Uор) одинаковых молекул?
1.U = −(2μ4 / 3r6 )kT
2.U = −(2μ12μ22 / 3r6 )kT
3.μ = αF.
4.U = −2αμ2 / r 6
5. |
U = −( |
3hν |
0 )× |
α2 |
= |
3 |
αI |
1 |
||
4 |
r |
6 |
4 |
r |
6 |
|||||
|
|
|
|
|
|
|
||||
2. Какое уравнение описывает энергию индукционного взаимодействия (Uинд) моле-
кул?
1.U = −(2μ4 / 3r 6 )kT
2.U = −(2μ12μ22 / 3r6 )kT
3.μ = αF.
4.U = −2αμ2 / r6
5. U = −( |
3hν |
0 |
) × |
α2 |
= |
3 |
αI |
1 |
4 |
|
r 6 |
4 |
r 6 |
||||
|
|
|
|
|
146

3. Какое уравнение описывает энергию дисперсионного взаимодействия (Uдис) одинаковых молекул?
1.−(2μ4 / 3r 6 )kT
2.−(2μ12 μ22 / 3r 6 )kT
3.−(3h2ν0 ) × Iα1 1+αI22 I1 I2 r16
4.− 2αμ2 / r 6
5. −( |
3hν |
0 |
) × |
α2 |
= |
3 |
αI |
1 |
4 |
|
r 6 |
4 |
r 6 |
||||
|
|
|
|
|
4. Какое уравнение описывает энергию дисперсионного взаимодействия (Uдис) двух разных молекул?
1.−(2μ4 / 3r 6 )kT
2.−(2μ12 μ22 / 3r 6 )kT
3.−(3h2ν0 ) × Iα1 1+αI22 I1I2 r16
4.− 2αμ2 / r 6
5.− 34 α 2 I r16
5.Какая энергия межмолекулярного взаимодействия зависит от температуры?
1.дисперсионная
2.ориентационная
3.индукционная
4.никакая
5.энергия отталкивания
6.Какое аналитическое выражение описывает потенциальную кривую межмолекулярного взаимодействия?
1.−(2μ4 / 3r6 )kT
2.−(2μ12μ22 / 3r6 )kT
3.−(3h2ν0 ) × Iα1 1+αI22 I1I2 r16
147

4. |
− 2αμ2 / r 6 |
|
|
|
|
|
|||
5. |
−( |
2 |
μ4 |
+ 2αμ2 |
+ |
3α |
2 |
I )r −6 |
+ Aexp{−r / ρ} |
3 |
kT |
4 |
|
||||||
|
|
|
|
|
|
|
|||
7.Значение энергии межмолекулярного взаимодействия имеет порядок?
1.1-10 дж/моль
2.несколько кДж/моль 3.десятки кДж/моль 4.сотни кДж/моль 5.дж/моль
8.Какое из уравнений описывает взаимодействие при сближении двух одинаковых неполярных молекул ?
|
U = −( |
3hν |
0 |
|
) × |
|
α α |
|
|
I1I2 |
1 |
||||||||
1. |
|
|
|
|
|
1 2 |
|
|
|
|
|
||||||||
2 |
|
|
|
|
I1 |
+ I2 |
|
|
s |
6 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
2. |
U = −( |
3hν |
0 |
) × |
α2 |
= |
3 |
αI |
1 |
|
|
|
|||||||
|
4 |
|
|
|
s6 |
4 |
s |
6 |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
3.U = −(3h2ν0 ) ×I1I2 s16
4.U = Iα1 1+αI22 I1 I2 s16
5. |
Uдис = −( |
3hν0 |
) × |
α1α2 |
|
I1 I2 |
|
2 |
I1 + I |
2 |
|||||
|
|
|
|
Тест 14
1. Какое аналитическое выражение, описывающее потенциальную кривую межмолекулярного взаимодействия, называют формулой Леннард-Джонса?
1.−(2μ4 / 3r 6 )kT
2.−(2μ12 μ22 / 3r 6 )kT
3.−(3h2ν0 ) × Iα1 1+αI22 I1 I2 r16
148

4. |
|
σ |
12 |
−( |
σ |
6 |
|
|
|
||
4ε ( |
r |
) |
|
r |
) |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
5. |
−(2 |
μ4 |
|
+ 2αμ |
2 + |
3α2 |
I )r−6 + A |
||||
|
4 |
||||||||||
|
3 kT |
|
|
|
|
|
|||||
2. Какое аналитическое выражение описывает энергию взаимодействия между ионом и неполярной молекулой в растворе?
1. −(2μ4 / 3s6 )kT
2. −(2μ |
2 |
μ2 / 3s6 )kT |
|||||||||
|
|
|
|
|
1 |
|
2 |
|
|
|
|
3. |
− |
α e2 |
− |
c |
|
|
|||||
|
2s4 |
|
s6 |
|
|||||||
|
|
|
|
|
|
|
|||||
4. |
−(eμ |
+ |
αe2 |
) |
|||||||
|
|
|
s2 |
|
|
2s4 |
|
||||
5. |
− |
|
3 |
α |
2 I |
1 |
|
|
|
||
4 |
s6 |
|
|||||||||
|
|
|
|
|
|
||||||
3.Какая из перечисленных ниже связей будет наиболее слабой? 1.-σ 2.-π
3.-ионная
4.-водородная связь
5.-Ван-дер Ваальса
4. Какое из уравнений, приведенных ниже, описывает взаимодействие между ионом и неполярной молекулой в растворе?
1. −(eμ +αe2 )
s2 2s4
2.−α2se42 − sc6
3.−(2μ4 / 3s6 )kT
4.− 34α2 I s16
5.− 2αs4 − sc6
5. Какую из величин, входящую в уравнение Леннард-Джонса , называют диаметром «столкновения»
1. ε
149
2.s
3.σ
4.4ε
5.s12
6.Какая из величин, входящая в уравнение Леннард-Джонса, соответствует максимальной энергии взаимодействия между молекулами?
1.ε
2.s
3.σ
4.4ε
5.s12
7. Какие из молекул будут взаимодействовать между собой только за счет дисперсионных сил?
1.H2O
2.NO
3.N2
4.H2S
5.SO2
8. Для какие молекул возможно ориентационное взаимодействие?
1.СН4
2.С2Н6
3.N2
4.H2S
5.S8
Тест 15
1 При образовании водородной связи какое координационное число приписывают атому водорода?
1.2
2.1
3.0
4.1,5
4.3
2.Какое из предположений о характере водородной связи считается наиболее вероят-
ными?
1.атом водорода может быть двухвалентным
2.возникновение резонансных структур
3.диполь-дипольное взаимодействие молекул
150
