
ФОТП 2013
.pdf
По определению дифференциал (бесконечно малого приращения) функции двух переменных можем записать:
du(υ,T ) |
u |
|
|
dυ |
u |
|
|
dT , |
(10.11) |
|
|
|
|||||||
υ |
|
|
T |
||||||
|
|
T |
|
|
|
υ |
|
||
|
|
|
|
|
где υ и Т – параметры состояния – удельный объём и абсолютная температура соответственно, м3/кг, К; u (υ, Т) – удельная внутренняя энергия
идеального газа, как функция переменных υ и Т, Дж/кг; |
u |
|
|
и |
u |
|
|
– част- |
|
|
|
||||||
υ |
|
|
T |
|||||
|
|
T |
|
|
|
υ |
||
|
|
|
|
ные производные от внутренней энергии: по удельному объёму, при постоянной температуре, и по температуре, при постоянном удельном объёме, соответственно, Дж/м3, Дж/(кг · К), dυ и dT – дифференциалы удельного объёма и температуры соответственно, м3/кг, К.
Экспериментально установлено, что внутренняя энергия идеальных газов не зависит от их удельного объёма υ. Это означает, что первое слагаемое в (10.11) равно нулю, как производная, взятая от константы. Следовательно, из (10.11) получаем:
du(T ) |
du |
|
dT . |
(10.12) |
|
||||
|
dT |
|
υ |
|
|
|
|
Величина dTdu υхарактеризует изменение внутренней энергии идеаль-
ного газа в процессе при постоянном удельном объёме υ = const. Для такого процесса dυ = 0 (как дифференциал от константы). Соответственно первый закон термодинамики для такого процесса при постоянном υ принимает вид:
du |
|
υ dq |
|
υ pdυ dq |
|
υ. |
(10.13) |
|
|
|
|||||
|
|
|
|
С другой стороны, по определению (10.10) истинной удельной теплоёмкости при постоянном объёме сυ имеем:
dq |
|
υ cυ dT |
|
υ. |
(10.14) |
|
|
||||
|
|
|
Сравнивая (10.13) и (10.14) получаем:
31
du |
|
υ cυ dT |
|
υ , или |
du |
|
cυ. |
(10.15) |
|
|
|
||||||
|
|
|||||||
|
|
|
|
|
dT |
|
υ |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
Подставляя (10.15) в (10.12) получаем формулу для вычисления изменения внутренней энергии идеального газа при любых процессах, когда, в общем случае, одновременно могут меняться и давление, и удельный объём:
du cυ dT . |
(10.16) |
Изменение удельной внутренней энергии идеального газа в некотором процессе 1 – 2 определяется путём интегрирования (10.16) в соответствующих пределах:
|
T2 |
|
u2 u1 |
cυ dT , |
(10.17) |
|
T1 |
|
где Т1 и Т2 – начальная и конечная температуры идеального газа соответственно, К.
Формула (10.17) показывает, что рассчитать изменение внутренней энергии идеального газа в любом процессе можно по известной истинной удельной теплоёмкости этого газа при постоянном объёме.
2) У идеальных газов удельные теплоёмкости связаны меду собой соотношением:
ср – сυ = R, |
(10.18) |
где ср и сυ – удельные теплоёмкости при постоянном давлении и при постоянном объёме соответственно (это могут быть либо истинные, либо средние теплоёмкости), Дж/(кг · К); R – газовая постоянная данного идеального газа, Дж/(кг · К).
Докажем справедливость (10.18) опираясь на первый закон термодинамики и свойство идеальных газов (10.16):
dq = du + p dυ = cυ dT + p dυ. |
(10.19) |
По правилам вычисления дифференциала от произведения имеем:
d (p υ) = p · dυ + υ ·dp. |
(10.20) |
32
Выражаем из (10.20) p dυ и подставляем в (10.19), учитывая, что
p υ = R T: |
|
dq = cυ dT + d (R · T) – υ dp = (cυ + R) dT – cυ dp. |
(10.21) |
Выражение (10.21) справедливо для любых процессов.
Далее будем рассматривать только процессы при постоянном давлении р = const, а значит dp = 0. Для такого процесса (10.21) принимает вид:
dq = (cυ + R) dT. |
(10.22) |
С другой стороны, для такого процесса из определения ср – истинной удельной теплоёмкости при постоянном давлении (10.8) следует:
dq = cр · dT. |
(10.23) |
После сравнения (10.22) и (10.23) получаем:
cр = cυ + R или cр – cυ = R. |
(10.24) |
Выражение (10.24) впервые было получено немецким врачом Майером в 1824 году и называется соотношением Майера. Из него следует, что газовая постоянная некоторого идеального газа (например, азота) равна разности между его удельными теплоёмкостями при постоянном давлении и при постоянном объёме.
10.2. Теплоёмкость твёрдых и жидких тел
Для веществ, находящихся в твёрдом или жидком состояниях, также как и для газов вводятся понятия удельных теплоёмкостей при постоянном давлении и постоянном объёме:
c pm |
|
|
q p |
, |
(10.25) |
|||||
|
T2 |
|
T1 |
|||||||
|
|
|
|
|
|
|
||||
c p |
dq p |
|
, |
|
|
(10.26) |
||||
|
dT |
|
|
|
||||||
|
|
|
|
|
|
|
|
|||
c |
|
qυ |
, |
(10.27) |
||||||
|
||||||||||
υm |
|
|
T2 |
T1 |
|
|
||||
|
|
|
|
|
||||||
33
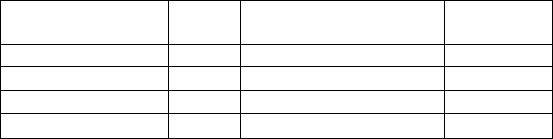
c |
|
dqυ |
. |
(10.28) |
|
||||
υ |
|
dT |
|
|
Особенностью жидких и твёрдых тел является то, что в расчётах их можно рассматривать практически несжимаемыми. При любом давлении объём тела остаётся практически неизменны. Следовательно, отличие сυ и ср, при их экспериментальном определении, весьма незначительны, и в большинстве инженерных расчётов этим отличием можно пренебречь.
Для всех технически важных твёрдых и жидких веществ в справочной литературе приводится универсальная формула типа (10.6) для истинной удельной теплоёмкости при постоянном давлении:
ср(Т) = a + b · T + c · T –2, Дж/(кг · К), |
(10.29) |
где a, b и c – известные константы для каждого вещества.
Также для многих веществ приводятся таблицы для средних теплоёмкостей сpm.
Примечание:
При очень низких температурах теплоёмкость многих веществ рассчитывается по эмпирическому уравнению Дебая [5]:
μc 1837,2 (T )3 , |
(10.30) |
υ θ
где μсυ – удельная мольная теплоёмкость при постоянном объёме, кДж/(кмоль · К); θ – температура Дебая, К.
Значения θ для некоторых веществ приводится в табл. 10.1.
Таблица 10.1
Значения температуры Дебая для некоторых веществ
Вещество |
θ, К |
Вещество |
θ, К |
Свинец |
88 |
Медь |
315 |
Калий |
100 |
Алюминий |
390 |
Золото |
170 |
Железо |
420 |
Серебро |
215 |
Алмаз |
1860 |
34
11. Открытие энтропии
Примерно в 1860 году немецкий физик Клазиус, изучая тепловые процессы впервые пришёл к следующему выводу. У каждой термодинамической системы существует такая функция состояния, которая в ходе равновесного процесса изменяется только тогда, когда энергия к системе подводится или отводится в форме теплоты. Причём это изменение происходит таким образом, что, всегда выполняется равенство:
dQ = T · dS, |
(11.1) |
где dQ – дифференциал (бесконечно малое приращение) теплоты, котоая подводится к системе, Дж; Т – текущая температура системы, К; dS – дифференциал открытой Клазиусом новой функции состояния термодинамической системы, Дж/К.
Функцию S назвали э н т р о п и′ я. Термин греческого происхожде-
ния, который означает поворот, превращение, поворачиваюсь внутрь, способность к превращению.
Запишем (11.1) в более удобной форме для удельных величин. Для этого поделим обе части (11.1) на массу системы М, кг:
dq = T · ds, |
|
|
или |
|
|
ds dq |
, |
(11.2) |
T |
|
|
где q – удельная теплота процесса, Дж/кг; s – функция состояния - удельная энтропия, Дж/(кг · К).
Так как энтропия является функцией состояния, то это означает, что она является непрерывной функцией каких-то двух из трёх (р, υ, Т) параметров состояния. То есть её значение однозначно определено, например, в каждой точке рυ-плоскости. Следовательно, разность энтропий в двух разных точках определяется только положением этих точек на рυ-плоскости и не зависит от вида уравнения процесса перехода из одной точки в другую.
Докажем это, исходя из первого закона термодинамики в дифференциальном виде (10.11). Как уже отмечалось, выражение (10.11) описывает равновесные процессы, протекающие в любых термодинамических системах: в системах, находящихся в состоянии идеального газа; в системах, находящихся в состоянии реальных газов; в системах, находящихся в жидкой или твёрдой фазах. Запишем (9.11) в виде:
35
dq = du + p · dυ, |
(11.3) |
где q – удельная теплота процесса, Дж/кг; u – удельная внутренняя энергия системы, Дж/кг; p – давление внутри системы, Па; υ- удельный объём системы, м3/кг.
Вначале рассмотрим доказательство справедливости утверждения (11.2) для случая, когда систему можно рассматривать как идеальный газ, то есть когда уравнение состояния системы имеет вид (см. раздел 2):
|
|
p υ = R T. |
|
|
(11.4) |
||||
Из (11.4) получаем: |
|
|
|
|
|
|
|
|
|
|
|
p |
RT . |
|
|
|
(11.5) |
||
|
|
|
υ |
|
|
|
|
||
Обе части (11.3) делим на Т: |
|
|
|
|
|
|
|
|
|
|
|
dq du |
|
pdυ |
. |
(11.6) |
|||
|
|
T |
|||||||
|
|
T |
|
T |
|
|
|
||
Подставляем в правую часть (11.6) формулы для идеального газа |
|||||||||
(11.5) и (10.16) получаем: |
|
|
|
|
|
|
|
|
|
dq |
|
cυ dT |
|
|
R dυ |
. |
(11.7) |
||
T |
T |
|
|
|
υ |
||||
|
|
|
|
|
|
|
|||
Для наглядности будем считать сυ постоянной величиной.
Введём в рассмотрение новую непрерывную функцию двух параметров состояния s следующего вида:
s = сυ ln T + R ln υ + const. |
(11.8) |
|||||
Очевидно, что: |
dT |
|
dυ |
|
|
|
ds cυ |
R |
. |
(11.9) |
|||
T |
|
|||||
|
|
υ |
|
|||
Сравнивая (11.9) и (11.7) получаем:
36
dq |
ds или dq = T·ds, |
(11.10) |
T |
|
|
где s – некоторая новая функция состояния системы – непрерывная функция двух параметров состояния (11.8), Дж/(кг · К).
Полученное из первого закона термодинамики выражение (11.10) является доказательством справедливости утверждения (11.2) для идеальных газов. Справедливость утверждения (11.2) для других термодинамических систем (реальных газов, жидких и твёрдых тел) приводится в Приложении 6.
Таким образом, выражение (11.2) можно рассматривать как определение удельной энтропии термодинамической системы.
Для всех технически значимых веществ значения удельной энтропии определены на базе экспериментальных данных. Эти значения приводятся в справочной литературе в виде таблиц, например, в виде зависимости удельной энтропии от давления и температуры s = s (p, T).
Пример:
Рассмотрим, как можно экспериментальным методом (на основе экспериментальных данных) определить изменение удельной энтропии газа. Экспериментальные данные – это его удельная теплоёмкость при постоянном давлении ср. Для наглядности будем считать ср известной постоянной величиной.
Будем рассматривать некий процесс 1 – 2 при р = const, в котором к газу подводится теплота q.
По определению удельной теплоёмкости для такого процесса можем записать:
dq = ср dT. |
(11.11) |
С другой стороны, по определению удельной энтропии имеем:
dq = T·ds. |
|
(11.12) |
Сравнивая (11.12) и (11 11) получаем: |
|
|
ср dT = T·ds или ds c p |
dT . |
(11.13) |
|
T |
|
После интегрирования (11.13) в пределах процесса 1 – 2 получаем:
37
2 |
T2 |
dT |
T2 |
|
|
|
ds s2 |
s1 c p |
T |
c p ln( |
|
) . |
(11.14) |
T |
||||||
1 |
T1 |
|
1 |
|
|
|
На базе таких экспериментальных данных могут быть построены таблицы для энтропии, как функции температуры и давления.
Примечание:
1) Воспользовавшись определением удельной энтропии (11.2) запишем первый закон термодинамики в виде:
du = dq – dl = T ds – p dυ. |
(11.15) |
Из (11.15) видно, что s – величина, сопряженная с Т, подобно тому как υ – величина, сопряжённая с р. То есть s и υ являются экстенсивными величинами, а р и Т – интенсивными. Экстенсивные величины изменяются под воздействием соответствующих интенсивных величин.
2) По определению удельной энтропии (11.2) можем записать:
ds dq . |
(11.16) |
T |
|
Это означает, что если в элементарном равновесном процессе к 1 кг некоторого вещества подводится энергия в виде теплоты в количестве dq при температуре Т, то это обязательно приведёт к изменению энтропии вещества на ds dqT .
При этом следует отметить, что если в равновесном процессе такое же количество энергии будет подведено к веществу не в виде теплоты dq, а в виде работы dl, то энтропия системы не изменится ds = 0.
12. Второй закон термодинамики
Второй закон термодинамики, как и первый, установлен экспериментально.
В теоретических работах приводятся различные формулировки второго закона, которые, по сути, являются обобщенными интерпретациями наблюдаемых в природе явлений.
При этом сами формулировки являются эквивалентными: исходя из какой-то одной можно доказать справедливость других.
38
Второй закон относится к неравновесным (необратимым) термодинамическим процессам – устанавливает признаки, отличающие их от равновесных (обратимые) процессов.
Второй закон термодинамики может быть сформулирован следующим образом:
изменение удельной энтропии термодинамической системы в неравновесном (необратимом) процессе sн всегда больше изменения энтропии в аналогичном равновесном процессе:
sн > sр. |
(12.1) |
Это означает, в частности, следующее. Если в некотором равновесном (необратимом) процессе термодинамическая система благодаря подводу теплоты в количестве q переходит из начального состояния 1 в конечное состояние 2, и её удельная энтропия при этом меняется от s1 до s2, то это изменение, в соответствии с результатом интегрирования (11.2), будет определяться соотношением:
|
2 dq |
|
|
sp s2 s1 |
1 T |
, |
(12.2) |
где sp − изменение удельной энтропии в результате равновесного процес-
са 1 − 2, Дж/(кг · К).
Если же переход термодинамической системы из того же начального состояния 1 произойдёт при той же подведенной теплоте, в неравновесном (необратимом) процессе в другое конечное состояния 2′, то, согласно
принципу возрастания энтропии (12.1), будет справедливо неравенство:
s |
í |
s |
s |
> |
s |
2 |
s |
(12.3) |
|
или, с учётом (12.2): |
2 |
1 |
|
|
1 |
|
|||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
dq |
|
|
|
|
|
|
s н |
> |
|
|
, |
|
|
|
(12.4) |
|
|
T |
|
|
|
|||||
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
где sн – изменение удельной энтропии в результате неравновесного (необратимого) процесса 1 – 2′, Дж/(кг · К); s2 – значение удельной энтропии
системы в конце неравновесного процесса 1 − 2′ подвода теплоты q (оно определяется после того, как система пришла в новое равновесное состояние 2′ через какое-то время после окончания неравновесного процесса), Дж/(кг · К).
39

Из принципа возрастания энтропии также вытекает следующее. Если в некотором равновесном процессе 1 − 2 к системе из окружающей среды подводится удельная работа в количестве l, Дж/кг, (энергия в форме работы), то, как было отмечено выше, ее энтропия не изменяется, т.е.:
sр = s2 – s1 = 0. |
(12.5) |
Если такое же количество энергии в виде работы подводится из окружающей среды к системе в некотором неравновесном (необратимом) процессе 1 − 2′, который начинается из того же начального состояние системы 1, то её энтропия, в соответствии с (12.1), обязательно возрастёт, т. е. будет
справедливо неравенство: s2 |
s1 sн > |
sр , или, с учетом (12.5): |
|
sн > 0, |
(12.6) |
где s2 – значение удельной энтропии в конце неравновесного (необрати-
мого) процесса 1 − 2′ подведения того же количества удельной работы l, Дж/кг, (оно определяется после того, как система пришла в новое состояние равновесия 2′ через какое-то время после завершения неравновесного процесса), Дж/(кг · К).
Данное возрастание энтропии объясняется тем, что в неравновесном (необратимом) процессе часть переданной из внешней среды работы обязательно самопроизвольно превращается в теплоту (например, благодаря наличию сил трения в реальных системах). То есть, в результате такого неравновесного процесса часть энергии, поступившей к системе из внешней среды, обязательно поступит к ней в форме теплоты, что обязательно приведет к росту ее энтропии (последнее следует из самого определения энтропии).
Очевидно, что для принципа возрастания энтропии варианты, когда теплота и работа отводятся от термодинамической системы в некоторых неравновесных процессах, могут быть рассмотрены аналогичным образом.
Если аналитически обобщить оба принципа существования (11.2) и возрастания (12.1) энтропии в форме одного соотношения, то можно записать:
2 dq |
, |
(12.7) |
|
s |
T |
||
1 |
|
|
|
|
|
|
|
где s – конечное изменение удельной энтропии системы в любом (равновесном или неравновесном) процессе в результате подвода или отвода удельных теплоты q и работы l, Дж/(кг · К); dq дифференциал (бесконеч-
40
