
- •Вопрос 1.8
- •Задача 1.19
- •Вопрос 1.19
- •Задача 1.26
- •Вопрос 1.26
- •Задача 2.8
- •Вопрос 2.8
- •Задача 2.19
- •Вопрос 2.19
- •Задача 2.26
- •Вопрос 2.26
- •Задача 3.8
- •Вопрос 3.8.
- •Задача 3.19
- •Вопрос 3.19
- •Задача 3.26
- •Вопрос 3.26
- •Вопрос 4.8
- •Задача 4.19
- •Вопрос 4.20
- •Вопрос 4.26
- •Вопрос 4.31
- •Задача 5.8
- •Вопрос 5.8
- •Задача 5.19
- •Вопрос 5.19
- •Вопрос 5.26
- •Вопрос 5.31
- •Задача 6.8.
- •Вопрос 6.8.
- •Вопрос 6.9
- •Задача 6.26
- •Вопрос 6.26
- •Список использованной литературы
Вопрос 6.9
Изобразите схему абсорбционной холодильной установки и опишите её работу. Как повышается давление холодильного агента в этой установке?
Ответ
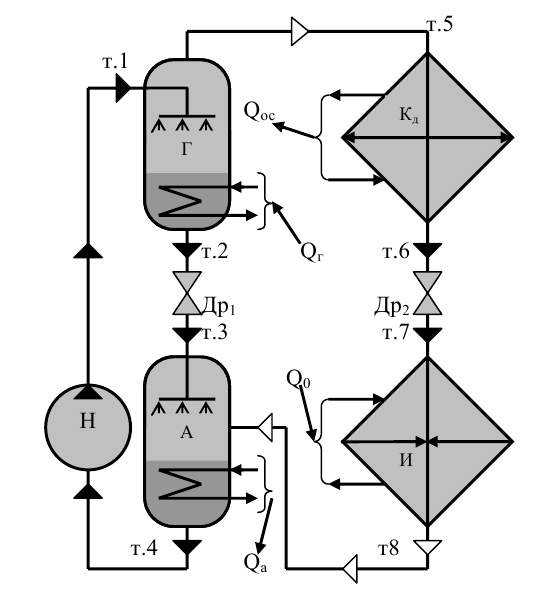
Рис. 38
Принципиальная схема простейшей абсорбционной машины приведена на Рис. 38.В кипятильнике или генераторе (Г) происходит кипение раствора хладоагента за счет подвода теплоты Qг от внешнего источника. Процесс кипения происходит при постоянном давлении, концентрация хладоагента в паре будет значительно выше концентрации его в растворе. Непрерывное удаление этого пара из генератора приводит к обеднению раствора в нем. Таким образом, из генератора выходят слабый раствор и крепкий пар. Первый поступает в дроссель и, в конечном итоге, абсорбер, второй -непосредственно в конденсатор.
За счет отвода теплоты фазового перехода Qoc в окружающую среду происходит конденсация паров в конденсаторе (Кд). При этом, в результате полной конденсации образуется крепкий раствор. Таким образом, из конденсатора выходит жидкий раствор более крепкий, чем тот, что кипит в генераторе. Далее, этот очень крепкий раствор хладоагента дросселируется в дросселе (Др2) до давления в испарителе (И), которое обеспечивает требуемую температуру кипения и, следовательно, отвода теплоты Q0 от объекта охлаждения.
Из испарителя холодный, но крепкий пар поступает в абсорбер (А), где абсорбируется горячим, но слабым раствором. Для обеспечения работы абсорбера от него отводится теплота Qa. Слабый раствор в абсорбер поступает из генератора. Для понижения давления раствора от давления в генераторе до давления в абсорбере между ними установлен дроссель (Др1). Из абсорбера раствор, обогащенный в результате абсорбции крепких паров, насосом подается в генератор, на чем замыкается цикл абсорбционной холодильной машины.
Задача 6.26
Холодопроизводительность парокомпрессионной холодильной установки с редукционным вентилем, работающей на углекислоте, составляет 200 кДж/с. Установка работает в интервале температур t1=-100C до t2=150C, пар углекислоты выходит из компрессора сухим насыщенным. Рассчитать идеальный цикл установки, определив удельную холодопроизводительность углекислоты, холодильный коэффициент, а так же расход хладоагрегата и теоретическую мощность компрессора.
Решение
Изобразим схему и диаграмму цикла ( Рис. 39,Рис. 40)
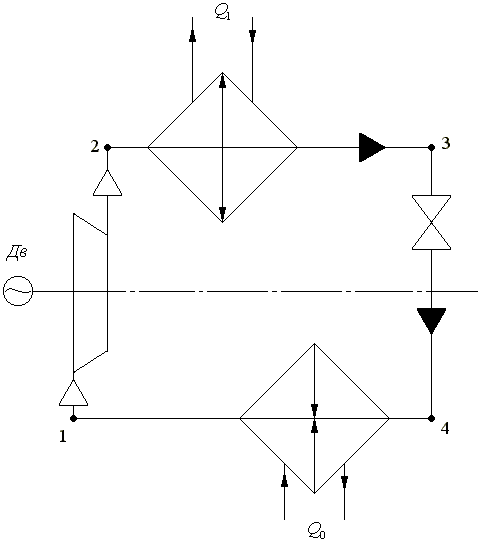
Рис. 39
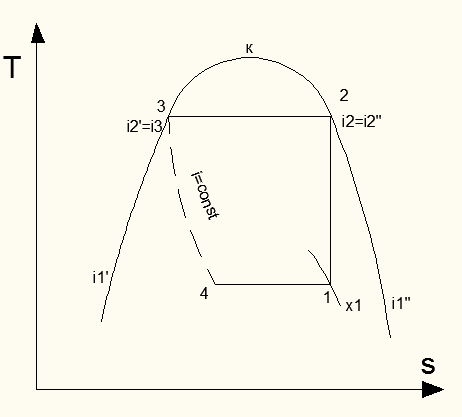
Рис. 40
По таблице «Насыщенный пар углекислоты» найдём значения энтальпии и энтропии характерных точек:
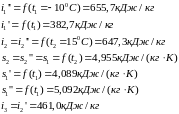
Зная значение энтропии в т.1 и в точках можем найти степень сухости углекислоты перед компрессором.
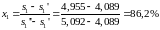
Теперь, зная в т.1 степень сухости, можем найти энтальпию.
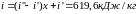
Так как процесс дросселирования считаем изоэнтальпным, то
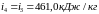
Зная энтальпии характерных точек, можем найти удельную хладопроизводительность, удельную работу цикла

Определим холодильный коэффициент:
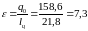
Зная связь между удельной хладопроизводительностью и хладопроизводительностью можем найти расход хладагента
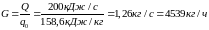
Определим мощность компрессора:
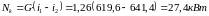
Ответ:
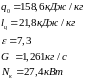
Вопрос 6.26
Сформулируйте закон Кирхгофа и поясните, какими причинами обусловлено изменение теплового эффекта химической реакции с имением температуры, при которой она протекает. Как вычисляется разница между тепловыми эффектами химической реакции при разных температурах для систем, компоненты которых находятся в идеально-газовом состоянии?
Ответ
В общем случае тепловой эффект химической реакции зависит от температуры и давления, при которых проводится реакция. Влиянием давления на тепловой эффект химической реакции обычно пренебрегают; влияние температуры на величину теплового эффекта описывается формулой Кирхгофа. Имея в виду в первую очередь зависимость H = f(T), рассмотрим изменение энтальпии в ходе некоторой реакции
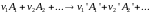 (187)
(187)
Каждому из участников реакции присуще определённое мольное значение энтальпии Hi, суммирующееся из мольной внутренней энергии Ui и произведения давления на молярный объём PVi. Тогда тепловой эффект реакции можно представить в виде алгебраической суммы:
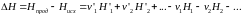 (188)
(188)
Для нахождения зависимости H = f(T) продифференцируем уравнение (188) по температуре при постоянном давлении:
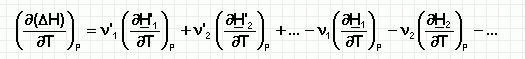 (189)
(189)
Производная мольной энтальпии вещества по температуре при P = const представляет собой мольную теплоёмкость этого вещества при постоянном давлении:
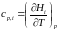 (190)
(190)
Поэтому
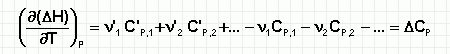 (191)
(191)
Температурный коэффициент теплового эффекта химической реакции равен изменению теплоемкости системы в ходе реакции.
Разделив переменные в уравнении (191) и проинтегрировав его, получаем:
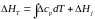 (192)
(192)
Здесь ΔHJ – постоянная интегрирования. При определённом интегрировании от Т1 до Т2 получим:
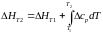 (193)
(193)
Если считать ΔСP не зависящим от температуры, уравнение (193)преобразуется к виду:
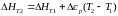 (194)
(194)
Поскольку обычно известны табличные значения стандартных тепловых эффектов ΔН°298, преобразуем выражение(194):
 (195)
(195)
