
- •Методичні вказівки
- •«Охорона повітря від забруднення та його нормування в газовому середовищі»
- •Охрана воздуха
- •Окислительная деградация и детоксикація атмосферных загрязнителей растениями
- •Методичні вказівки
- •«Поширення хімічних елементів та їх сполук в біосфері. Кларки основних хімічних елементів земної кори»
- •Методичні вказівки
- •«Комплексометричне визначення кальцію і магнію в рослинах»
- •Методичні вказівки
- •«Визначення марганцю в рослинах (за методом а.А. Власюка і л.Д. Лейденської)»
- •Методичні вказівки
- •«Визначення міді в рослинах»
- •Методичні вказівки
- •«Визначення бору в рослинах ( за методом х. М. Починка)»
- •Концентрація в, мкг/мг
- •Методичні вказівки
- •«Прискорене визначення азоту, фосфору і калію з однієї наважки (за методом к. Гінзбург та ін. )»
- •Методичні вказівки
- •«Визначення небілкового і білкового азоту в одній наважці методом хлораміну ( за методом х.М. Починка)»
- •Методичні вказівки
- •«Міграція хімічних елементів в організмі людини, тваринних та рослинних організмах»
Методичні вказівки
До виконання лабораторної роботи з курсу «Біогеохімія»
Для студентів спеціальності 7.070801
«Екологія та охорона навколишнього середовища»
Лабораторна робота № 8
«Визначення небілкового і білкового азоту в одній наважці методом хлораміну ( за методом х.М. Починка)»
Мета лабораторної роботи: Експериментальним шляхом дослідити вміст небілкового і білкового азоту в рослинних об’єктах (зразках)
Затверджено на засіданні
кафедри
прикладної екології
протокол
№_2__від _11.10___2010 р.
Кривий Ріг
2010
Обладнання, об'єкти, реактиви: аналітичні терези і різноважки; водяна баня; центрифуги ЦУМ-1 або ЦЛН-2; ступки; колби К'єльдаля; мірні циліндри місткістю 100 мл; бюретки; центрифужні пробірки; піпетки місткістю 10 мл; скляні палички, досліджувані рослини з вегетаційних дослідів або з навчально-дослідних ділянок, реактиви.
Розчин хлораміну (0,12 н.). 15 г хлораміну Т або 16 г хлораміну Б розчиняють у дистильованій воді, старанно збовтують, доводять до об'єму 1л І фільтрують крізь вату. Реактив зберігають у темній склянці з притертим корком.
Бвзаміачна дистильована вода. До 20 мл дистильованої води в пробірці додають одну краплю реактиву Неслера, жовте забарвлення свідчить про наявність аміаку в воді. Щоб видалити аміак, воду кип'ятять у колбі доти, поки не зникне жовте забарвлення.
Розчин молібдату натрію (10% -й). 10 г На2Мо04 розчиняють в 100 мл дистильованої води, додають 0,5 мл. 2 н. ЫаОН, нагрівають суміш до кипіння і кип'ятять 15 хв. Після цього розчин охолоджують, доводять безаміачною водою до 100 мл і зберігають у посудині з притертим корком. Розчин сульфату міді (3% -й). 30-г 8045Н20 розчиняють у безаміачній воді, доводять до 1 л і зберігають у добре критій склянці.
Розчин тіосульфату натрію (0,02 н.). Титрований 0.4, розчин Ыа282055Н20 розбавляють дистильованою водою в 5 разів. Для виготовлення 0,1 н. розчину 25 г титрованого тіосульфату натрію розчиняють у 0,5 л дистильованої води, в якій перед цим розчинено 0,2 г Ка2С03 старанно перемішують і доводять до 1 л. Визначають нормальність виготовленого розчину за біхроматом калію. Для цього до 2,5 мл 0,1 н, розчину біхромату калію додають 5 мл 20 %-го розчину, 10 мл Н2804 і титрують тіосульфатом натрію приналежності їмл 0,5%-го розчину крохмалю. Нормальність тіосульфату натрію обчислюють за такою формулою:

де К — нормальність титрованого розчину,
а — об'єм тіосульфату, який пішов на титрування 25 мл К2Сг207, мл. Розчин щавлевої кислоти (8%-й). 80 г Ыа282С>42Н20 розчиняють у колбі з гарячою дистильованою водою і доводять до об'єму 1л.
Розчин їдкого натру (2 н.). 80 г №ОН розчиняють віл дистильованої води, нагрівають до кипіння і кип'ятять ЗО хв. Охолоджений розчин доводять до 1 л безаміалною дистильованою водою і зберігають у добре закритій склянці. Безаміачний розчин сульфату калію. 200 г сульфату галію х. ч. висипають у склянку, додають 1 л дистильованої води і 5 мл розчину №ОН. Суміш нагрівають до кипіння і кип'ятять доти, поки розчин не помутніє (випала сіль). Розчин переносять у фарфорову чашку і випаровують приблизно до об'єму 100 мл, охолоджують і прозорий розчин зливають, а залишок висушують на повітряній бані (весь час помішуючи). Суху сіль зберігають у склянці з; натертим корком.
Фосфатний буферний розчин з бромідом калію (рН-6,7). 2,8 г висушеної при І00°С.солі КН2Р04 і 100 г КВг, обидві солі розчиняють разом у безаміачній воді, додають 80 мл 2 н. розчину №ОН, доводять безаміачною водою до 1 л, перемішують і зберігають у добре закритій склянці. Основні відомості. Азот входить до складу найважливіших сполук рослинного організму: білків, нуклеїнових кислот, амінокислот, хлорофілу, алкалоїдів, глюкозидів та ін. Вміст азоту в рослинних білках коливається в середньому від 12 до 20 %. Вважають, що вся рослинність земної кулі містить понад 1,1 * 109 т азоту. Азот є основним елементом живлення рослин. Низька врожайність багатьох сільськогосподарських культур найчастіше зумовлюється нестачею саме азоту. Тому вивчення й застосування методів визначення азоту і його сполук у рослинах має велике значення. Розрізняють небілковий і білковий азот. До небілкового азоту входить азот розчинених у воді речовин: амінокислот, амідів, азотистих органічних основ і аміаку. Щоб оцінити врожайність сільськогосподарських культур і поживну цінність кормів, визначають вміст білкового азоту.
Проведення роботи. На аналітичних терезах зважують 0,25—0,5 г повітряно-сухого або 1—2 г сирого досліджуваного рослинного матеріалу, кладуть у фарфорову ступку і розтирають з 2 мл дистильованої води до однорідної маси. До розтертої маси додають 3 мл 3%-го розчину сульфату міді, перемішують і переносять в центрифужну пробірку. Залишок споліскують 8 мл води. Пробірку кип'ятять на водяній бані 3 хв., періодично помішуючи скляною паличкою. Після цього пробірку виймають, додають З мл 0,2 н. розчину МаОН, перемішують, відстоюють 10 хв. і центрифугують. Розчин зливають у колбу К'єльдаля на 100 мл, а осад промивають двічі гарячою водою до 10 мл, додаючи до порцій промивної води по 1 краплі 3 %- го розчину сульфату міді.
Визначення небілкоеого азоту. До розчинів у колбі К'єльдаля додають 2 мл концентрованої сірчаної кислоти, 0,3 мл 10 %-го розчину молібдату натрію, 4 краплі 30%-го оксиду водню і випаровують на плиті до появи піни. Далі зменшують нагрівання так, щоб піна не потрапила в горло колби, і продовжують нагрівати до появи білої, пари сірчаної кислоти, Після цього колбу закривають скляною кульковою пробкою, збільшують нагрівання і спалюють до і просвітління розчину. Розчин охолоджують і до залишку в колбі і додають 10 мл дистильованої води, розчин переносять у мірну колбу на 50 мл, промивають залишок водою, перемішують і доводять водою до 50 мл.
Щоб визначити небілковий азот, 25 г розчину виливають у колбу для титрування додають 1 краплю 0,5%-ного розчину метилового оранжевого і, охолоджуючи, нейтралізують 2 н. розчином їдкого натру до переходу забарвлення індикатора в оранжево-жовтий колір (не перетитрува-ти!). Далі додають 10 мл фосфатного буферного розчину (рН-б,7), який містить бромід калію, 5 мл 0,12 н. розчину хлораміну. Колбу накривають годинниковим скельцем і залишають на 25 хв. Після цього додають 2 мл 20 % -го розчину йодиду калію, 10 мл 8 %-вого розчину щавлевої кислоті і йод, який виділився при ньому, титрують 0,02 н. розчином тіосульфату натрію при наявності індикатора крохмалю. 1 мл 0,02 н. розчину тіосульфату натрію відповідає 0,09338 мг азоту. Для підрахунку вмісту азоту в реактивах проводять контрольний дослід. Вміст небілкового азоту обчислюють за такою формулою:

де х - вміст небілкового азоту, %, 50 - об'єм досліджуваного розчину, мл,
25 - об'єм досліджуваного розвину, взятий для визначення небілкового азоту хлорамінним методом, мл,
а - об'єм 0,02 н. розчину тіосульфату натрію, витраченого на титрування контролю, мл,
б - об'єм 0,02 н. розчину тіосульфату натрію, витраченого на титрування досліджуваного розчину, мл, г - нормальність розчину тіосульфату натрію, п - наважка досліджуваного матеріалу, г.
Визначення білкового азоту. До осадку , який містить білковий азот, у пробірку доливають 5 мл дистильованої води, перемішують і виливають у колбу К'єльдаля місткістю 100 мл, залишок зливають невеликими порціями води. В колбу додають 0,3 мл 10 %-го розчину молібдату натрію, 0,4 г сульфату калію, 3 мл концентрованої Н2804, ставлять на плитку і випаровують при невеликому нагріванні до появи піни. Далі вміст колби охолоджують, додають 4 краплі ЗО %-го оксиду водню, знову ставлять на плитку і обережно нагрівають, не допускаючи підняття піни у горло колби. Як тільки розчин закипить, колбу закривають скляною пробкою і спалюють до просвітлення розчину. Розчин охолоджують і додають по стінці колби 10 мл дистильованої води. Розчин переносять у мірну колбу місткістю 50 мл, доливають водою до об'єму 50 мл і старанно збовтують.
Для визначення білкового азоту 10 мл розчину виливають у колбу для титрування, додають 1 краплю 0,1 %-го розчину метилового оранжевого і нейтралізують 2 н. розчину ЫаОН до переходу забарвлення індикатора в оранжево-жовтий колір. Після цього додають 10 мл фосфатного буферного розчину (рН=6,7), який містить КВг 5 мл 0,12 н. розчину хлораміну. Далі проводять усі ті операції, що й при визначенні небілкового азоту. Одночасно також проводять контрольний дослід на вміст азоту в реактивах. Вміст білкового азоту обчислюють за такою формулою:
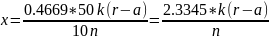
де х — вміст білкового азоту, %. Решту позначень дивись у раніше наведеній формулі.
Міністерство освіти і науки України
Криворізький технічний університет
Кафедра прикладної екології
