
- •Методичні вказівки
- •«Охорона повітря від забруднення та його нормування в газовому середовищі»
- •Охрана воздуха
- •Окислительная деградация и детоксикація атмосферных загрязнителей растениями
- •Методичні вказівки
- •«Поширення хімічних елементів та їх сполук в біосфері. Кларки основних хімічних елементів земної кори»
- •Методичні вказівки
- •«Комплексометричне визначення кальцію і магнію в рослинах»
- •Методичні вказівки
- •«Визначення марганцю в рослинах (за методом а.А. Власюка і л.Д. Лейденської)»
- •Методичні вказівки
- •«Визначення міді в рослинах»
- •Методичні вказівки
- •«Визначення бору в рослинах ( за методом х. М. Починка)»
- •Концентрація в, мкг/мг
- •Методичні вказівки
- •«Прискорене визначення азоту, фосфору і калію з однієї наважки (за методом к. Гінзбург та ін. )»
- •Методичні вказівки
- •«Визначення небілкового і білкового азоту в одній наважці методом хлораміну ( за методом х.М. Починка)»
- •Методичні вказівки
- •«Міграція хімічних елементів в організмі людини, тваринних та рослинних організмах»
Методичні вказівки
До виконання лабораторної роботи з курсу «Біогеохімія»
Для студентів спеціальності 7.070801
«Екологія та охорона навколишнього середовища»
Лабораторна робота № 4
«Визначення марганцю в рослинах (за методом а.А. Власюка і л.Д. Лейденської)»
Мета лабораторної роботи: визначити на рослинних зразках наявність марганцю в рослинах, наявність бору в рослинах (за методом А.А. Власюка і Л.Д. Лейденської)
Затверджено на засіданні
кафедри
прикладної екології
протокол
№_2__від _11.10___2010 р.
Кривий Ріг
2010
Обладнання, об'єкти, реактиви: фотоелектроколориметр ФЕК-М технохімічні терези; ситечко з діаметром отворів 0,25 мм; фарфорові тиглі; електроплитка; муфельна піч; фарфорові чашки; колби місткістю 25—100 мл; піпетки місткістю 5 мл; скляні палички; дослідні рослини. Реактиви. Азотна кислота, розбавлена (1:1). 0.2 %-й розчин нітрату срібла. 200 мг нітрату срібла розчиняють у 100 мл дистильованої води. Надсірчанокислий амоній, сухий реактив, 0,01 н. розчин КМпСЬ. 10 %-й розчин Ге804*7Н20
Основні відомості. Марганець бере участь в роботі багатьох біокаталізаторів — ферментів, які регулюють процеси фотосинтезу, дихання, азотного обміну тощо. Проте ще багато питань фізіологічної ролі марганцю в обміні речовин рослинного організму досі не вивчено. Суть цього методу визначення марганцю в рослинах полягає в оксидації двовалентного марганцю до семивалентного за допомогою надсірчанокислого амонію при наявності каталізатора— нітрату срібла. Оксидація відбувається в кислому середовищі при нагріванні. В результаті утворюється аніон марганцевої кислоти, який забарвлює розчин у фіолетово-рожевий колір. Інтенсивність забарвлення пропорційна кількості-марганцю в розчині.
Проведення роботи. Подрібнений повітряно-сухий рослинний матеріал просівають крізь решето з діаметром отворів 0,25 мм, відважують 1-3 г, кладуть у фарфоровий прожарений тигель і спалюють без втрат на плитці, а потім у муфелі при темно-червоному розжаренні. Тигел охолоджують, а золу розчиняють 45 мл розбавленої азотної кислоти (1:1). Розчин переливають у фарфорову чашку, тигель споліскують і для повного розчинення оксиду марганцю додаюсь 1—2 краплі 10 %-го розчину Ге804*7Н20 Після цього вміст чашки випаровують до суха. Сухий залишок у чашці розчиняють у 2 мл азотної кислоти (1:1) і переносять у колбу місткістю 100 мл, змивають поверхню чашки дистильованою водою, наливаючи води приблизно до об'єму 30 мл. До розчину в колбі додають 1—2 мл 0,2 %-го розчину нітрату срібла (для осадження залишків хлору і як каталізатор для окислення нітратних солей марганцю в марганцеву кислоту). Нагрівають до кипіння, шоо осадити хлориди, і фільтрують у мірну колбу місткістю 100 мл. Осад на фільтрі промивають кілька разів дистильованою водою (кількість промив -іих вод не повила перевищувати об'єму колби). Фільтрат доводять до риски водою перемішують і визначають вміст марганцю. З цією метою в колбочки місткістю 25 мл (якщо аналізують стебла і листки) і місткість:» 40 мл (якщо аналізують корені або насіння) додають по 5 мл розбавленої (1:1) азотної кислоти, нагрівають до кипіння і обережно додають приблизно 1 г сухого падсірчанокислого амонію. Далі кип'ятять 2 хв до появи стійкого забарвлення, розчин охолоджують, розбавляють дистильованою водою до 60 мл і колоримєтрують на фотоелектроколориметрі. Щоб визначення було точним, проводять контрольне визначення марганцю в реактивах. Знайдену кількість марганцю при контрольному визначенні віднімають від результатів досліду. Результата обчислюють за такою формулою:
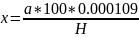
де X — кількість марганцю в рослині, %; а — кількість марганцю, знайдена за калібрувальним графіком: Н — наважка, взята для аналізу г: 300— перерахунок (проценти); 0.00010е) — кількість марганцю, що міститься в 1 мл 0,01 в;, розчину, г
Виготовлення стандартних розчинів для калібрувального графіка. Беруть 0,3 мг. 0,5 мг, 0.7 мг, 0,9 мг (1. 2, 3, 4, 5 мл) 0,01 н. розчину перманганату калію в мірні колбочки місткістю 50 мл, розбавляють дистильованою водою до риски і порівнюють на ФЕК На підставі добутих даних будують калібрувальний графік.
Міністерство освіти і науки України
Криворізький технічний університет
Кафедра прикладної екології
