
- •1Лабораторна робота: Одержання каталізаторів глибокого окислення вуглеводів (метану) методом співосадження активних компонентів
- •1.1Стислі теоретичні відомості
- •1.2Експериментальна частина
- •1.3Методика розрахунку
- •2.2Експериментальна частина
- •2.3Методика розрахунку
- •3.2Експериментальна частина
- •3.3Методика розрахунку
- •4.2Експериментальна частина
- •4.3Методика розрахунків
- •5.2Експериментальна частина
- •6.2Експериментальна частина
- •6.3Обробка експериментальних даних
- •7.2Експериментальна частина
- •7.3Методика розрахунків
- •7.4Результати
- •7.5Висновки
- •8Лабораторна робота: Визначення загальної поруватості каталізатора
- •8.1Короткі теоретичні відомості
- •8.2Експериментальна частина
- •8.3Методика розрахунків
- •8.4Результати
- •8.5Висновки
- •9Лабораторна робота: Розрахунок кінетичних параметрів
- •I спосіб:
- •II спосіб:
6.3Обробка експериментальних даних
Розрахунки заносять до таблиці 6.1 (кількість таблиць відповідає кількості зразків, що досліджуються).
Таблиця 6.1 – Допоміжна таблиця
Номер зразка |
Експеримент |
Розрахунки |
||||
|
p/ps |
Δg, г |
V, г/моль |
1- p/ps |
V·(1- p/ps) |
p/ps/( V·(1- p/ps)) |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Встановлені або розраховані за формулою (5.3) значення заносять до колонки 2 .
Розраховують кількість адсорбованого бензолу (колонка 3)
![]() , (6.4)
, (6.4)
де
 - останнє значення при зважуванні ( маса
пікнометра + маса наважки максимально
насиченої бензолом),
- останнє значення при зважуванні ( маса
пікнометра + маса наважки максимально
насиченої бензолом),
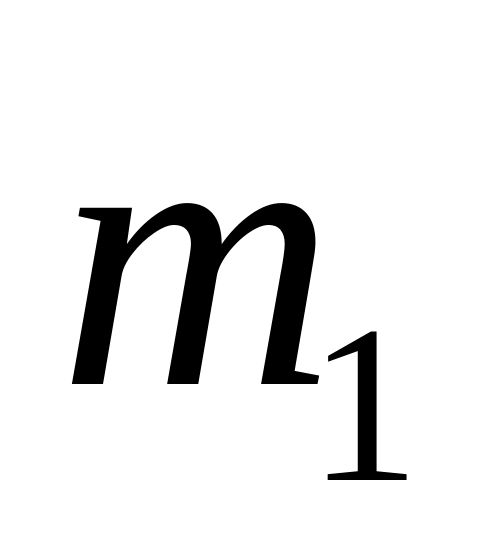 - маса пікнометра + маса наважки (перед
адсорбцією бензолу).
- маса пікнометра + маса наважки (перед
адсорбцією бензолу).Розраховують кількість адсорбованого бензолу в молях на г наважки (колонка 4):
![]() , (6.5)
, (6.5)
де
![]() - адсорбованого бензолу, г; g
– маса
наважки сорбенту, г; 78 – молекулярна
маса бензолу, моль/г.
- адсорбованого бензолу, г; g
– маса
наважки сорбенту, г; 78 – молекулярна
маса бензолу, моль/г.
Розраховують значення ординати для лінеаризованої теорії БЕТ (колонка 7), для зручності спочатку розраховують колонку 6.
Рівняння БЕТ в лінеаризованій формі:
 ,
(6.6)
,
(6.6)
де
![]() - константи і
- константи і
![]() - кількість бензолу, що відповідає
мономолекулярному покриттю адсорбента.
- кількість бензолу, що відповідає
мономолекулярному покриттю адсорбента.
Будують графік
 ,
тоді тангенс нахилу цієї прямої
,
тоді тангенс нахилу цієї прямої
 ,
а відрізок на осі ординат
,
а відрізок на осі ординат
 .
.Розв’яжемо систему рівнянь:
![]()
![]() ,
,
![]() .
.
Питома поверхня каталізатора:
![]() ,
(6.7)
,
(6.7)
де
![]() - число Авогадро; S
=
39·10-20
– площа, яку займає одна молекула
бензолу, м2.
- число Авогадро; S
=
39·10-20
– площа, яку займає одна молекула
бензолу, м2.
6.4Результати
6.5Висновки
7Лабораторна робота: Каталітичне окислення монооксиду вуглецю
Мета роботи: дослідження ступеня окислення оксиду вуглецю (II) залежно від виду каталізатора, температури, надлишку повітря та об’ємної швидкості газового потоку.
7.1Стислі теоретичні відомості
Очищення газових викидів від монооксиду вуглецю (II) є актуальною проблемою в хімічній, металургійній, нафтохімічній промисловості. Найперспективнішим методом очищення є каталітичне окислення оксиду вуглецю (II) до оксиду (IV) за рівнянням:
2СО + О2 = 2СО2 + Q (1.1)
В практиці найбільше поширення отримали паладієві та платинові каталізатори. Враховуючи величезний дефіцит в Україні паладію та платини, заміна каталізаторів платинової групи на не платинові має практичну цінність. Активність у реакціях окислення проявляють сітчасті каталізатори на основі нітридів Al, Zr, Ti, а також каталізатори на основі лантану.
Дослідження впливу типу каталізатора, температури процесу, об’ємної швидкості газового потоку, концентрації кисню, дозволяє визначити оптимальний режим окислення.
