
- •Химическая технология
- •Содержание
- •Введение
- •1. Порядок прохождения лабораторного практикума
- •1.1. Правила и приемы безопасной работы в лаборатории
- •1.1.1. Токсикологическая характеристика веществ, применяемых в практикуме
- •1.1.2. Требования безопасности перед началом работы
- •1.1.3. Требования безопасности во время работы
- •1.1.4. Требования безопасности в аварийной ситуации
- •1.1.5. Требования безопасности по окончании работы
- •1.1.6. Требования пожарной безопасности
- •1.1.7. Характеристика пожарной опасности применяемых веществ
- •1.2. Отчет о лабораторной работе
- •1.2.1. Оформление и представление отчета
- •2.1.2. Методика проведения работ по «варке» гипса
- •2.2.2. Методика выполнения работы
- •Контрольные вопросы
- •2.3.2. Методика проведения работы
- •2.4.2. Методика проведения работы
- •2.5.2. Методика проведения работы Вариант I
- •Вариант II
- •Контрольные вопросы
- •2.6.2. Методика проведения работ Вариант 1
- •Инструкция к лабораторной работе
- •Вариант 2
- •2.7.2. Методика проведения работы
- •2.7.3. Испытание защитных свойств фосфатной пленки
- •Инструкция к лабораторной работе «Фосфатирование металлов»
- •2.8.2. Методика проведения работы Вариант I – объемный метод определения скорости коррозии в электролитах
- •Вариант II – гравиметрический метод определения скорости коррозии металлов в кислых средах
- •2.9.2. Методика проведения работы
- •Контрольные вопросы и задачи
- •Список литературы
- •2.10. Лабораторная работа «получение амиачной селитры»
- •2.10.1. Краткие теоретические сведения
- •2.10.2. Порядок выполнения работы
- •2.10.3. Анализ аммиачной селитры на содержание аммонийного азота
- •2.11.2. Схема установки и порядок выполнения работы
- •2.11.3. Анализ щелоков производства гидроксида натрия «Определение общей щелочности»
- •2.12.2. Методики проведения работы
- •Контрольные вопросы
- •Литература
- •Заключение
- •Химическая технология
- •1 56961, Г. Кострома, ул. 1 Мая, д. 14
Вариант II
Цель работы – получить серный ангидрид и серную кислоту контактным способом. Сернистый газ получают в результате прохождения реакции медных стружек с концентрированной серной кислотой.
Оборудование и реактивы:
Газометр или баллон с кислородом
Источник сернистого газа (колба, капельная воронка, серная кислота, медные стружки или бисульфит натрия)
Склянки Дрекселя и склянка Вульфа
Фарфоровая или кварцевая трубка
Катализатор (пятиокись ванадия и асбест)
U-образная трубка
Две пробирки
Стакан с охлаждающей смесью или снегом
Электропечь
Пирометр с термопарой
Электрофильтр
Индукционная катушка
Аккумулятор
Ход работы: Ниже описывается более простой вариант получения серного ангидрида и серной кислоты (рис. 2.5.2). Выход серной кислоты не определяется.
Сернистый газ получается взаимодействием медных стружек с концентрированной серной кислотой в колбе 1. Для осушки сернистый газ проходит через осушительную склянку 2 с серной кислотой, а затем поступает в смеситель 3. Туда же из газометра поступает кислород, который предварительно проходит через счетчик пузырьков – промывную склянку, наполненную серной кислотой, и колонки с хлористым кальцием. В смесителе 3 газы подвергаются дополнительной осушке.
Газовая
смесь поступает в фарфоровую или
кварцевую трубку 4,
наполненную
ванадиевым катализатором. Для его
приготовления берут порошкообразную
пятиокись ванадия, которую перемешивают
с асбестом. После контактирования серный
ангидрид поступает в U-образный
приемник 5,
опущенный в охладительную смесь. Частично
серный ангидрид поступает в пробирки
с подкисленным раствором хлорида бария
7
и с раство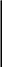 ром
индикатора 5,
позволяющего обнаружить наличие ионов
водорода.
ром
индикатора 5,
позволяющего обнаружить наличие ионов
водорода.
Перед началом работы включают электропечь и пропускают небольшое количество кислорода (~0,5 л). Когда температура печи достигнет 500 °С, в колбу с медными стружками наливают серной кислоты и подогревают до получения равномерного тока сернистого газа. Одновременно пропускают кислород и включают электрофильтр. Газы должны проходить со скоростью 1–2 пузырька в 1 сек. Необходимо следить за показаниями пирометра, так как перегрев печи приводит к снижению выхода серного ангидрида и к порче катализатора, а охлаждение уменьшает выход серного ангидрида.
В U-образной трубке постепенно накапливается серный ангидрид, в первой пробирке образуется осадок сульфата бария, а во второй – изменяется окраска индикатора.
После прекращения подачи газа выключают печь. К серному ангидриду добавляют 1–1,5 мл серной кислоты и получают олеум.
Примечание. Трубку с катализатором можно обогревать пламенем газовой горелки или 2–3 спиртовками. Можно также на трубку навить спираль от электроплитки и подключить к электроосветительной сети. В простейшем случае можно взять стеклянную трубку диаметром 1 см и нагревать спиртовкой.
В этом опыте можно воспользоваться кислородом воздуха. Скорость прохождения пузырьков воздуха должна быть в 3–4 раза больше скорости прохождения сернистого газа. При использовании воздуха серный ангидрид сильно разбавлен азотом, и потому его конденсация происходит с трудом: большая часть серного ангидрида проходит в пробирки, а затем в виде тумана поступает в электрофильтр.
Рис.2.5.2. Получение серного ангидрида и серной кислоты
контактным способом:
1 – колба для получения сернистого газа; 2 – осушительная склянка с серной
кислотой; 3 – смеситель – промывалка с серной кислотой; 4 – трубка с ванадиевым катализатором; 5 – приемник для серного ангидрида; 6 – охладительная смесь; 7 – пробирка с хлоридом бария; 8 – пробирка с индикатором;
9 – термопара; 10 – пирометр; 11 – электропечь; 12 – электрофильтр;
13 – индукционная катушка; 14 – аккумулятор.
Оформление результатов работы
Зарисовать установку для получения серного ангидрида и серной кислоты и описать ее работу.
