
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
§3. Условия равновесия на границе двух сред. Краевой угол
Р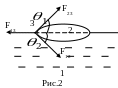 ассмотрим
условия, возникающие на границе
соприкосновения двух несмешивающихся
друг с другом жидкостей.
ассмотрим
условия, возникающие на границе
соприкосновения двух несмешивающихся
друг с другом жидкостей.
Пусть капля жидкости
2 помещена на поверхности другой жидкости
1 (рис.2). В зависимости от видов жидкостей
капля второй жидкости может иметь вид
чечевицы или же образовать пленку.
Рассмотрим, при каких условиях образуется
чечевица, а при каких - тонкая пленка. В
рассматриваемом случае граничат друг
с другом следующие среды: жидкость 1
граничит с жидкостью 2, жидкости 1
и 2 граничат со средой 3. Среда 3 – это
смесь паров
жидкостей 1 и 2 с воздухом. Границей
соприкосновения трех сред является
окружность, ограничивающая чечевицу.
На элемент длины
![]() этой окружности
действуют три силы поверхностного
натяжения:
этой окружности
действуют три силы поверхностного
натяжения:
![]() - сила на границе
между жидкостями 1 и 2;
- сила на границе
между жидкостями 1 и 2;
![]() - сила на границе
жидкость 1-газ;
- сила на границе
жидкость 1-газ;
![]() -
сила на границе жидкость 2-газ.
-
сила на границе жидкость 2-газ.
Каждая из этих сил направлена по касательной к поверхности соприкосновения соответствующих сред. Чтобы жидкость 2 находилась в равновесии, необходимо, чтобы сумма проекций всех трех сил на оси координат равнялись нулю, т.е.
![]() ,
,
![]() ,
(6.4)
,
(6.4)
или
![]() ,
,
![]() .
(6.5)
.
(6.5)
Возведя оба эти равенства в квадрат, и сложив их, получим:
![]() ),
),
или
![]() .
(6.6)
.
(6.6)
Уравнениями (6.5) и
(6.6) определяются углы
![]() и
и
![]() .
Углы
называются
краевыми углами. Краевые углы определяются
соотношением трех коэффициентов
.
Углы
называются
краевыми углами. Краевые углы определяются
соотношением трех коэффициентов
![]() .
В частности, соотношение между
коэффициентами
может быть
таким, что
.
В частности, соотношение между
коэффициентами
может быть
таким, что
![]() ,
т.е.
,
т.е.
![]() .
Тогда жидкость 2 растекается тонким
слоем по поверхности жидкости 1. В этом
случае говорят, жидкость 1 полностью
смачивается жидкостью 2. Физически это
означает, что сила
.
Тогда жидкость 2 растекается тонким
слоем по поверхности жидкости 1. В этом
случае говорят, жидкость 1 полностью
смачивается жидкостью 2. Физически это
означает, что сила
![]() по величине
больше равнодействующей сил
по величине
больше равнодействующей сил
![]() ,
или
,
или
![]() .
Если
.
Если
![]() ,
то жидкость будет стягиваться до тех
пор, пока
не станет
равной
,
то жидкость будет стягиваться до тех
пор, пока
не станет
равной
![]() .
Это и есть условие образования чечевицы.
.
Это и есть условие образования чечевицы.
§4. Граница жидкости и твердого тела
Пусть жидкость 2 (см. рис.3) граничит с плоской поверхностью твердого тела 1. Величина кривого угла определяется из условия равновесия, т.е.
![]() ,
,
откуда
![]() .
Если
.
Если
![]() ,
то
,
т.е. жидкость расте-
,
то
,
т.е. жидкость расте-
к ается
тонким слоем по поверхности твердого
тела. Это же будет наблюдаться и при
ается
тонким слоем по поверхности твердого
тела. Это же будет наблюдаться и при
![]() .
Явление полного растекания жидкости
называется полным
смачиванием (примером является растекание
воды на чистом стекле). Случай
.
Явление полного растекания жидкости
называется полным
смачиванием (примером является растекание
воды на чистом стекле). Случай
![]() (
(![]() )
соответствует
полному несмачиванию твердого тела
жидкостью. Больше всех наблюдаются
промежуточные случаи частичного
смачивания (
)
соответствует
полному несмачиванию твердого тела
жидкостью. Больше всех наблюдаются
промежуточные случаи частичного
смачивания (![]() (рис.4) или же частичного несмачивания
(
(рис.4) или же частичного несмачивания
(![]() (рис.5).
(рис.5).

В заимодействие
частиц жидкости с частицами твердого
тела влияет и на форму поверхности
жидкости, налитой в сосуд. Если большое
количество жидкости налито в широкий
сосуд, то форма ее поверхности определяется
силой тяжести, которая обеспечивает
плоскую и горизонтальную поверхность.
Однако у самих стенок сосуда поверхность
жидкости все же искривлено, так что
возникает мениск вогнутый у смачивающих
жидкостей (рис.6) и выпуклый у несмачивающих.
заимодействие
частиц жидкости с частицами твердого
тела влияет и на форму поверхности
жидкости, налитой в сосуд. Если большое
количество жидкости налито в широкий
сосуд, то форма ее поверхности определяется
силой тяжести, которая обеспечивает
плоскую и горизонтальную поверхность.
Однако у самих стенок сосуда поверхность
жидкости все же искривлено, так что
возникает мениск вогнутый у смачивающих
жидкостей (рис.6) и выпуклый у несмачивающих.
