
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
Скорость газовых молекул
Введём понятие
среднеквадратичной скорости
ср.кв.,
определив следующим образом:
![]()
Тогда из уравнения (3.11) получим выражение для среднеквадратичной скорости
![]() ,
(3.14)
,
(3.14)
которая для данного газа зависит только от температуры. Отметим, что в этой формуле m-это масса одной частицы.
Перепишем формулу (3.14), используя следующие преобразования
![]() . (3.15)
. (3.15)
Здесь m=mNA
– молярная масса газа. Так как для
одного моля идеального газа RТ=PV,
а
![]() ,
где
,
где
![]() – плотность газа, имеем
– плотность газа, имеем
![]() .
(3.16)
.
(3.16)
Выражение (3.16) не
означает, что
ср.кв.
зависит от давления газа и его плотности.
В это уравнение входит отношение
![]() ,
а так как давление и плотность изменяются
одинаково, то их отношение не зависит
ни от плотности, ни от давления.
,
а так как давление и плотность изменяются
одинаково, то их отношение не зависит
ни от плотности, ни от давления.
Скорость ср.кв. того же порядка, что и скорость звука в газе, которая определяется как
![]() ,
,
где g - адиабатическая постоянная.
Обе скорости связаны соотношением
![]() .
.
Из формулы (3.15) для
молекулярного водорода (m=2,016кг/кмоль)
при температуре 0oС
получим следующее значение
![]() .
.
§3. Броуновское движение
Одним из наиболее убедительных подтверждений основ молекулярно-кинетической теории является броуновское движение. Это явление было открыто в 1827 году английским ботаником Броуном. Оно заключается в том, что все мельчайшие частицы, взвешенные в жидкости, находятся в непрерывном движении. Характер броуновского движения зависит от свойств жидкости и газа, в которых взвешены частицы, но не зависит от свойств вещества самих частиц. Скорость движения броуновских частиц возрастает с повышением температуры и с уменьшением размеров частиц. Все эти закономерности легко объяснить, если мы примем, что движения взвешенных частиц возникают вследствие ударов, испытываемых ими со стороны беспорядочно движущихся молекул жидкости или газа, в которых они находятся.
Броуновское движение объясняется тем, что благодаря хаотичному движению молекул, число ударов молекул на взвешенную частицу с разных сторон не будет одинаковым, в результате возникает некоторая равнодействующая сила определенного направления. Это приводит к движению броуновской частицы по направлению этой силы. Через короткий промежуток времени направление равнодействующей силы изменится и вместе с тем изменится направление движения частицы. Отсюда следует хаотичное движение броуновских частиц, отражающая хаотичность молекулярного движения. Вероятность возникновения равнодействующей силы, связанной ударами молекул о частицу тем больше, чем меньше размеры частиц.
Рассмотрим количественную теорию броуновского движения, созданную Эйнштейном и независимо Смолуховским.
Вследствие неполной
компенсации ударов молекул на броуновскую
частицу действует, как мы указали выше,
некоторая результирующая сила
![]() ,
под действием которой и частица движется.
Кроме этой силы на частицу действует
сила трения
,
под действием которой и частица движется.
Кроме этой силы на частицу действует
сила трения
![]() ,
вызванная вязкостью среды и направленная
против силы
.
Для простоты предположим, что броуновские
частицы имеют форму сферы радиуса
,
вызванная вязкостью среды и направленная
против силы
.
Для простоты предположим, что броуновские
частицы имеют форму сферы радиуса
![]() .
Тогда сила трения может быть выражена
формулой Стокса:
.
Тогда сила трения может быть выражена
формулой Стокса:
![]() ,
(3.17)
,
(3.17)
где
![]() - коэффициент
вязкости среды,
- скорость
движения частицы. Уравнение движения
частицы запишется в виде:
- коэффициент
вязкости среды,
- скорость
движения частицы. Уравнение движения
частицы запишется в виде:
![]() .
(3.18)
.
(3.18)
Здесь
![]() - масса
частицы,
- масса
частицы,
![]() - радиус-вектор
относительно произвольной системы
координат,
- радиус-вектор
относительно произвольной системы
координат,
![]() - скорость частицы.
- скорость частицы.
Рассмотрим проекцию радиус-вектора на ось Х. Для этой составляющей уравнение (3.18) перепишется в виде:
![]() ,
(3.19)
,
(3.19)
где
![]() - проекция
результирующей силы
на ось Х.
- проекция
результирующей силы
на ось Х.
Наша задача
определить смещение
![]() броуновской частицы, которое она получит
под действием ударов молекул. Различные
частицы получают смещение, отличающиеся
как по величине, так и по направлению.
Вероятное значение суммы смещений всех
частиц равно нулю, так как смещения с
одинаковой вероятностью могут быть как
положительными, так и отрицательными.
Среднее значение смещения частиц
броуновской частицы, которое она получит
под действием ударов молекул. Различные
частицы получают смещение, отличающиеся
как по величине, так и по направлению.
Вероятное значение суммы смещений всех
частиц равно нулю, так как смещения с
одинаковой вероятностью могут быть как
положительными, так и отрицательными.
Среднее значение смещения частиц
![]() также будет
также равно нулю. Но не будет равно нулю
среднее значение квадрата смещения
также будет
также равно нулю. Но не будет равно нулю
среднее значение квадрата смещения
![]() .
Преобразуем уравнение (3.19) так, чтобы в
него входила величина
.
Преобразуем уравнение (3.19) так, чтобы в
него входила величина
![]() .
Для этого умножим обе части этого
уравнения на
:
.
Для этого умножим обе части этого
уравнения на
:
![]() .
(3.20)
.
(3.20)
Используем очевидные тождества:
 .
.
Поставив это выражение в (3.20), получим:
![]() .
.
Это равенство для любой частицы и поэтому она справедлива также для средних значений входящих в него величин, если усреднение вести по достаточно большому числу частиц. Поэтому можно записать:
![]() .
.
![]() - среднее значение
квадрата составляющей скорости частицы
по оси Х. Для большого числа частиц
и
одинаково
часто принимают как положительные, так
и отрицательные значения, поэтому
- среднее значение
квадрата составляющей скорости частицы
по оси Х. Для большого числа частиц
и
одинаково
часто принимают как положительные, так
и отрицательные значения, поэтому
![]() .
Уравнение
(3.19) примет вид:
.
Уравнение
(3.19) примет вид:
![]() .
(3.21)
.
(3.21)
Так как движения частиц вполне хаотичны, средние значения квадратов составляющих скорости по всем трем координатным осям должны быть равны друг другу, т.е.
![]() .
.
Очевидно, что
![]() ,
,
где
![]() - среднее
значение квадрата скорости частицы,
откуда следует
- среднее
значение квадрата скорости частицы,
откуда следует
![]() .
.
Таким образом, интересующее нас выражение, входящее в (3.21), равно:
![]() ,
,
где
![]() - средняя
кинетическая энергия броуновской
частицы.
- средняя
кинетическая энергия броуновской
частицы.
Сталкиваясь с
молекулами жидкости или газа, броуновские
частицы обмениваются с ними энергией,
и находятся в тепловом равновесии со
средой, в которой они находятся. Поэтому
средняя кинетическая энергия
поступательного движения броуновской
частицы должны быть равна средней
кинетической энергии молекул жидкости
или газа, которая равно, как известно,
![]() :
:
![]() .
.
Следовательно
![]() .
(3.22)
.
(3.22)
Учитывая (3.22), уравнение (3.21) перепишется в виде:
![]() .
(3.23)
.
(3.23)
Это уравнение
легко интегрируется. Обозначив
![]() ,
получим:
,
получим:
![]() .
.
После разделения переменных, имеем:
 .
.
Интегрируя левую часть этого уравнения в пределах от 0 до z, а правую от 0 до t, получим:
 .
.
Или
![]() .
.
Отсюда
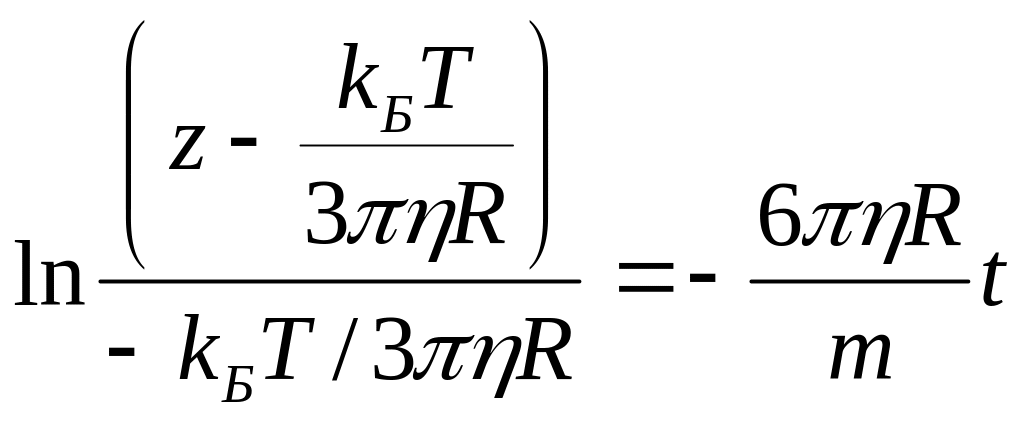 .
.
Из этого выражения получим, что
![]() .
.
Величина
![]() ничтожно
мала, если отрезок времени между
последовательными наблюдениями за
частицей превышает 10-5
сек., что, конечно, всегда имеет место.
Тогда можем записать:
ничтожно
мала, если отрезок времени между
последовательными наблюдениями за
частицей превышает 10-5
сек., что, конечно, всегда имеет место.
Тогда можем записать:
![]() .
(3.24)
.
(3.24)
Для конечных
промежутков времени
![]() и соответствующих
перемещений
и соответствующих
перемещений
![]() ,
уравнение (3.24) можно переписать в виде:
,
уравнение (3.24) можно переписать в виде:
![]() .
.
Тогда
![]() .
(3.25)
.
(3.25)
Среднее значение квадрата смещения броуновской частицы за промежуток времени вдоль оси Х или другой любой оси, пропорционально этому промежутку времени. Формула (3.25) позволяет вычислить средние значения квадрата перемещений по всем частицам, участвующим в явлении. Но эта формула справедлива и для среднего значения квадрата многих последовательных перемещений одной единственной частицы за равные промежутки времени.
