
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
§15. Цикл Карно
Одним из процессов, часто происходящих в природе при переходе какой-нибудь системы к равновесию является превращение механической энергии в тепловую. Выделение тепла за счёт механической энергии – это процесс превращение макроскопической энергии в энергию микроскопических тепловых движений. Обратный этому процесс – это превращение тепловой энергии в механическую или получение механической энергии за счёт тепла
Иногда результатом произведённой механической работы может явиться возникновение равного количества тепла. Это значит, что энергия макроскопического движения целиком переходит в энергию микроскопических движений молекул вещества, т. е. механическая работа может полностью превратиться в теплоту. Возникает вопрос – тепловая энергия может ли полностью перейти в механическую работу. Для этого рассмотрим цикл Карно, в процессе которого тепловая энергия преобразуется в механическую работу.
Для того чтобы теплота могла быть использована для получения работы, необходимо каким – то образом отнять у тела часть его тепловой энергии. Это можно сделать, приводя в соприкосновение другое тело с более низкой температурой. Благодаря теплопроводности тепло будет передаваться от одного тела к другому. Это необратимый процесс, он не сопровождается совершением работы, так как в этом процессе нет никакого перемещения тел. Таким образом, простой обмен теплом двух соприкасающихся тел различной температуры не может привести к совершению работы. Необходимо третье тело, которое бы принимало тепло от более нагретого тела, перемещаясь при этом, передавало бы его менее нагретому и при этом оно совершило бы механическую работу. Это промежуточное тело будем называть рабочим телом. Более нагретое тело назовём нагревателем, более холодное тело холодильником. Процесс получения тепла от нагревателя и передачи к холодильнику должен произойти при одинаковых температурах. В противном случае необратимый процесс теплопроводности будет приводить к бесполезной потере теплоты. Всё сказанное относится к реально существующим установкам для превращения тепла в механическую работу (паровые машины, турбины, двигатели внутреннего сгорания), которые действуют циклически, т. е. процесс передачи энергии от нагретого тела к холодному телу периодически повторяется. Рабочее тело, совершив определённые процессы, при которых через его посредство от нагревателя к холодильнику было передано некоторое количество теплоты, а им совершена некоторая работа, возвращается в исходное состояние, чтобы снова начать весь процесс. Другими словами рабочее тело претерпевает круговой процесс – т. е. совершает цикл. Работа, совершаемая во время кругового процесса равна поглощаемому количеству теплоты, т.е. Q=A
Рассмотрим круговой процесс, при котором тепло, отнятое от какого-нибудь тела, можно превратить в работу, так чтобы эта работа была максимальной. Чтобы осуществит этот процесс нужно иметь три тела: нагреватель – рабочее тело – холодильник. Предположим, что нагреватель и холодильник имеют большую теплоёмкость, так что за счёт отданного или полученного тепла их температуры не меняются (рис.3).
Н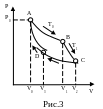 ачнём
круговой процесс над рабочим телом с
того, что оно сжатое до некоторого
давления, находится в контакте с
нагревателем и имеет такую же температуру,
что и нагреватель. Процесс теплопроводности
при этом не происходит, так как нет
разности температур. Таким образом, не
происходит передача тепла без совершения
работы. Представим рабочему телу
возможность расшириться, оставаясь в
контакте с нагревателем.
AB
– изотермическое расширение. При этом
будет совершена работа. Она будет
совершена за счёт тепла отнятого у
нагревателя. Полученное тепло нужно
передать холодильнику. Это нельзя
осуществить при непосредственном
соприкосновении рабочего тела с
холодильником, потому что тепло будет
переходить к холодильнику без совершения
полезной работы. Рабочее тело нужно
охладить до температуры холодильника.
Для охлаждения рабочее тело должно быть
теплоизолированным от нагревателя и
испытывать адиабатическое расширение.
При этом рабочее тело охлаждается и
совершает работу. В точке C
рабочее тело приводят в соприкосновение
с холодильником. При этом завершается
первая половина цикла, во время которого
тело совершает полезную работу за счёт
тепла, полученного от нагревателя.
ачнём
круговой процесс над рабочим телом с
того, что оно сжатое до некоторого
давления, находится в контакте с
нагревателем и имеет такую же температуру,
что и нагреватель. Процесс теплопроводности
при этом не происходит, так как нет
разности температур. Таким образом, не
происходит передача тепла без совершения
работы. Представим рабочему телу
возможность расшириться, оставаясь в
контакте с нагревателем.
AB
– изотермическое расширение. При этом
будет совершена работа. Она будет
совершена за счёт тепла отнятого у
нагревателя. Полученное тепло нужно
передать холодильнику. Это нельзя
осуществить при непосредственном
соприкосновении рабочего тела с
холодильником, потому что тепло будет
переходить к холодильнику без совершения
полезной работы. Рабочее тело нужно
охладить до температуры холодильника.
Для охлаждения рабочее тело должно быть
теплоизолированным от нагревателя и
испытывать адиабатическое расширение.
При этом рабочее тело охлаждается и
совершает работу. В точке C
рабочее тело приводят в соприкосновение
с холодильником. При этом завершается
первая половина цикла, во время которого
тело совершает полезную работу за счёт
тепла, полученного от нагревателя.
Сейчас рабочее тело надо вернуть к исходному состоянию. Это делается в два этапа: CD – изотермическое сжатие, во время которого рабочее тело находится в контакте с холодильником, DA – адиабатическое сжатие до температуры нагревателя, при этом оно нагревается за счёт внешней работы, совершаемой над ним. Рабочее тело приводят в соприкосновение с нагревателем. При сжатии работа совершается внешними силами. На всех стадиях кругового процесса не допускается соприкосновения тел с различной температурой, т. е. весь процесс идёт обратимо. Это цикл Карно. В результате первого процесса Карно некоторое количество тепла оказывается переданным посредством рабочего тела от нагревателя к холодильнику. В ходе этого процесса рабочее тело совершает некоторую работу. Во второй половине процесса над рабочим телом совершают работу внешние силы. Получается ли при этом полезная механическая работа.
Для этого рабочее
тело представим как идеальный газ. Пусть
рабочее тело представляет 1 моль
идеального газа и пусть исходное
состояние характеризуется точкой
A(Po,Vo).
Температура газа
![]() равна
температуре нагревателя, T1-
температура холодильника. Значит T0>T1.
При изотермическом расширении на участке
АВ совершается работа
равна
температуре нагревателя, T1-
температура холодильника. Значит T0>T1.
При изотермическом расширении на участке
АВ совершается работа
A1=RT0ln![]() =Q0
,
=Q0
,
где Q0- количество теплоты отнятое газом у нагревателя. Bо втором этапе газ изолируется от нагревателя и дальнейшее его расширение происходит адиабатно, вследствие чего газ охлаждается. Это адиабатическое расширение продолжается до тех пор, пока температура газа не станет равной температуре холодильника. Значит, объём V2, до которого должен расшириться газ определяется из уравнения адиабаты
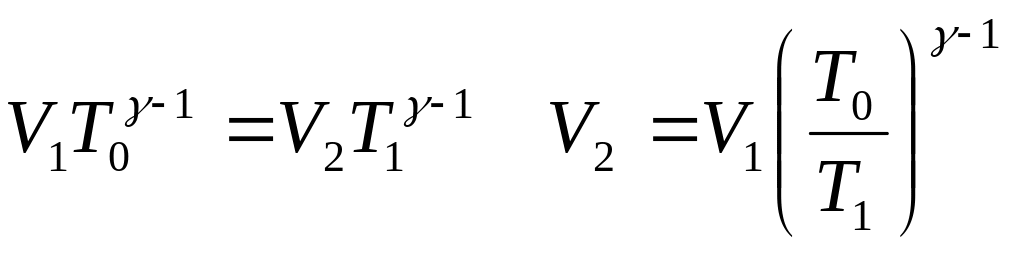 .
(1.33)
.
(1.33)
Работа, совершаемая во втором процессе на участке ВС равна
![]() .
.
Таким образом, вся положительная работа, совершаемая газом при его расширении равна
![]() .
.
На третьем этапе (участок СД) газ изотермически сжимается внешними силами при температуре холодильника Т1 от объема V2 до объема V3. При этом совершается работа
![]() ,
,
которая выделяется в виде тепла и передаётся холодильнику.
В последнем этапе ДА происходит адиабатное сжатие до исходного объема V0 давления Р0, при которых температура станет равной Т0. Для этого необходимо, чтобы объем V3, до которого изотермически сжимается газ, определился следующим образом
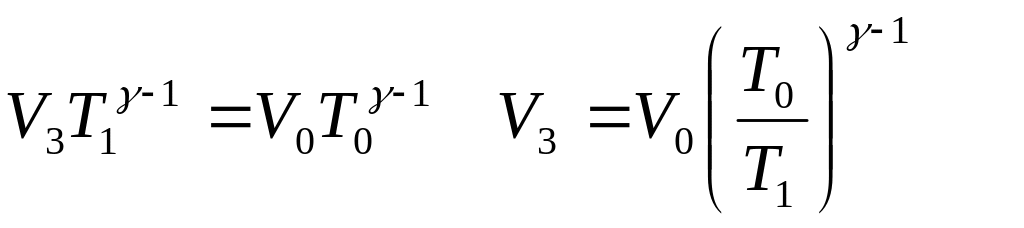 (1.34)
(1.34)
Работа сжатия на этом этапе равна
![]() .
.
Газ теперь опять в первоначальном состоянии, цикл Карно завершен, и процесс можно снова начать. Общая работа, совершенная газом, равна
![]() .
.
Из формул (1.33) и (1.34) следует
![]() .
.
Следовательно, общая работа
![]() ,
,
и так как
![]() ,
то A>0.
Значит, работа, совершаемая газом при
расширении, больше работы внешних сил,
затраченной на его сжатие. За счёт
теплоты, полученной рабочим телом от
нагревателя, совершена, таким образом,
некоторая полезная работа. Это работе
не равно количеству теплоты Q0,
которое рабочее тело получило от
нагревателя. Из отданного нагревателем
количества тепла
,
то A>0.
Значит, работа, совершаемая газом при
расширении, больше работы внешних сил,
затраченной на его сжатие. За счёт
теплоты, полученной рабочим телом от
нагревателя, совершена, таким образом,
некоторая полезная работа. Это работе
не равно количеству теплоты Q0,
которое рабочее тело получило от
нагревателя. Из отданного нагревателем
количества тепла
![]() .
.
часть равная
![]()
было передано холодильнику. В полезную работу удалось преобразовать лишь часть полученной теплоты, равную
![]() .
.
Этим процесс преобразования теплоты в работу отличается от обратного процесса преобразования работы в тепло (механическая работа может превратиться в тепло полностью).
Из полученных выше соотношений для Q0, Q1, Q0-Q1 следует важное выражение
![]() .
(1.35)
.
(1.35)
