
- •Предисловие
- •Программа курса «Молекулярная физика. Термодинамика.»
- •2. Учебно-тематический план
- •3. Содержание курса
- •4. Примерная тематика семинарских занятий
- •5. Средства обеспечения дисциплины
- •Введение
- •Все вещества состоят из атомов или молекул
- •Атомы и молекулы веществ находятся в состоянии беспорядочного движения
- •Между атомами и молекулами вещества действуют как силы притяжения, так и силы отталкивания.
- •Глава 1 Термодинамика
- •§1. Температура и термодинамическое равновесие
- •Давление
- •§2. Уравнение состояния идеального газа
- •§3. Законы идеальных газов
- •Изотермический процесс
- •Изобарический процесс
- •Закон Авогадро
- •Закон Дальтона
- •§4. Первое начало термодинамики
- •§5. Макроскопическая работа
- •I начало термодинамики для системы в адиабатической оболочке
- •§6. Внутренняя энергия
- •§7. Количество теплоты. Математическая формулировка первого начала термодинамики
- •§8. Различные приложения I начала термодинамики. Теплоёмкость
- •§9. Внутренняя энергия идеального газа. Закон Джоуля
- •Уравнение Роберта Майера
- •§10. Адиабатический процесс. Уравнение Пуассона
- •Работа при адиабатическом изменении объёма газа
- •§11. Политропический процесс
- •Вопросы и задания для самостоятельной работы студентов Основы термодинамики. I начало термодинамики
- •§12. II начало термодинамики
- •Различные формулировки основного постулата, выражающего II начало термодинамики
- •§13. Равновесные состояния
- •§14. Обратимые и необратимые процессы
- •Необратимость и вероятность
- •§15. Цикл Карно
- •Коэффициент полезного действия в цикле Карно
- •§16. Холодильная машина
- •§17. Свободная энергия
- •§18. Энтропия
- •§19. Некоторые термодинамические соотношения
- •§20. Закон возрастания энтропии. Второе начало термодинамики
- •Увеличение энтропии при теплопередаче
- •§21. Энтропия и вероятность
- •§22. Энтропия и беспорядок
- •§23. Третье начало термодинамики
- •Вопросы для контроля самостоятельной работы студентов
- •II начало термодинамики. Энтропия.
- •Глава 2. Неравновесная термодинамика §1. Основные принципы линейной термодинамики
- •§2. Нелинейная термодинамика
- •§3. Принцип синергетики
- •Свойства и примеры самоорганизации диссипативных структур
- •Глава 3. Статистическая физика и её применение к идеальному газу
- •§1. Давление газа с точки зрения молекулярно – кинетической теории
- •§2. Температура как мера средней энергии хаотичного движения молекул
- •Скорость газовых молекул
- •§3. Броуновское движение
- •§4. Кинетическая теория теплоты Внутренняя энергия идеального газа
- •§5. Классическая теория теплоёмкости и её недостатки
- •§6. Барометрическая формула
- •Закон Больцмана
- •§7. Распределение молекул по скоростям
- •§8. Функция распределения
- •§9. Формула Максвелла
- •§10. Средняя арифметическая, средняя квадратичная и наивероятнейшая скорости молекул
- •§11. Среднее число молекул, сталкивающихся со стенкой сосуда
- •Вопросы для контроля знаний студентов Молекулярно-кинетическая теория
- •Глава 4. Явления переноса §1. Столкновение молекул и явления переноса
- •§2. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- •§3. Рассеяние молекулярного пучка в газе
- •§4. Явление переноса в газах. Уравнение переноса
- •§5. Диффузия
- •§6. Нестационарная диффузия
- •§7. Теплопроводность газов
- •§8. Вязкость газов (внутреннее трение)
- •§9. Соотношения между коэффициентами переноса
- •§10. Физические явления в разреженных газах
- •Вопросы для самостоятельного контроля знаний студентов Явления переноса
- •Глава 5 §1. Неидеальные газы. Уравнение Ван-дер-Ваальса. Отклонение свойств газов от идеальности
- •Уравнение Ван-Дер-Ваальса
- •§2. Учет сил отталкивания между молекулами
- •§3. Учет сил притяжения между молекулами
- •§4. Изотермы Ван-дер-Ваальса
- •§5. Критическая температура и критическое состояние
- •§6. Недостатки уравнения Ван-дер-Ваальса
- •§7. Внутренняя энергия газа Ван-дер-Ваальса
- •§8. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- •§9. Сжижение газов
- •Эффект Джоуля-Томсона
- •Вопросы для самоконтроля изученного материала Реальные газы
- •Глава 6. Жидкое состояние §1.Строение жидкостей
- •§2. Поверхностное натяжение
- •§3. Условия равновесия на границе двух сред. Краевой угол
- •§4. Граница жидкости и твердого тела
- •§5. Силы, возникающие на кривой поверхности жидкости
- •§6. Капиллярные явления
- •§7. Упругость насыщенного пара над кривой поверхностью жидкости
- •Вопросы для самоконтроля знаний студентов
- •Глава 7. Жидкие растворы §1. Свойства растворов
- •§2. Упругость насыщенного пара над идеальным раствором
- •§3. Закон Генри
- •§4. Осмотическое давление
- •Глава 8. Кристаллическое состояние §1. Отличительные черты кристаллического состояния
- •§2. Классификация кристаллов
- •§3. Физические типы кристаллических решеток
- •§4. Тепловое движение в кристаллах
- •Глава 9. Фазовые переходы §1. Фаза и фазовые равновесия
- •§2. Условия равновесия фаз химически однородного вещества
- •§3. Уравнение Клапейрона
- •Вопросы для самоконтроля знаний студентов
- •Содержание
Вопросы для самоконтроля изученного материала Реальные газы
1. В чем отличие реального газа от идеального? При каких условиях в поведении газов наступает отступление от законов Менделеева-Клапейрона?
2. Каков физический смысл поправок в уравнении Ван-дер-Ваальса? Как они вычисляются: а) из молекулярно-кинетической теории; б) через параметры критического состояния?
3. Как будут располагаться изотермы Ван-дер-Ваальса на графике PV для различных температур? Какой вид будет иметь изотерма Ван-дер-Ваальса: а) для температуры ниже критической; 6) для температуры выше критической?
4. Сравните изотермы Ван-дер-Ваальса с экспериментальными кривыми для одного и того же газа.
5.Какой эффект Джоуля-Томсона называют положительным, какой отрицательным?
6. От каких параметров зависит температура инверсии? Как записать эту зависимость? Каков физический смысл температуры инверсии?
7. Что называют насыщенным паром? Чем определяется давление насыщенного пара?
8. Какой физический смысл имеют величины b, V-b, а/V2, входящие в уравнение Ван-дер-Ваальса?
9. Для двух различных газов, взятых в равных количествах и имеющих одинаковые объемы и температуры, рассчитали давление по уравнению Ван-дер-Ваальса. Результаты сравнили с давлением идеального газа с такими же параметрами. Оказалось, что давление одного газа больше давления идеального газа, другое меньше. Чем объяснить полученные отличия в давлениях?
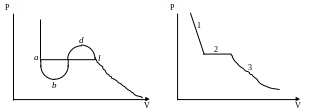 10.Зависимость
давления от объема, полученная при
решении уравнения Ван-дер-Ваальса,
изображена на рис.1, экспериментальная
кривая показана на рис.2. Чем объясняется
различие в графиках?
10.Зависимость
давления от объема, полученная при
решении уравнения Ван-дер-Ваальса,
изображена на рис.1, экспериментальная
кривая показана на рис.2. Чем объясняется
различие в графиках?
Рис.1 Рис.2
12. В каком агрегатном состоянии находится вещество, если его состояние на графике (рис.2) определяется точками 1,2,3?
13.Какому физическому состоянию соответствуют участки ав, вб, dl кривой на рис. 1?
14.Что можно сказать о значениях заштрихованных площадей на рис.1?
15.Как с увеличением температуры вещества меняется ход графиков, приведенных на рис.1?
16.В замкнутом сосуде, содержащем некоторое вещество в двух фазах, поддерживается постоянное давление. Температура постепенно повышается от значения меньшего критического до значения большего критического. Начертите на координатной плоскости VT примерные графики процесса для случаев: а) давление равно критическому; б) давление больше критического; в) давление меньше критического. Считайте, что при температурах больших критической, вещество имеет свойства идеального газа.
17.Чем объясняется, что в процессе дросселирования при комнатной температуре водород нагревается, а кислород охлаждается?
18.Каков в опыте Джоуля-Томсона знак приращения внутренней энергии газа? Энтропии? Тепловой функции? (энтальпии)
19.Начертите экспериментальную изотерму процесса сжатия реального газа и объясните ход графика.
20.Каков смысл коэффициента в уравнении Ван-дер-Ваальса и как он выражается через размеры атомов?
21.Каков смысл коэффициента а в уравнении Ван-дер-Ваальса и как он определяется?
22.Начертите изотерму Ван-дер-Ваальса и укажите, каким состояниям соответствуют различные участки изотермы?
23.Что такое критическая температура?
24.3а счет каких физических факторов сжимаемость реального газа при малом давлении больше, чем идеального, а при большом — меньше?
25.Какие соображения позволяют выбрать давление, при котором должна быть проведена горизонтальная изотерма реального газа, соответствующая двухфазному состоянию?
26.Как наглядно объяснить зависимость знака дифференциального эффекта Джоуля-Томсона от давления газа?
27.Каким физическим условиям в газе соответствует точка инверсии дифференциального эффекта Джоуля-Томсона?
28.Чем свойства пара отличаются от свойств газа? При каких условиях к пару можно применить газовые законы?
29.От каких термодинамических параметров зависит внутренняя энергия газа
Ван-дер-Ваальса?
30.В чем заключается эффект Джоуля-Томсона? Каким уравнением описывается это явление?
31.В чем сущность процесса дросселирования газа? Является ли выпуск сжатого газа в пустоту процессом дросселирования? Как изменяется температура идеального газа при выпуске его в пустоту?
32.В чем заключается явление Джоуля-Томсона? Каким уравнением описывается это явление?
33.Какая температура называется температурой инверсии Джоуль-Томсон эффекта?
34.Какие значения должны иметь величины а и b в уравнении Ван-дер-Ваальса, чтобы газ всегда охлаждался при дросселировании?
35.Какие участки кривой Ван-дер-Ваальса соответствует нестабильным и метастабильным состояниям? Объясните смысл и возможность осуществления этих состояний.
36.Что такое перегретая жидкость? Укажите ее область на изотерме Ван-дер-Ваальса.
37.Что такое дросселирование газа? Почему процесс дросселирования в идеальном газе не сопровождается изменением температуры, а в не идеальном газе сопровождается?
38. Что происходит с газом Ван-дер-Ваальса с поправкой а =0 в опыте Джоуля-Томсона, газ нагревается, охлаждается или температура газа не меняется?
39. Что происходит с газом Ван-дер-Ваальса с поправкой в =0 в опыте Джоуля-Томсона, газ нагревается, охлаждается или температура газа не меняется?
40.Какое значение имеет приращение внутренней энергии газа ΔU в опыте Джоуля-Томсона для случая, когда начальное состояние характеризуется точкой, лежащей па кривой инверсии, - положительное, отрицательное или не изменяется?
41.Как изменяются температуры водорода и кислорода в результате дросселирования при комнатной температуре?
42. Получите приведенное уравнение Ван-дер-Ваальса. В чем его преимущество?
43. Каким выражением определяется критическая температура газа Ван-дер-Ваальса?
44. Каким выражением определяется критический объем газа Ван-дер-Ваальса?
45. Каким выражением определяется критическое давление газа Ван-дер-Ваальса?
46. Какому выражению соответствует связь между давлением, объемом и температурой киломоля газа Ван-дер-Ваальса в критической точке?
48. Найти приращение энтропии ΔS киломоля газа Ван-дер-Ваальса при изотермическом расширении от объема V1 до объема V2. Считать, что поправка Ван-дер-Ваальса в известна.
