
- •1.Электрический заряд и его свойства. Дискретность. Элементарный электрический заряд. Закон сохранения электрического заряда.
- •2.Электрическое поле. Закон Кулона. Диэлектрическая проницаемость.
- •4.Работа в электростатическом поле. Потенциальная энергия поля. Потенциальность поля.
- •5.Потенциал. Разность потенциалов. Связь между напряжением и напряженностью
- •7.Электроемкость. Конденсаторы. Емкость плоского конденсатора. Энергия электрического поля
- •8.Последовательное и параллельное соединение конденсаторов
- •9.Электрический ток. Условия существования эл.Тока. Сила тока и плотность тока
- •10.Закон Ома для участка цепи. Сопротивление. Зависимость сопротивления проводника от температуры
- •11.Последовательное и параллельное сопротивление проводников
- •12.Работа и мощность электрического поля. Закон Джоуля-Ленца
- •13.Электродвижущая сила. Закон Ома для замкнутой цепи
- •14.Магнитное поле. Индукция магнитного поля. Магнитные силовые линии. Взаимодействие параллельных токов
- •15.Проводник с током в магнитном поле
- •16.Сила Лоренца. Движение заряженной частицы в магнитном поле
- •17.Магнитный поток. Явление электромагнитной индукции. Закон электромагнитной индукции и правило Ленца
- •18.Эдс индукции в движущихся проводниках в магнитном поле. Вихревое электрическое поле
- •19.Самоиндукция. Индуктивность. Эдс самоиндукции. Энергия магнитного поля
- •20.Колебательное движение. Гармонические колебания и их характеристики.
- •21.Пружинный и математический маятники. Энергетические превращения при их колебаниях.
- •22.Свободные электромагнитные колебания в колебательном контуре. Энергетические превращения в колебательном контуре. Формула Томпсона
- •23.Вынужденные электрические колебания. Переменный ток и его характеристики
- •24.Получение переменного тока при вращении витка в магнитном поле. Генератор переменного тока.
- •25.Передача и распределение электроэнергии. Устройство и принцип действия трансформатора
- •26.Электромагнитное поле. Электромагнитные волны и их свойства. Принципы радиосвязи. Радиолокация
- •27.Электромагнитная природа света. Скорость света. Зависимость между длиной световой волны и частотой электромагнитных колебаний
- •28.Интерференция света. Когерентность и монохроматичность
- •29.Дифракция света. Дифракционная решетка
- •30.Отражение и преломление света. Полное внутреннее отражение света
- •31.Дисперсия света. Разложение белого света призмой
- •32.Преломление света в линзах
- •33.Экспериментальные основы теории относительности. Постулаты Энштейна. Следствия из постулат
- •34.Зависимость массы от скорости в сто. Закон взаимосвязи массы и энергии
- •35.Гипотеза Планка. Фотон и его свойства. Корпускулярно-волновой дуализм
- •36.Внешний фотоэффект и его законы. Уравнение Энштейна для фотоэффекта
- •37.Опыты Резерфорда. Планетарная модель атома
- •38.Квантовые постулаты Бора. Оптические спектры. Излучение и поглощение энергии атомами. Строение атома водорода по Борну
- •39.Тепловое равновесие. Температура. Тепловое расширение тел. Измерение температуры
- •40. Идеальный газ. Уравнение состояния идеального газа
- •41.Газовые законы. Применение газов в технике
- •42.Внутренняя энергия идеального газа
- •43.Работа в термодинамике – ебала какая-то
- •44.Количество теплоты
- •45.Первое начало термодинамики. Применение 1 начала термодинамики к изопроцессам в идеальных газах
- •46.Второе начало термодинамики. Тепловые двигатели. Кпд тепловых двигателей. Цикл Карно. Максимальный кпд тепловых двигателей
- •47.Основные положения молекулярно-кинетической теории вещества, и их опытное доказательство. Диффузия и броуновское движение
- •48.Размеры и масса молекул. Постоянная Авогадро
- •49.Силы взаимодействия молекул. Особенности внутреннего строения газов, жидкостей и твердых тел
- •50.Давление газа. Основное уравнение молекулярно-кинетической теории
- •51.Насыщенный пар и его свойства. Кипение жидкости
- •52.Влажность воздуха. Абсолютная и относительная влажность. Приборы для измерения влажности
- •53.Поверхностное натяжение. Смачивание. Капиллярные явления
- •54.Характеристики твердого состояния вещества. Кристаллы. Строение и свойства кристаллических веществ. Аморфные тела
- •55.Деформация. Виды деформации. Механическое напряжение. Закон Гука. Диаграмма напряжений и ее характеристики
- •56.Электрический ток в полупроводниках. Собственная и примесная проводимости. Электронно-дырочный переход. Полупроводниковый переход
- •57.Электрический ток в электролитах. Законы Фарадея
- •58.Электрический ток в газах. Самостоятельный и несамостоятельный разряды. Различные типы самостоятельного разряда и их техническое применение
- •59.Электрический ток в вакууме. Электронные лампы
- •60.Магнитная проницаемость вещества. Три класса магнитных веществ
- •61.Радиоактивность. Альфа- бета- и гамма распады. Закон радиоактивного распада
- •62.Биологическое действие радиоактивного излучения
- •63.Состав атомного ядра. Масса и энергия атомных ядер. Ядерные силы
- •64.Ядерные реакции. Энергетический выход ядерных реакций
- •65.Деление тяжелых атомных ядер. Ядерные реакторы. Ядерная энергетика и экологические проблемы
38.Квантовые постулаты Бора. Оптические спектры. Излучение и поглощение энергии атомами. Строение атома водорода по Борну
Постулаты Бора показали, что атомы "живут" по законам микромира.
I постулат - постулат стационарных состояний:
В атоме существуют стационарные квантовые состояния, не изменяющиеся с течением времени без внешнего воздействия на атом.
В этих состояниях атом не излучает электромагнитных волн, хотя и движется с ускорением.
Каждому стационарному состоянию атома соответствует определенная энергия атома.
Стационарным состояниям соответствуют стационарные орбиты, по которым движутся электроны.
II постулат - правило частот:
При переходе атома из одного стационарного состояния в другое излучается или поглощается 1 фотон.
а) Атом излучает 1 фотон(который несет 1 квант энергии), когда электрон переходит из состояния с большей энергией (Е k) в состояние с меньшей энергией (Е n).
Энергия
излученного фотона:
![]()
Здесь (Ek - En) - разность энергий стационарных состояний.
При Ек > Eп происходит излучение фотона.
Частота излучения:
![]()
где k и n - номера стационарных состоянии, или главные квантовые числа.
б) Атом поглощает 1 фотон, когда переходит из стационарного состояния с меньшей энергией (E n) в стационарное состояние с большей энергией (E k).
При Ек < Еn происходит поглощение фотона.
После экспериментальных проверок правильности модели атома Резерфорда и принятия постулатов Бора ученым пришлось признать ограниченность применения законов классической физики для микроскопических тел.
Модель атома водорода по Бору
Свои постулаты Н. Бор применил для построения теории строения простейшего атома (атома водорода).
Согласно этой теории Бор смог вычислить для атома водорода:
- возможные радиусы орбит электрона и размеры атома
- энергии стационарных состояний атома
- частоты излучаемых и поглощаемых электромагнитных волн.
Распределение энергетических уровней при излучении (испускании) и поглощении атомом водорода электромагнитных волн:
При (n = 1) - основное энергетическое состояние, ему соответствует радиус орбиты электрона r = 0,5 • 10 -11 м.
При (n больше 1) - возбужденные состояния.
При поглощении атомом кванта энергии (фотона) атом переходит в возбужденное состояние, при этом электрон переходит на более отдаленную орбиту и его связь с ядром слабеет.
Переходы в первое возбужденное состояние (Е2) с верхних уровней соответствует частотам видимой части (кр з с с) спектра водорода.
Линечатый спектр атома водорода состоит из линий, сгруппированных в серии.
Частоты каждой серии спектра можно подсчитать по формуле Бальмера-Ритберга:
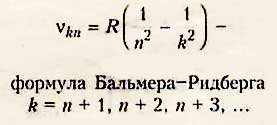
В спектре водорода обнаружены следующие серии:
n = I - серия Лаймана - ультрафиолетовое излучение
n = 2 - серия Бальмера - видимое излучение
n = 3 - серия Пашена - инфракрасное излучение и т.д.
Однако, надо помнить, что для атомов с большим числом электронов ( больше 1) расчеты по теории Бора неприменимы.
