
- •Технологический колледж сервиса
- •Основы техники работы в лаборатории, безопасность проведения эксперимента.
- •1.2 Характеристика основных видов посуды и правил работы с весоизмерительным оборудованием.
- •1.3. Сущность методов и результаты определения плотности потребительских товаров.
- •1.4. Сущность метода и особенности работы с рефрактометром
- •2. Определение кислотности хлеба.
- •1.6 Сущность метода и результаты определения влажности потребительских товаров.
- •2.Изучение ассортимента товаров, реализуемых в ооо дикси-челябинск
- •2.1. Ознакомление с торговым предприятием и организацией торговли
- •2.2. Изучение ассортимента выбранной группы товаров, реализуемых ооо дикси-челябинск
- •3. «Изучение потребительских предпочтений выбранной группы товаров».
- •3.2.0Бработка полученных данных исследования, анализ и использование результатов исследований для формирования выводов и
- •Товароведение, экспертиза и стандартизация ( автор: Волошко н.И.)
1.3. Сущность методов и результаты определения плотности потребительских товаров.
Плотность — количество массы данного вещества в единице объема. При анализе измеряют относительную плотность, которая определяется по формуле
d= , где
, где
d - Относительная плотность исследуемого вещества
р - плотность вещества, кг\м3
р0 - Плотность стандартного вещества, кг\м3
В качестве стандартного вещества — дистиллированная вода.
Относительную плотность определяют с помощью ареометрического и
пикнометрического методов анализа
Показатели плотности характеризуются основными свойствами материала: гигроскопичность, устойчивость к разным нагрузкам, степень истираемости. Плотность молока имеет важное значение при оценке его качества, так как характеризует соотношение всех находящихся в нем компонентов. Сухие обезжиренные вещества повышают плотность, а жир снижает. При разведении молока водой плотность его уменьшается на 0,003 единицы на каждый 10% добавленной воды.
Натуральное целое молоко коровье имеет плотность при 20С в пределах от 1,027 кг\м3 до 1,034 кг\м3, а в среднем для сборного коровьего молока она принята за постоянную величину - 1,034 кг\м3.
Пикнометрический метод анализа.
Сущность пикнометрического метода анализа заключается в определении массы равных объемов исследуемого продукта и воды при t=20°C. относительная плотность исследуемой жидкости вычисляется по формуле
d20=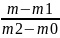 где m2
-
m0
где m2
-
m0
d20 - Относительная плотность исследуемого вещества при 20°С;
m- масса пустого пикнометра, используемого для исследуемой жидкости,
m1- масса пикнометра с исследуемой жидкостью, г;
m0-масса пустого пикнометра, используемого для дистиллированной воды, г;
m2 - масса пикнометра с дистиллированной водой, г При пикнометрировании следует обратить внимание на точное поддержание t=20°C, на тщательность обтирания пикнометра перед взвешиванием и на точность доведения объема жидкости в пикнометре до метки. Ареометрический метод. Сущность метода. Простота и быстрота. По точности уступает пикнометрическому методу. Ареометры предназначенные для определенного вида жидкости — денсиметры. Так лактоденсиметр — для определения относительной плотности молока. При исследовании прозрачных жидких продуктов отсчет производят по нижнему мениску, а при исследовании непрозрачных — по верхнему мениску. Таблица 2— Результаты определения плотности исследуемого продукта
Наименование исследуемого образца |
Значение показателя плотности |
|
ареометрический метод, кг\м3 |
пикнометрический метод, кг\м3 |
|
молоко |
1,038 кг\м3 |
1,032кг\м3 |
d20=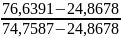 =
=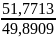 =
1,038
=
1,038
Данный метод отличается простотой и быстротой определения. Однако по точности он уступает пикнометрическому методу. При исследовании прозрачных жидких продуктов отсчет производят по нижнему мениску, а при исследовании непрозрачных — по верхнему мениску.
1.4. Сущность метода и особенности работы с рефрактометром
Рефракция — это преломление или изменение направления луча, которая имеет место при переходе из одной среды в другую, более или менее плотную. Падающий и преломленный луч всегда лежат в одной плоскости.
Угол преломления - это угол, образованный направлением преломленного луча ОВ и продолжением той же нормали.
Рефрактометрия основана на измерении относительных показателей преломления веществ, под которыми понимают отношение скорости света в воздухе Св и в данной среде Сс то есть т]=Св/Сс
Прохождение через какую-либо среду свет, как электромагнитное излучение взаимодействует с молекулами и атомами веществ и изменяет свою скорость. Каждая среда имеет постоянный показатель преломления, который зависит от строения, состава, плотности, степени дисперсии среды. Небольшую скорость световой луч имеет в вакууме (С°=3* 10s м/с)
Если угол падения максимально приближен к 90°, то соответствующий ему угол преломления будет предельным.
Рефрактометром называют приборы, служащие для определения коэффициентов рефракции жидких веществ и растворов. Они имеют две призмы — измерительную и осветительную, между которыми помещают исследуемое вещество. Измерительная призма изготовлена из оптического стекла с высоким показателем преломления. Одна из ее граней служит границей раздела, где происходит преломление светового луча.
Рефрактометр имеет двойную шкалу — одна - показатели преломления, вторая — соответствующее этим показателям процентное содержание сухих веществ.
Показатели снимаются с помощью визира, видимого в окуляр и имеющего вид крестообразно скрещивающихся линий, ограниченных окружностью.
Порядок работы с рефрактометром. Перед началом работы необходимо проверить установку 0- пункта рефрактометра. Установку пункта и измерения на рефрактометре необходимо проводить при одной и той же температуре.
Проверка и установку 0-пункта проводится по дистиллированной воде ( при этом показатель преломления должен быть равен 1,33299 и содержание сухих веществ -0% следующим образом:
-промыть поверхность призм дистиллированной водой и протереть насухо салфеткой;
-оплавленным концом стеклянной палочки нанести на плоскость измерительной призмы 1— 2 капли жидкости и закрыть верхнюю камеру; -свет от осветителя направить в окно верхней камеры (если растворы мутные или темноокрашенные - в окно нижней камеры)
-вращая барабан ввести в поле зрения границу светотени при необходимости удалить дисперсию (окрашенность границы светотени) с помощью рукоятки компенсатора дисперсии; добиться максимальной контрастности границы предельного луча;
-границу светотени подвести к центру перекрестия и снять показания со шкалы (показатель преломления и процент сухих веществ).
Таким путем производят не менее трех отсчетов. Окончательным результатом является среднее арифметическое из всех произведенных отсчетов. В процессе определения необходимо следить за показаниями термометра. Если температура окажется выше или ниже 20 ОС , то необходимо ввести температурные поправки.
Измерения показателей преломления и процента сухих веществ для
анализируемых растворов проводят по аналогичной схеме. Одним из существенных критериев эффективности косметических кремов для кожи является их увлажняющее свойство. Наиболее доступным сырьевым компонентом косметических кремов, способствующих увлажнению и смягчению кожи, является глицерин. Глицерин используют только для производства кремов типа масло/вода (вода, содержащая капельки жира) или смешанных. Однако повышенное содержание глицерина в косметических кремах является нежелательным, так как свидетельствует о повышенном содержании спирта в изделии. Спирт используют в качестве растворителя глицерина и он в свою очередь оказывает неблагоприятное воздействие на кожу человека. Поэтому массовая доля глицерина в косметических кремах нормируется в строгих пределах. Вода является неотъемлемой частью косметических кремов, ее концентрация и способ распределения определяет тип эмульсии косметического крема. Массовая доля влаги нормируется в строгих пределах, поскольку определяет не только качество, но сохраняемость косметического изделия. Одним из методов, позволяющих определить концентрацию глицерина и
массовую долю влаги в косметических товарах является рефрактометрия.
Таблица 3 — результаты оценки показателей качества косметических кремов.
Наименование показателя |
Значение показателя, % |
|
действительное |
нормируемое |
|
Массовая доля влаги |
87% |
- |
Массовая доля глицерина |
15% |
- |
Жир преломляет свет в разной степени в зависимости от его жирнокислотоного состава. Показатель преломления жирных кислот, входящих в состав глицеридов, является важной качественной характеристикой. Рост длины цепи, увеличение количества двойных связей приводят к заметному увеличению показателя преломления. По величине показателя преломления можно судить о природе масла, его чистоте и степени окисления. Преломляющая способность жиров возрастает с увеличением молекулярной массы, а также непредельности жирных кислот. В окисленных маслах числовое значение показателя преломления выше по сравнению со свежими.
1.5.Сущноеть метода и результаты определения титруемой кислотности
потребительских товаров
Титреметрия — количественный аналитический метод, заключающийся в определении концентрации определенного вещества путем постепенного добавления к анализируемому раствору реактива (R) известной концентрации до полного завершения реакции с определяемым веществом (X).
Процесс прибавления титрированного раствора R к раствору X называется титрированием.
Титреметрический метод анализа складывается из следующих этапов:
1. Отбор проб проводят после предварительного осмотра партии товаров с соблюдением определенных условий, гарантирующих соответствие качества образца качеству всей партии.
2. Подготовка пробы в зависимости от характера и консистенции исследуемых продуктов может заключаться в:
приготовление вытяжки (экстракция органическими растворителями кислот исследуемой пробы, при этом повышать скорость и полноту экстракции можно воздействуя температурным фактором);
разбавление пробы дистиллированной водой (понижение концентрации кислот и изменение консистенции продукта с целью повышения точности 1 эксперимента);
осветление окрашенных растворов (удаление солями тяжелых металлов веществ, мешающих проведению эксперимента);
удаление углекислоты (воздействие на пробу температурным фактором с целью предотвращения преждевременного обесцвечивания индикатора, при этом не допускаются удаление летучих кислот) и др.;
3. Проведение химической реакции. На определенный компонент пробы X воздействуют реагентом R, в результате чего образуется продукт реакции Р.
X+R ->Р
На данном этапе следует создать такие условия, при которых определяемое вещество полностью превращается в продукт реакции Р, т.е. чтобы реагент R не давал побочных продуктов реакции.
При этом важно располагать способом установления аналитического сигнала (точки эквивалентности). Методы установления точки эквивалентности можно разделить на 2 группы:
индикаторные;
физико-химические (потенциометрические, амперометрические, кулонометрические и т.д.).
Индикаторы представляют собой химические соединения, которые дают какой — либо внешний эффект при концентрации реагирующих веществ, соответствующих точке эквивалентности.
Этот внешний эффект может состоять в изменении, возникновении или исчезновении окраски, образовании или растворении мало растворимого соединения (осадка).
Физико-химические методы установления аналитического сигнала основаны на изменении, какого — либо физического параметра системы при прибавлении к ней титранта. Для определения аналитического сигнала используются соответствующие приборы (потенциометры, кондуктометры, вольтамперметры и т.д.).
Титреметрический метод анализа находит широкое применение в оценке качества потребительских товаров. Данный метод позволяет определить кислотность, щелочность продукции, содержание поваренной соли. Титреметрия — составная часть методик определения содержания углеводов, витаминов, тяжелых металлов.
Изучение методов определения кислотности / щелочности потребительских товаров.
При исследовании потребительских товаров кислотность/щелочность как показатель качества имеет большое значение. Для пищевых продуктов она обуславливает не только их вкусовые свойства, но и является показателем свежести и доброкачественности. Для непродовольственных товаров данный показатель свидетельствует об их безвредности для организма человека (воздействие парфюмерно-косметических изделий на кожу), а также определяет характер их воздействия на соприкасающиеся с ними материала (разрушающее воздействие моющих средств на текстильные материалы). Кислотность/щелочность зависит от природы и качества сырья, рецептуры, технологического режима производства изделия, а также способов и сроков его хранения.
При оценке качества потребительских товаров различают показатели активной и титруемой кислотности.
Активная кислотность характеризуется концентрацией свободных ионов водорода в растворе и выражается в условных единицах рН.
Титруемой кислотностью называют количество свободных органических кислот и их кислых солей, содержащихся в исследуемом продукте и определяемых титрованием раствором едкой щелочи.
Щелочностью называют количество свободной и связанной щелочи,
содержащейся в исследуемом продукте и определяемой титрованием раствором кислоты. Титруемая кислотность выражается в различных единицах измерения. Это объясняется тем, что в некоторых пищевых продуктах при титровании нейтрализуются не только свободные кислоты, но и кислые соли, занимающие иногда большой удельный вес среди свободных кислот продукта. Но для некоторых пищевых продуктов титруемую кислотность выражают по той кислоте, которая преобладает. В таких случаях кислотность выражают в процентах на преобладающую кислоту. Для пищевых продуктов, в которых нельзя отдать предпочтение какой-либо одной кислоте (жир, хлеб, молочные продукты, пиво), кислотность выражается в условных единицах - градусах» причем в отдельных продуктах градусы кислотности имеют различное значение.
Щелочность, как правило, выражают в %.
Несмотря на то, что активная кислотность является показателем истинои кислотности, качество многих продуктов регламентируется по показателю титруемой кислотности.
Определение кислотности (щелочности) методом титрования основано способности щелочи (кислоты) количественно нейтрализовать находящиеся в исследуемом растворе свободные кислоты (щелочи) и их кислые соли.
[Н*] [ОН*] = 10 -7или рН =|7
При этом учитывают что растворы, имеющие одинаковую нормальность реагируют между собой в эквивалентных количествах.
При определении данного показателя качества продуктов в большинстве случаев в качестве индикатора применяют фенолфталеин и тимолфталеин (для бесцветных растворов).
Таблица 4 - Интервал перехода окраски наиболее часто встречающихся индикаторов.
Индикаторы |
Окраска в среде |
Интервал, рН |
|
|
кислой |
щелочной |
|
Тимоловый синий |
Красная |
Желтая |
1,2...2,8 |
Метиловый желтый |
Красная |
Желтая |
2,9...4,0 |
Метиловый оранжевый |
Красная |
Оранжево-Желтая |
3,1...4,4 |
Метиловый красный |
Красная |
Желтая |
4,4...6,2 |
Бромтимоловый синий |
Желтая |
Синяя |
6,0...7,6 |
Тимолфталеин |
Бесцветная |
Синяя |
9,4... 10,6 |
Фенолфталеин |
Бесцветная |
Красно-Фиолетовая |
8,0...9,8 |
Феноловый красный |
Желтая |
Красная |
6,4...8,0 |
Метод определения титруемой кислотности потребительских товаров.
1. Определение кислотности молока.
Кислотность является основным показателем, по которому определяют свежесть молока. Кислотность свежего молока зависит от наличия в нем белков, кислых, фосфорнокислых и молочно - кислых солей, лимонной и молочной кислоты. Кислотность молока принято выражать в единицах титруемой кислотности - градусах Тернера (количеством 0,1н раствора едкой щелочи, необходимое для нейтрализации кислот, находящихся в 100 мл или граммах продукта) и активной величины рН при 20°С. Реализуемое молоко должно иметь титруемую кислотность не более 2 ЮТ, активная кислотность колеблется от 6,55 до 6,75. При хранении кислотность возрастает в следствие накопления молочной кислоты.
Сущность метода. Метод основан на нейтрализации свободных кислот, кислых солей и свободных кислых групп белков раствором едкого натра или едкого кали с использованием индикатора фенолфталеина.
Порядок проведения работы. В коническую колбу вместимостью
100 150 мл отмеривают пипеткой 10 мл хорошо перемешанного молока,
прибавляют 20 мл дистиллированной воды и 3 капли фенолфталеина, смесь тщательно перемешивают и титруют 0,1н раствором едкого натра (едкого кали) до появления слабо — розовой окраски, соответствующей окраске контрольного образца (эталона) и не исчезающей в течение минуты, при этом отмечают количество NaOH, прошедшее на титрование.
Обработка результатов. Кислотность молока (X) в градусах Тернера определяется по формуле:
Х = а*К*10, где
а — количество 0,1н раствором едкого натра (едкого кали) затраченный на титрование, мл
К - поправку к титру 0,1 н раствор едкого натра (едкого кали);
10 - коэффициент пересчета на 100 мл молока
a=10,6*1*10=106
Расхождение между параллельными определениями не должно быть более 1 Т. За результат анализа принимают среднее арифметического двух параллельных определений.
Этот метод может использоваться и для исследования других продуктов, например хлеба.
