- •Кинематика колебательного движения.
- •Тема 1.7.Механические волны–процесс распространения механических колебаний в среде (жидкой,твердой,газообразной).
- •Раздел 2. Основы молекулярной физики и термодинамики
- •Тема 2.2. Основные законы термодинамики.
- •Раздел 3. Электродинамика
- •Тема 3.1.Электростатика-раздел теории электричества, в котором изучается взаимодействие неподвижных электрических зарядов.
- •Тема 3.2. Постоянный электрический ток.Электрический ток - упорядоченное движение заряженных частиц под действием сил электрического поля или сторонних сил.
- •Эдс индукции
- •Тема 3.3. Магнитное поле в вакууме
Тема 2.2. Основные законы термодинамики.
Внутренняя
энергия идеального газа—это
сумма энергий молекулярных взаимодействий
и тепловых движений молекулы. Внутренняя
энергия является однозначной функцией
состояния системы.
![]() ,
, ![]() .
.
Внутренняя энергия на один моль идеального газа
![]()
Работа в термодинамике–это изменение внутренней энергии системы, связанное с изменением ее объема и расположения ее частей относительно друг друга.
|
или в пределе при ΔVi → 0:
|
Коли́чество теплоты́ — энергия, которую получает или теряет тело при теплопередаче. Количество теплоты является одной из основных термодинамических величин.
Количество
теплоты является функцией процесса,
а не функцией состояния,
то есть количество теплоты, полученное
системой, зависит от способа, которым
она была приведена в текущее состояние.
Количеством теплоты,
сообщённой телу
![]() в
некотором процессе, будем называть
величину
в
некотором процессе, будем называть
величину
![]() ,
где
,
где
![]() —
изменение внутренней
энергии
тела
—
изменение внутренней
энергии
тела
![]() .
.
Физическая величина, численно равная количеству теплоты, которое необходимо сообщаить для нагревания данного тела на один кельвин называется теплоемкостью тела
Удельная
теплоемкость—физическая
величина, равная количеству теплоты,
которое необходимо сообщить единице
массы вещества для нагревания её на
один кельвин
![]() Дж/(кг*К)
Дж/(кг*К)
Молярная теплоемкость равна количеству теплоты, которое необходимо сообщить одному молю вещества для нагревания его на один кельвин Дж/(моль*К)
Связь
молярной и удельной теплоемкостями .
.
Теплоемкость тела зависит от условий его нагревания.
Первое начало термодинамики- количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы против внешних сил.
1-е
начало термодинамики: Количество
теплоты, сообщенное системе, расходуется
на изменение внутренней энергии системы
и на совершение системой работы против
внешних сил
 .
.
Если
система получает тепло извне, то
 ,
если отдает, то
,
если отдает, то
 .
Если работу совершает система, то
.
Если работу совершает система, то
 ,
если работу совершают внешние силы, то
,
если работу совершают внешние силы, то
 .
.
Первое
начало можно записать для малого
изменения состояния системы (для
элементарного процесса)
 ,
где
,
где
 - элементарное количество тепла,
- элементарное количество тепла,
 - элементарная работа,
- элементарная работа,
 - приращение внутренней энергии.
- полный дифференциал, т.к. при совершении
любого процесса, в результате которого
система возвращается в исходное
состояние, изменение ее внутренней
энергии равно нулю
- приращение внутренней энергии.
- полный дифференциал, т.к. при совершении
любого процесса, в результате которого
система возвращается в исходное
состояние, изменение ее внутренней
энергии равно нулю
 .
Теплота и работа таким свойством не
обладают, поэтому
и
не являются полными дифференциалами.
.
Теплота и работа таким свойством не
обладают, поэтому
и
не являются полными дифференциалами.

Изохорный
процесс
 .
вся теплота, сообщаемая газу, идет на
изменение его внутренней энергии
.
вся теплота, сообщаемая газу, идет на
изменение его внутренней энергии
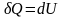 или
или
Изобарный
процесс
 .Осуществляется
при нагревании или охлаждении газа в
цилиндре с подвижным поршнем, на который
действует постоянное внешнее давление.
Элементарное количество теплоты,
сообщаемое газу в изобарном процессе
.Осуществляется
при нагревании или охлаждении газа в
цилиндре с подвижным поршнем, на который
действует постоянное внешнее давление.
Элементарное количество теплоты,
сообщаемое газу в изобарном процессе

Первое начало термодинамики для изобарного процесса
Изотермический
процесс
 .
.
 ,
,
Т. е. все тепло, подведенное к газу, идет только на совершение им работы, так как изменение внутренней энергии, ввиду постоянства температуры, равно нулю
Адиабатным называется процесс, при котором отсутствует теплообмен между термодинамической системой и окружающей средой.
Условие
адиабатного процесса

Из
1-го начала термодинамики следует
 . Это значит, что работа совершается
системой за счет убыли ее внутренней
энергии.
. Это значит, что работа совершается
системой за счет убыли ее внутренней
энергии.
Круговой процесс (цикл)-процесс, при котором система, проходя через ряд состояний, возвращается в первоначальное.
Тепловые двигатели—устройство, совершающее работу за счет использования внутренней энергии топлива,тепловаямашина,превращающая тепло в механическую энергию использует зависимость теплового расширения вещества от температуры. Действие теплового двигателя подчиняется законам термодинамики. Для работы необходимо создать разность давлений по обе стороны поршня двигателя или лопастей турбины. Для работы двигателя обязательно наличие топлива.Это возможно при нагревании рабочего тела (газа),который совершает работу за счёт изменения своей внутренней энергии. Повышение и понижение температуры осуществляется, соответственно, нагревателем и охладителем.
Цикл Карно-идеальный термодинамический цикл. Одним из важных свойств цикла Карно является его обратимость: он может быть проведён как в прямом, так и в обратном направлении, при этом энтропия адиабатически изолированной (без теплообмена с окружающей средой) системы не меняется.
Тепловая машина Карно,работающая по этому циклу,обладает максимальным КПД из всех машин,у которых максимальная и минимальная температуры осуществляемого цикла совпадают соответственно с максимальной и минимальной температурами цикла Карно. Состоит из 2 адиабатических и 2 изотермических процессов.КПД реального и идеального тепловых двигателей-
![]() КПД
реального теплового
двигателя.
КПД
реального теплового
двигателя.
![]() КПД идеального теплового
двигателя (максимально возможный)
КПД идеального теплового
двигателя (максимально возможный)
Второе
начало термодинамики-невозможен
самопроизвольный. Переход тепла от
тела менее нагретого к телу более
нагретого.
закон
возрастания энтропии замкнутой
системы при необратимых процессах:
любой
необратимый процесс в замкнутой системе
происходит так, что энтропия системы
при этом возрастает. приведенное
количество тепла – это отношение
количества тепла
,
полученного термодинамической системой
от какого-либо тела (нагревателя), к
температуре этого тела
 .
.
 .
.
Энтропия- понятие,впервые введенное в термодинамике для определения меры необратимого рассеяния энергии. Величины и имеют один и тот же знак, поэтому по характеру изменения энтропии можно судить о направлении процесса теплообмена: при нагревании системы ее энтропия возрастает, при охлаждении – убывает.
Поскольку
величина
 является полным дифференциалом,
изменение энтропии при всяком обратимом,
но не круговом процессе, не зависит от
вида процесса, а зависит только от
начального и конечного состояний
системы. Следовательно, энтропия –
функция состояния.
является полным дифференциалом,
изменение энтропии при всяком обратимом,
но не круговом процессе, не зависит от
вида процесса, а зависит только от
начального и конечного состояний
системы. Следовательно, энтропия –
функция состояния. ,
,
где
 - приращение энтропии.
- приращение энтропии.
 -энтропия
идеального газа
-энтропия
идеального газа
Статистическое толкование второго начала термодинамики-в статистической теории энтропия получает очень точное математическое выражение как логарифм вероятности. Этот логарифм можно рассчитать теоретически, если у нас есть данная физическая модель. Затем расчетную величину можно сравнить с экспериментальной.
Третье начало термодинамики-—физический принцип, определяющий поведение энтропии при приближениитемпературы к абсолютному нулю. Является одним из постулатов термодинамики,принимаемым на основе обобщения значительного количества экспериментальных данных. для любого обратимого цикла приведенное количество тепла, сообщаемое системе на всех участках цикла, равно нулю