
- •Глава 8. Физико-химические методы очистки сточных вод
- •8.1. Коагуляция и флокуляция
- •8.2. Флотация
- •8.3. Адсорбция
- •8.4. Ионный обмен
- •8.5. Экстракция
- •8.6. Обратный осмос и ультрафильтрация
- •8.7. Десорбция, дезодорация и дегазация
- •8.8. Электрохимические методы
- •Глава 9. Химические методы очистки сточных вод
- •9.1. Нейтрализация
- •9.2.Окисление и восстановление
- •9.3. Удаление ионов тяжелых металлов
- •Глава 10. Биохимические методы очистки сточных вод
- •10.1. Общие положения
- •10.2. Закономерности распада органических веществ
- •10.3. Влияние различных факторов на скорость биохимического окисления
- •10.4. Очистка в природных условиях
- •10.5. Очистка в искусственных сооружениях
- •10.6. Анаэробные методы биохимической очистки
- •10.7. Обработка осадков
- •10.8. Рекуперация активного ила
- •Глава 11. Термические методы очистки сточных вод
- •11.1. Концентрирование сточных вод
- •11.2. Выделение веществ из концентрированных растворов
- •11.3. Термоокислительные методы обезвреживания
Глава 8. Физико-химические методы очистки сточных вод
К физико-химическим методам очистки сточных вод относят коагуляцию, флотацию, адсорбцию, ионный обмен, экстракцию, ректификацию, выпаривание, дистилляцию, обратный осмос и ультрафильтрацию, кристаллизацию, десорбцию и др. Эти методы используют для удаления из сточных вод тонкодисперсных взвешенных частиц (твердых и жидких), растворимых газов, минеральных и органических веществ.
Использование физико-химических методов для очистки сточных вод по сравнению с биохимическими имеют ряд преимуществ: 1) возможность удаления из сточных вод токсичных биохимически неокисляемых органических загрязнений; 2) достижение более глубокой и стабильной степени очистки; 3) меньшие размеры сооружении; 4) меньшая чувствительность к изменениям нагрузок; 5) возможность полной автоматизации; 6) более глубокая изученность кинетики некоторых процессов, а также вопросов моделирования, математического описания и оптимизации, что важно для правильного выбора и расчета аппаратуры; 7) методы не связаны с контролем за деятельностью живых организмов; 8) возможность рекуперации различных веществ.
Выбор того или иного метода очистки (или нескольких методов) производят с учетом санитарных и технологических требований, предъявляемых к очищенным производственным сточным водам с целью дальнейшего их использования, а также с учетом количества сточных вод и концентрации загрязнений в них, наличия необходимых материальных и энергетических ресурсов и экономичности процесса.
8.1. Коагуляция и флокуляция
Коагуляция. Это процесс укрупнения дисперсных частиц в результате их взаимодействия и объединения в агрегаты. В очистке сточных вод ее применяют для ускорения процесса осаждение тонкодисперсных примесей и эмульгированных веществ. Коагуляция наиболее эффективна для удаления из воды коллоидно-дисперсных частиц, т. е. частиц размером 3—100 мкм. Коагуляция может происходить самопроизвольно или под влиянием химических и физических процессов. В процессах очистки сточных вод коагуляция происходит под влиянием добавляемых к ним специальных веществ — коагулянтов. Коагулянты в воде образуют хлопья гидроксидов металлов, которые быстро оседают под действием силы тяжести. Хлопья обладают способностью улавливать коллоидные и взвешенные частицы и агрегировать их. Так как коллоидные частицы имеют слабый отрицательный заряд, а хлопья коагулянтов слабый положительный заряд, то между ними возникает взаимное притяжение.
Для коллоидных частиц характерно образование на поверхности частиц двойного электрического слоя. Одна часть двойного слоя фиксирована на поверхности раздела фаз, а другая создает облако ионов, т. е. одна часть двойного слоя является неподвижной, а другая подвижной (диффузный слой). Разность потенциалов, возникающая между неподвижной и подвижной частями слоя (в объеме жидкости), называется дзета-потенциалом ξ или электрокинетическим потенциалом, отличным от термодинамического потенциала Е, который представляет собой разность потенциалов между поверхностью частиц и жидкостью. Дзета-потенциал зависит как от Е, так и от толщины двойного слоя. Его значение определяет величину электростатических сил отталкивания частиц, которые предохраняют частицы от слипания друг с другом. Малый размер коллоидных частиц загрязнений и отрицательный заряд, распределенный на поверхности этих частиц, обусловливает высокую стабильность коллоидной системы.
Чтобы вызвать коагуляцию коллоидных частиц, необходимо снизить величину их дзета-потенциала до критического значения добавлением ионов, имеющих положительный заряд. Таким образом, при коагуляции происходит дестабилизация коллоидных частиц вследствие нейтрализации их электрического заряда. Эффект коагуляции зависит от валентности иона коагулянта, несущего заряд, противоположный знаку заряда частицы. Чем выше валентность, тем более эффективно коагулирующее действие.
Для начала коагуляции частицы должны приблизиться друг к другу на расстояние, при котором между ними действуют силы притяжения и химического сродства. Сближение частиц происходит в результате броуновского движения, а также при ламинарном или турбулентном движении потока воды. Коагулирующее действие солей есть результат гидролиза, который проходит вслед за растворением.
Процесс гидролиза коагулянтов и образования хлопьев происходит по следующим стадиям:
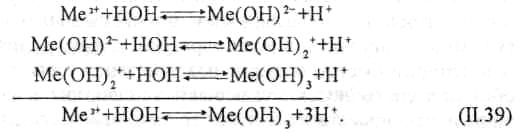
В действительности процесс гидролиза протекает значительно сложнее. Ион металла образует ряд промежуточных соединений в результате реакций с гидроксид-ионами и полимеризации. Образующиеся соединения имеют положительный заряд и легко адсорбируются отрицательно заряженными коллоидными частицами.
В качестве коагулянтов обычно используют соли алюминия, железа или их смеси. Выбор коагулянта зависит от его состава, физико-химических свойств и стоимости, концентрации примесей в воде, от рН и солевого состава воды.
В качестве коагулянтов используют сульфат алюминия A12(SO4)318H2O; алюминат натрия NaA1О2; гидроксохлорид алюминия А12(ОН)5С1; тетраоксосульфаты алюминия-калия и алюминия-аммония [квасцы — алюмокалевые KA1(SO4)2 12H2O и аммиачные NH4A1(SO4)212H2O]. Из них наиболее распространен сульфат алюминия, который эффективен в интервале значений рН=5-7,5. Он хорошо растворим в воде и имеет относительно низкую стоимость. Его применяют в сухом виде или в виде 50%-го раствора. При коагулировании сульфата алюминия он взаимодействует с гидрокарбонатами, имеющимися в воде:
![]()
![]() Алюминат
натрия применяют в сухом виде или в виде
45%-го раствора. Он является щелочным
реагентом, при рН=9,3-9,8 образует
быстроосаждающиеся хлопья. Для
нейтрализации избыточной щелочности
можно использовать кислоты или дымовые
газы, содержащие СO2:
Алюминат
натрия применяют в сухом виде или в виде
45%-го раствора. Он является щелочным
реагентом, при рН=9,3-9,8 образует
быстроосаждающиеся хлопья. Для
нейтрализации избыточной щелочности
можно использовать кислоты или дымовые
газы, содержащие СO2:
![]() В
большинстве случаев используют смесь
NaA1O2+Al(SO4)3
в соотношении (10 : 1) — (20:1):
В
большинстве случаев используют смесь
NaA1O2+Al(SO4)3
в соотношении (10 : 1) — (20:1):
Совместное употребление этих солей дает возможность повысить эффект осветления, увеличить плотность и скорость осаждения хлопьев, расширить оптимальную область рН среды.
Оксихлорид алюминия обладает меньшей кислотностью и поэтому пригоден для очистки слабощелочных вод; ввиду высокого содержания в нем водорастворимого алюминия ускоряется хлопьеобразование и осаждение коагулированной взвеси, например, по реакции:
2А12(ОН)5С1+Са(НСО3)2 → 4А1(ОН)3+СаС12+2СО2. (II.42)
Из солей железа в качестве коагулянтов используют сульфаты железа Fe2(SO4)3*2H2O, Fe2(SO4)3*3H2O и FeSO4*7H2O, a также хлорное железо FeCl3. Наибольшее осветление происходит при использовании солей трехвалентного железа. Хлорное железо применяют в сухом виде или в виде 10-15%-х растворов. Сульфаты используют в виде порошков. Доза коагулянта зависит от рН сточных вод. Для Fe3+ рН равен 6-9, а для Fe2+ рН 9,5 и выше. Для подщелачивания сточных вод используют NaOH и Са(ОН)2. Образование хлопьев протекает по реакциям:
FeCl3+3H2O→Fe(OH)3+3HCl, 3)
Fe2(SO4)3+6H2O →2Fe(OH)3+3H2SO4; (II.44)
при подщелачивании:
2FeCl3+3Ca(OH)2→2Fe(OH)3+3CaCl2 (II.45)
Fe2(SO4)3+3Ca(OH)2→2Fe(OH)3+3CaSO4. (II.46)
Соли железа как коагулянты имеют ряд преимуществ перед солями алюминия: лучшее действие при низких температурах воды; более широкая область оптимальных значений рН среды; большая прочность и гидравлическая крупность хлопьев; возможность использовать для вод с более широким диапазоном солевого состава; способность устранять вредные запахи и привкусы, обусловленные присутствием сероводорода. Однако имеются и недостатки: образование при реакции катионов железа с некоторыми органическими соединениями сильно окрашивающих растворимых комплексов; сильные кислотные свойства, усиливающие коррозию аппаратуры; менее развитая поверхность хлопьев.
При использовании смесей A12(SO4)3 и FeCl3 в соотношениях от 1:1 до 1:2 достигается лучший результат коагулирования, чем при раздельном использовании реагентов. Происходит ускорение осаждения хлопьев. Кроме названных коагулянтов, для обработки сточных вод могут быть использованы различные глины, алюминийсодержащие отходы производства, травильные растворы, пасты, смеси, шлаки, содержащие диоксид кремния.
Оптимальную дозу реагента устанавливают на основании пробного коагулирования.
Скорость коагуляции зависит от концентрации электролита. В общем виде эта зависимость показана на рис. II-16. При малых концентрациях электролита эффективность соударений частиц, т. е. отношение числа столкновений, окончившихся слипанием, к общему числу столкновений близка к нулю (ψ = 0). По мере роста концентрации скорость коагуляции увеличивается, но не все столкновения эффективны — такую коагуляцию называют медленной. При ψ = 1 наступает быстрая коагуляция, при которой все столкновения частиц заканчиваются образованием агрегатов.
Скорость быстрой коагуляции для неподвижной среды при броуновском движении частиц по теории Смолуховского равна:
dnx/dτ =K(no-nx)2. (II.47)
Количество частиц в единице объема воды за время τ для быстрой и медленной коагуляции определяется по формулам:
nτ=n0/(1+τ/Т1/2), nτ=n0/[1+ψ (τ /Т1/2)]. (II.48)
Для ламинарного и турбулентного движения потока воды число взаимодействий частиц за единицу времени в единице объема жидкости nл и nт. вычисляется по формулам:
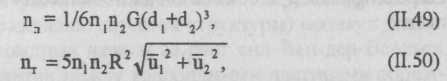
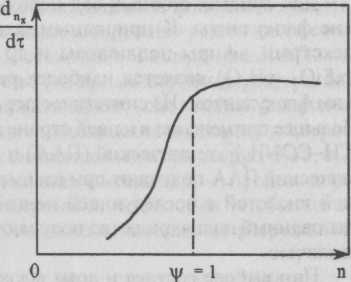 где
nх
— число агрегатов частиц; К — константа
коагуляции K
≈
4pR
≈
8pDr;
D
— коэффициент диффузии одиночных
частиц; r
— радиус частиц; R
— расстояние, на которое должны
приблизиться частицы, чтобы произошло
их объединение (R
≈
2r);
n0—
начальная концентрация частиц; Т1/2
— время коагуляции, в течение которого
количество частиц в единице объема
уменьшается вдвое; ψ
— коэффициент эффективности
столкновений частиц; nл
и nT—
число взаимодействий частиц за
единицу времени в единице объема
соответственно для ламинарного и
турбулентного движения потока воды; п,
и n2—
число частиц с размером d1
и d2
соответственно; (G
— скоростной градиент (G=dv
/dz);
u1
и u2—
среднеквадратичные скорости двух
коагулирующих частиц.
где
nх
— число агрегатов частиц; К — константа
коагуляции K
≈
4pR
≈
8pDr;
D
— коэффициент диффузии одиночных
частиц; r
— радиус частиц; R
— расстояние, на которое должны
приблизиться частицы, чтобы произошло
их объединение (R
≈
2r);
n0—
начальная концентрация частиц; Т1/2
— время коагуляции, в течение которого
количество частиц в единице объема
уменьшается вдвое; ψ
— коэффициент эффективности
столкновений частиц; nл
и nT—
число взаимодействий частиц за
единицу времени в единице объема
соответственно для ламинарного и
турбулентного движения потока воды; п,
и n2—
число частиц с размером d1
и d2
соответственно; (G
— скоростной градиент (G=dv
/dz);
u1
и u2—
среднеквадратичные скорости двух
коагулирующих частиц.
Рис. II-16. Зависимость относительной скорости коагуляции от концентрации электролита
В полидисперсных системах коагуляция происходит быстрее, чем в монодисперсных, так как крупные частицы при оседании увлекают за собой более мелкие. Форма частиц также влияет на скорость коагуляции. Например, удлиненные частицы коагулируют быстрее, чем шарообразные.
Размер хлопьев (в пределах 0,5-3 мм) определяется соотношением между молекулярными силами, удерживающими частицы вместе, и гидродинамическими силами отрыва, стремящимися разрушить агрегаты. Для характеристики хлопьев пользуются понятием эквивалентного диаметра:
![]()
где v — кинематическая вязкость воды; ρх— плотность хлопьев; woc — скорость свободного осаждения; Кф — коэффициент формы хлопьев.
Плотность хлопьев определяется с учетом плотностей воды рв и твердой фразы ρт и объема твердого вещества в единице объема хлопьев δт:
![]()
Прочность хлопьев зависит от гранулометрического состава образующихся частиц и пластичности. Агломераты частиц, неоднородных по размеру, прочнее, чем однородных. Вследствие выделения газов из воды а также в результате аэрации и флотации происходит газонасыщение хлопьев, которое сопровождается уменьшением плотности хлопьев и уменьшением скорости осаждения.
Флокуляция. Это процесс агрегации взвешенных частиц при добавлении в сточную воду высокомолекулярных соединений, называемых флокулянтами. В отличие от коагуляции при флокуляции агрегация происходит не только при непосредственном контакте частиц, но и в результате взаимодействия молекул адсорбированного на частицах флокулянта.
Флокуляцию проводят для интенсификации процесса образования хлопьев гидроксидов алюминия и железа с целью повышения скорости их осаждения. Использование флокулянтов позволяет снизить дозы коагулянтов, уменьшить продолжительность процесса коагуляции и повысить скорость осаждения образующихся хлопьев.
Для очистки сточных вод используют природные и синтетические флокулянты. К природным флокулянтам относятся крахмал, декстрин, эфиры целлюлозы и др. Активный диоксид кремния (xSiO2 * yH2O) является наиболее распространенным неорганическим флокулянтом. Из синтетических органических флокулянтов наибольшее применение в нашей стране получил полиакриламид [-СН2 -CH-CONH2]n , технический (ПАА) н гидролизованный (ГППА). Технический ПАА получают при взаимодействии акрилонитрила с серной кислотой с последующей полимеризацией акриламида. Гидролизованный полиакриламид получают омылением технического ПАА щелочью.
При выборе состава и дозы флокулянта учитывают свойства егомакромолекул и природу диспергированных частиц. Оптимальная доза ПАА для очистки промышленных сточных вод колеблется в пределах 0,4-1 г/м3. ППА действует в широком диапазоне рН среды. Однако скорость осаждения сфлокулированных хлопьев при рН>9 уменьшается.
Механизм действия флокулянтов основан на следующих явлениях: адсорбции молекул флокулянта на поверхности коллоидных частиц; ретикуляции (образование сетчатой структуры) молекул флокулянта; слипании коллоидных частиц за счет сил Ван-дер-Ваальса. При действии флокулянтов между коллоидными частицами образуются трехмерные структуры, способные к более быстрому и полному отделению от жидкой фазы. Причиной возникновения таких структур является адсорбция макромолекул флокулянта на нескольких частицах с образованием между ними полимерных мостиков. Коллоидные частицы заряжены отрицательно, что способствует процессу взаимной коагуляции с гидроксидом алюминия или железа. При добавлении активированного силиката увеличивается в 2-3 раза скорость осаждения и повышается эффект осветления. Полиакриламид выпускается в виде 7-9%-го геля, затвердевающего при температуре ниже 273°К. При добавлении ПАА к воде ее вязкость резко возрастает.
Эффективность любого флокулянта рассчитывают по формуле:
ηф = (wсф-w)/wq, (II.53)
где wсф и w — скорость осаждения сфлокулированного и несфлоку-лированного шлама соответственно, мм/с; q — расход флокулянта на 1 т твердого вещества, г.
Процесс очистки сточных вод коагуляцией и флокуляцией состоит из следующих стадий: дозирование и смешение реагентов со сточной водой; хлопьеобразование и осаждение хлопьев (рис.II-17).
Для смешения коагулянтов с водой применяют гидравлические и механические смесители. В гидравлических смесителях смешение происходит вследствие изменения направления движения и скорости потока воды. Схема одного из смесителей показана на рис. II-18, а. В механических смесителях — аппаратах с мешалкой — процесс перемешивания должен быть равномерным и медленным, чтобы частицы при сближении образовывали хлопья, которые не разрушались бы при вращении мешалки.
После смешения сточных вод с реагентами, воду направляют в камеры хлопьеобразования. Используют перегородчатые, вихревые и с механическими мешалками камеры. Образование хлопьев в камерах протекает медленно — за 10-30 мин. Схема перегородчатой камеры показана на рис. II-18, б.
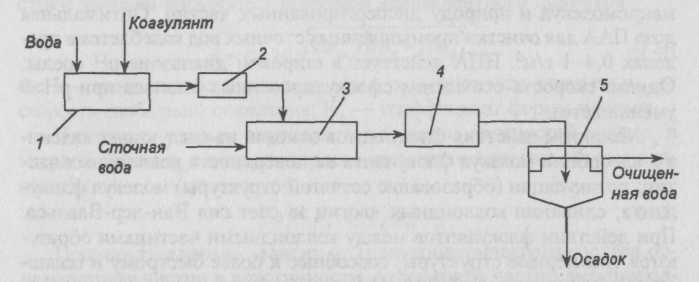
Рис. II-17. Схема установки для очистки вод коагуляцией: 1 — емкость; 2 — дозатор; 3 — смеситель; 4 — камера хлопьеобразования; 5 — отстойник
Она представляет собой резервуар, разделенный перегородками на ряд последовательно проходимых водой коридоров. Скорость воды в коридорах принимают 0,2-0,3 м/с.
Осаждение хлопьев происходит в отстойниках и осветлителях, конструкции которых описаны в седьмой главе. Часто стадии смешения, коагулирования и осаждения проводят в одном аппарате. Один из таких аппаратов показан на рис. II-18, в.
Сточная вода, смешанная с коагулянтом, по трубе поступает в воздухоотделитель. Затем вода движется по центральной трубе к распределительным трубам, которые заканчиваются соплами для распределения и вращения воды в кольцевой зоне, куда вводят флокулянт. Хлопья коагулянта образуются в кольцевой зоне. Взвешенные частицы с хлопьями оседают на дно и их удаляют из аппарата. Осветленная вода через отверстие попадает в желоб, откуда ее направляют на использование.
