
- •Теория металлургических процессов
- •Введение
- •1. Состав и свойства высокотемпературной газовой атмосферы
- •1.1. Термодинамика газовых атмосфер
- •1.2. Гомогенные газовые процессы
- •2. Анализ процессов горения твердого углерода
- •3. Оценка прочности химических соединений
- •3.1. Диссоциация карбонатов
- •3.2. Диссоциация оксидов железа
- •3.3. Механизм и кинетика процессов диссоциации
- •При этом образование зародыша новой фазы в недрах старой должно сопровождаться уменьшением энергии Гиббса системы, рассчитываемой по уравнению
- •3.4. Окисление твердых металлов
- •4. Процессы восстановления металлов
- •4.1. Термодинамическая характеристика процессов восстановления
- •4.2. Восстановление оксидов железа твёрдыми и газообразными восстановителями
- •4.3. Механизм и кинетика процессов восстановления
- •5. Металлургические расплавы
- •5.1. Общая характеристика
- •5.2. Металлические расплавы
- •5.3. Термодинамические свойства металлических расплавов. Параметры взаимодействия
- •5.4. Шлаковые расплавы. Состав, строение, термодинамические свойства
- •Газы в сталях. Процессы нитридообразования
- •7. Раскисление металлических расплавов
- •8. Распределение элементов между металлом и шлаком
- •Библиографический список
- •Оглавление
3. Оценка прочности химических соединений
Процессы диссоциации важнейших для металлургии соединений – оксидов, нитридов, карбонатов – являются весьма важными, поскольку являются прямым способом получения металлов. Данные процессы весьма однотипны, и в зависимости от температуры их можно представить уравнениями вида:
АВтв = Атв + Вгаз;
АВтв = Аж + Вгаз;
АВж = Атв + Вгаз;
АВж = Аж + Вгаз.
Величина равновесного парциального давления газообразного продукта этих реакций называется упругостью диссоциации соединения АВ и характеризует прочность данного соединения. Реакции диссоциации являются эндотермическими, т.е. с повышением температуры равновесие смещается в сторону продуктов реакции. Уменьшение давления при сохранении состава газовой фазы оказывает аналогичное действие.
Согласно правилу фаз Гиббса, число степеней свободы для реакций диссоциации определяется как
С = К + 2 Ф = 2 + 2 3 = 1,
т.е. для количественной характеристики достаточно лишь одного независимого параметра – температуры, от которой зависит константа равновесия процесса:
Кр = РВ = (Т).

Рис. 3.1. Зависимость упругости диссоциации соединения АВ от температуры
На рис. 3.1 представлена зависимость РВ от температуры для указанных реакций.
3.1. Диссоциация карбонатов
В черной металлургии наибольший практический интерес представляет анализ реакции диссоциации карбонатов кальция СаСО3, магния MgCO3, марганца MnCO3, железа FeCO3 (сидерит) и доломита CaMg(CO3)2. Процессы диссоциации этих соединений однотипны и протекают по уравнению:
MeCO3 = MeO + CO2,
Kp =
![]()
Величина
![]() является упругостью диссоциации
карбоната и характеризует меру химической
прочности соединения.
является упругостью диссоциации
карбоната и характеризует меру химической
прочности соединения.
Наибольший интерес представляет реакция диссоциации карбоната кальция, который входит в состав шихтовых материалов доменного и сталеплавильного производства, а также используется для получения СаО через обжиг известняка.
Реакция диссоциации СаСО3 описывается уравнением вида
СаCO3 = СаOтв + CO2, = 177 400 Дж ; (3.1)
GТ = 178 070 150 Т; Kp(3.1) =
Зависимость упругости диссоциации карбоната от температуры представлена на рис. 3.2.
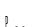
Рис. 3.2. Упругость диссоциации СаСО3
Анализ данной графической зависимости с использованием изотермы химической реакции показывает, что диссоциация карбоната возможна, когда фактическое значение меньше равновесного и при этом GТ < 0. Температура, при которой возможен этот процесс, является температурой начала диссоциации ТНД.
Любая фигуративная точка 1 выше равновесной линии на рис. 3.2 отвечает устойчивому существованию карбоната СаСО3. Любая фигуративная точка 2 ниже линии отвечает устойчивому существованию оксида СаО.
Процесс диссоциации карбоната протекает с высокой скоростью при температурах выше температуры химического кипения ТХК, при которой упругость диссоциации становится равной общему внешнему давлению газовой фазы.
