
- •Глава 2. Корпускулярні та хвильові властивості частинок
- •2.1. Відкриття корпускул
- •2.2. Вимірювання заряду електрона. Досліди Міллікена
- •Таким чином, у цих дослідах вдалося виміряти найменший від’ємний заряд речовини і його приписали зарядові електрона. За ці класичні досліди Мілікен у 1923 році був відзначений Нобелівською премією.
- •2.3. Маси атомів. Ізотопи
- •2.4. Релятивістські частинки. Рівняння їх руху
- •2.5. Зв’язок між масою, енергією та імпульсом
- •Розсіяння електронів розрідженими газами
- •2.7. Класичний розгляд розсіяння
- •- Кут розсіяння, - прицільна відстань, :
- •2.8. Зміна інтенсивності потоку частинок внаслідок розсіяння в речовині
- •2.9. Довжина вільного пробігу частинки в речовині
- •2.11. Ефект Рамзауера
- •На атомах Ar.
- •2.12. Неможливість пояснення процесів розсіяння електронів на основі класичних уявлень про електрон, як корпускулу
- •Висновки
- •Глава 3. Експериментальні передумови сучасної теорії атома
- •3.1. Досліди Резерфорда з розсіяння -частинок
- •3.2. Формула Резерфорда
- •3.3. Планетарна модель атома, труднощі її пояснення на підставі класичних уявлень
- •3.4. Загальні характеристики атомних спектрів
- •3.5. Спектральні терми
- •3.6. Комбінаційний принцип (Рідберга-Рітца)
- •3.7. Спектр атомів водню
- •3.8. Досліди Франка і Герца
- •3.9. Визначення потенціалів іонізації атомів
- •3.10. Висновки
- •Глава 4. Атом водню в моделі бора
- •4.1.Постулати Бора
- •4.2. Рівні енергії та стаціонарні орбіти
- •4.3. Позитроній та мезоатом
- •4.4. Еліптичні орбіти. Головне та орбітальне квантові числа.
- •4.5. Висновки
- •Глава 5. Хвильова природа матерії
- •5.1. Передумови пізнання хвильової природи матерії
- •5.1.1. Квантова природа випромінювання світла
- •Квантова природа поглинання світла
- •Короткохвильова границя неперервного спектра рентгенівських променів
- •Суцільного спектра рентгенівських променіввід енергії електронів .
- •5.1.4. Ефект Комптона
- •Розсіяних рентгенівських променів при різних кутах розсіяння .
- •В ефекті Комптона.
- •5.1.5. Некогерентне розсіяння квантів на електронах
- •5.1.6. Оптико-механічна аналогія
- •5.2. Гіпотеза та формула де Бройля
- •5.3. Експериментальне обґрунтування хвильової природи матерії
- •5.3.1. Досліди Рамзауера
- •5.3.2. Досліди Девісона та Джермера з відбиття електронів від граней монокристалів
- •Розсіяних електронів поверхнями речовини: а) аморфної, б) кристалічної, в-ж) кристалічної при різних енергіях електронів.
- •Променями, що відбиваються від двох сіткових площин:
- •5.3.3. Досліди Томсона по проходженню електронів крізь тонкі плівки речовини
- •5.4. Дифракція та інтерференція інших частинок та атомів
- •5.5. Дифракція поодиноких електронів
- •5.6.Визначення довжини хвилі де Бройля матеріальних частинок із дослідів по дифракції електронів на кристалах
- •5.7. Електронографія та нейтронографія
- •5.8. Висновки
- •Глава 6. Хвильова функція електронів та її фізичний зміст
- •6.1. Хвильова функція плоскої хвилі де Бройля
- •6.2. Хвильовий пакет, як модель частинки та її недосконалість
- •6.3. Фізичний зміст хвильової функції
- •Співвідношення невизначеностей
- •6.5. Висновки
- •Глава 7. Рівняння шредінґера
- •7.1. Рівняння Шредінґера
- •7.2. Найпростіші випадки розв’язку рівнянь Шредінґера
- •Частинка в потенціальній ямі з нескінченними стінками
- •7.2.2. Частинка в потенціальній ямі зі скінченними стінками
- •7.3. Гармонічний осцилятор
- •7.4. Прозорість потенціального бар’єра (тунелювання)
- •7.5. Оператори
- •7.6. Висновки
- •Глава 8. Уявлення про будову атома водню у квантовій механіці
- •8.1. Схема розв’язку рівняння Шредінґера для атома водню
- •8.2. Кутова частина рівняння Шредінґера
- •8.3. Кутовий розподіл густини ймовірності знайти електрон в атомі водню. Електронна хмара.
- •8.4. Атомні орбіталі атома водню
- •8.5. Фізичний зміст квантових чисел та
- •8.6. Просторове квантування
- •8.7. Радіальна частина хвильової функції електрона атома водню
- •8.8. Радіальний розподіл електронної хмари атома водню
- •Густини стану атому н: а) ; б) контурна карта;
- •8.9. Квантові числа та їх фізичний зміст
- •8.10. Правила відбору квантових чисел
- •8.11. Висновки
- •Глава 9. Експериментальні дані про будову та властивості складних атомів
- •9.1. Структура атомів лужних металів, валентний електрон
- •9.2. Зняття виродження за квантовим числом
- •9.3. Спектральні серії атомних спектрів лужних металів
- •9.4. Дублетна структура термів та спектральних ліній атомів лужних металів
- •9.5. Спін електрона
- •9.6. Сума моментів кількості руху
- •9.7. Тонка структура спектрів складних атомів як наслідок спін-орбітальної взаємодії
- •На ядрі, б) – початок координат на електроні, в) – розщеплення рівнів.
- •Особливості тонкої структури атомних спектрів лужних металів
- •Надтонка структура спектральних термів атомів лужних металів
- •9.10. Висновки
- •Глава 10. Тонка структура атомного спектра водню
- •10.1. Тонка структура спектральних ліній атомного спектра водню. Спін-орбітальна взаємодія
- •10.2. Надтонка структура ліній атомного спектра водню
- •10.3. Досліди Лемба і Різерфорда з вимірювання зміщення енергетичних рівнів атомів водню
- •Частоти електромагнітних хвиль, що опромінюють потік збуджених атомів водню.
- •Зсув та надтонка структура основного терму за рахунок впливу спіну ядра.
- •10.4. Поняття про нульові коливання та поляризацію вакууму як причини лембівського зсуву
- •10.5. Висновки
- •Глава 11. Векторна модель атома
- •11.1. Векторна модель атома. Типи зв’язку
- •11.2. Нормальний (l-s) або Рассел-Саундеровський зв’язок
- •11.3. Квантові числа складних атомів
- •11.4. Правила відбору
- •11.5. Правила Хунда (Гунда)
- •11.6. Систематика спектрів складних атомів з нормальним зв’язком
- •11.7. Приклади застосування векторної моделі атома
- •11.9. Висновки
- •12. Атом гелію
- •12.1. Рівняння Шредінґера для двохелектронного атома
- •12.2. Метод збурень
- •12.3. Принцип Паулі
- •12.4. Вплив антисиметричності хвильових функцій на стаціонарні стани атому Не
- •12.5. Висновки
- •Глава 13. Інтенсивність та ширина спектральних ліній
- •Ймовірність переходів
- •Золоте правило Фермі
- •Сила осцилятора
- •13.4. Поглинання світла
- •13.5. Інтенсивність спектральних ліній
- •13.6. Ширина спектральних ліній
- •13.7. Принципи генерації електромагнітних коливань (лазери)
- •- Дзеркала резонатора, 2-робоче тіло,
- •Рубіновий лазер
- •13.8. Висновки
- •Глава 14. Будова та заповнення оболонок складних атомів. Теорія періодичної системи елементів д.І. Менделєєва
- •14.1. Послідовність заповнення електронних
- •Оболонок атомів
- •14.2. Періодична система елементів
- •14.3. Недоліки квантової моделі періодичної системи елементів
- •14.4. Прикінцеві зауваження
- •Глава 15. Рентгенівські промені
- •15.1. Характеристичний спектр рентгенівських променів
- •Спектри поглинання рентгенівських променів
- •15.4. Висновки
- •Глава 16. Магнітні властивості атомів
- •16.1. Орбітальний та спіновий магнетизм. Магнетон Бора
- •Сумарний магнітний момент кількості руху. Множник Ланде
- •Розкладемо вектор на паралельну і перпендикулярну складові
- •Просторове квантування
- •Гіромагнітні ефекти
- •Досліди Штерна й Герлаха
- •16.6. Сучасні методи визначення атомних магнітних моментів
- •16.6.1. Електронний парамагнітний резонанс (епр)
- •Таким чином метод епр дозволяє отримувати такі результати:
- •16.6.2. Надтонка структура ліній епр
- •У магнітному полі з урахуванням ядерного спіну.
- •16.6.3. Резонансний метод Рабі дослідження магнітних моментів атомних ядер
- •16.6.4. Ядерний магнітний резонанс (ямр).
- •16.7. Значення магніто-резонансних методів для визначення атомних магнітних моментів
- •Висновки
- •Глава 17. Вплив магнітного та електричного полів на атоми
- •17.1. Ефект Зеємана
- •(Частота Лармора)
- •17.2. Аномальний ефект Зеємана і його квантова теорія
- •Ефект Пашена і Бака
- •17.4. Поляризація світла при ефекті Зеємана
- •Ефект Штарка
- •Сукупність атомів у магнітному полі
- •17.6.А. Парамагнетизм
- •17.6.Б. Діамагнетизм речовини. Теорема Лармора
- •17.7. Циклотронний резонанс
- •(А) та ділянки спектра поглинання при ньому (б, в і г).
- •17.8. Висновки
- •Глава 18. Природа хімічного зв'язку
- •18.1. Вступ
- •18.2. Іонний зв’язок
- •При ця задача, як і в главі 13, розділяється на дві незалежних задачі для не взаємодіючих атомів водню, для яких існує розв’язок у вигляді: , ; , .
- •18.4. Сили Ван-дер-Ваальса
- •18.5. Водневий зв’язок
- •18.6. Метод валентного зв’язку
- •18.7. Метод молекулярних орбіталей
- •18.8. Гібридизація орбіталей
- •18.9. Висновки
- •Глава 19. Спектри молекул
- •19.1. Загальна характеристика
- •19.2. Обертальні спектри молекул
- •Обертального спектру.
- •19.3. Коливальні спектри молекул
- •19.4. Коливально-обертальні спектри молекул
- •19.5. Електронні стани
- •Принцип Франка-Кондона. Якісне пояснення інтенсивності ліній молекулярних спектрів
- •19.7. Комбінаційне розсіяння світла
- •Висновки
- •Глава 20. Квантові властивості твердих тіл
- •20.1. Вступ
- •20.2. Електрон у полі періодичного потенціалу
- •20.3. Модель Кроніга – Пені
- •20.4. Зони Бріллюена
- •20.5. Заповнення зон електронами
- •20.6. Густина станів
- •(А) та його енергетичні рівні (б).
- •20.7. Динаміка електронів, ефективна маса, електрони та дірки
- •20.8. Ефект Холла
- •20.9. Електропровідність металів
- •20.10. Особливості власних напівпровідників
- •20.11. Домішкові напівпровідники
- •I(V) характеристика.
- •20.13. Магнітні властивості твердих тіл
- •20.14. Обмінний гамільтоніан Гeйзенберга. Спонтанна намагніченість, феромагнетизм та антиферомагнетизм
- •20.15. Феромагнітні домени, стінки Блоха
- •20.16. Спінові хвилі
- •20.17. Надпровідність
- •20.18. Магнітні властивості надпровідників
- •20.19. Квантування магнітного потоку
- •20.20. Критичний струм і критичне магнітне поле
- •20.21. Ефекти Джозефсона
- •20.22. Високотемпературна надпровідність
- •20.23. Прикінцеві зауваження
11.5. Правила Хунда (Гунда)
Векторна модель не дає енергетичної послідовності термів. Для визначення найбільш глибоких рівнів енергій користуються трьома емпіричними правилами Хунда (Гунда).
Перше правило Хунда. Для даної електронної конфігурації терми з більшою мультиплетністю мають більші абсолютні значення енергій:
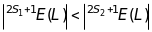 для
для 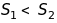 (11.11)
(11.11)
Наприклад,
триплетні терми на енергетичних
діаграмах, де енергія зв’язаного
електрона
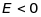 ,
знаходяться
нижче, ніж дублетні чи синглетні терми.
,
знаходяться
нижче, ніж дублетні чи синглетні терми.
Друге
правило Хунда.
Для даної електронної конфігурації та
мультиплетності, тобто при заданих
 і
,
основні терми атомів з більшими значеннями
сумарного орбітального числа
мають більші за абсолютною величиною
енергії, ніж терми з меншими значеннями
:
і
,
основні терми атомів з більшими значеннями
сумарного орбітального числа
мають більші за абсолютною величиною
енергії, ніж терми з меншими значеннями
:
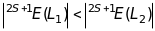 для
для  (11.12)
(11.12)
Третє правило Хунда. Для даної електронної конфігурації при заданих значеннях квантових чисел , і чим менше квантове число J, тим більша за абсолютною величиною енергія терма:
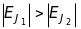 для
для 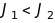 (11.13)
(11.13)
Така
ієрархія має місце у випадку,
коли валентна електрона оболонка
заповнена наполовину,
тобто на ній знаходиться електронів
менше ніж
 .
У випадку, коли
електронна оболонка
заповнена
більше, як на половину,
тобто, коли на ній знаходиться електронів
більше, ніж
,
то
в (11.13)
змінюється знак нерівності на протилежний
і терми заглиблюються із збільшенням
квантового числа
на енергетичних діаграмах,
,
.
У випадку, коли
електронна оболонка
заповнена
більше, як на половину,
тобто, коли на ній знаходиться електронів
більше, ніж
,
то
в (11.13)
змінюється знак нерівності на протилежний
і терми заглиблюються із збільшенням
квантового числа
на енергетичних діаграмах,
,
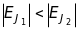 для
для
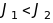 .
.
Перші два правила засновані на врахуванні електростатичної взаємодії електронів, а третє - на врахуванні магнітної взаємодії.
Перше правило пояснюється детальними розрахунками обмінної взаємодії, які показують, що в атомі більшої мультиплетності, наприклад, триплетному, електронний розподіл виявляється більш стиснутим, ніж в атомі меншої мультиплетності, наприклад, синглетному, що підсилює притяжіння електронів до ядра. Воно компенсує відштовхування між електронами з однаково направленими спінами і дає виграш в енергії атомів з паралельними спінами по відношенню до атомів з антипаралельними спінами.
Друге правило відображає здатність електронів уникати один одного, якщо орбітальні моменти примушують їх рухатись в одному напрямку. Електронам, що рухаються в одному напрямку, простіше залишатись віддаленими один від одного, що зменшує кулонівське відштовхування. Якщо електрони рухаються в різних напрямках, то вони більш часто зустрічаються, і тому середня відстань між ними менша, а кулонівське відштовхування більше.
Третє правило відображає спін-орбітальну взаємодію, яка буде меншою при протилежно направлених магнітних моментах орбітального і спінового.
Правило
Гунда в основному добре працює для
визначення основних термів (найнижчих
по енергії) для атомів, для яких
справедливий
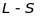 звязок.
Для атомів для яких справедливий
звязок.
Для атомів для яких справедливий
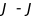 зв’язок правило Гунда може давати не
вірні результати.
зв’язок правило Гунда може давати не
вірні результати.
11.6. Систематика спектрів складних атомів з нормальним зв’язком
Мета систематики термів і спектрів складних атомів – це встановлення структури термів та спектральних ліній – визначення їх мультиплетності та енергетичної (частотної) ієрархії. Вона складається з таких етапів.
По-перше, користуючись принципом Паулі, який дає правило заповнення електронних атомних оболонок (глава 13), визначають електронну конфігурацію атома – розподіл електронів на оболонках.
По-друге,
за допомогою векторної моделі визначають
квантові числа електронів
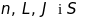 валентної оболонки атома.
Для обрахунку максимального сумарного
орбітального квантового числа
,
потрібно брати суму всіх орбітальних
чисел електронів на незаповненій
електронній оболонці
валентної оболонки атома.
Для обрахунку максимального сумарного
орбітального квантового числа
,
потрібно брати суму всіх орбітальних
чисел електронів на незаповненій
електронній оболонці
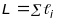 .
Сума дає вірні результати, коли електронна
конфігурація не має еквівалентних
електронів.
.
Сума дає вірні результати, коли електронна
конфігурація не має еквівалентних
електронів.
Еквівалентні
електрони - це електрони
з однаковими квантовими числами
і
.
Їхня максимальна кількість дорівнює
кількості можливих станів
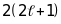 .
Тому заповнені оболонки мають електронні
конфігурації:
.
Тому заповнені оболонки мають електронні
конфігурації:
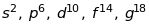 .
Еквівалентні електрони заповненої
оболонки мають нульові моменти кількості
руху
.
Еквівалентні електрони заповненої
оболонки мають нульові моменти кількості
руху
 .
Оболонка заповнюється так: спочатку
електрони заповнюють
.
Оболонка заповнюється так: спочатку
електрони заповнюють
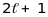 станів з різними магнітними квантовими
числами
станів з різними магнітними квантовими
числами
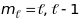 ,
,
 ,
,
 …,
…,
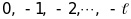 при однаковому квантовому числі
при однаковому квантовому числі
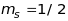 ,
а потім
,
а потім
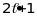 станів із спіновим магнітним числом
станів із спіновим магнітним числом
 .
Наприклад, оболонка p має
.
Наприклад, оболонка p має
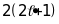 =
6 станів (p6).
Спочатку на ній заповнюються стани з
=
6 станів (p6).
Спочатку на ній заповнюються стани з
 з проекцією спіну
:
px,
py
,
pz
- конфігурації
з проекцією спіну
:
px,
py
,
pz
- конфігурації
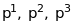 відповідно. Потім починають заповнюватись
стани з протилежно направленою проекцією
спіну
:
px,
py,
pz
- конфігурація
відповідно. Потім починають заповнюватись
стани з протилежно направленою проекцією
спіну
:
px,
py,
pz
- конфігурація
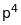 ,
після цього конфігурація p5
(px,
py,
pz)
і потім конфігурація p6
(px,
py,
pz
).
,
після цього конфігурація p5
(px,
py,
pz)
і потім конфігурація p6
(px,
py,
pz
).
Емпірично
встановлено, що стан N еквівалентних
електронів коли ,
еквівалентний стану з електронами в
кількості
,
еквівалентний стану з електронами в
кількості
 (11.14)
(11.14)
Наведемо
приклад еквівалентних електронів.
Конфігурація
еквівалентна конфігурації
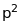 ;
конфігурація
;
конфігурація
 еквівалентна конфігурації
еквівалентна конфігурації
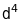 ;
конфігурація
;
конфігурація
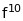 еквівалентна конфігурації
еквівалентна конфігурації
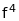 ,тощо.
,тощо.
По-третє,
за допомогою квантового числа сумарного
спіну S
встановлюється мультиплетність термів
за
формулою
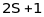 .
Максимальне значення числа S знаходиться
як сума спінових чисел окремих електронів
.
Максимальне значення числа S знаходиться
як сума спінових чисел окремих електронів
 ,
де
.
Для парних
,
де
.
Для парних
 максимальне спінове число дорівнює
максимальне спінове число дорівнює
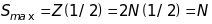 тому
мультиплетність термів буде непарною,
бо
тому
мультиплетність термів буде непарною,
бо
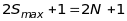 ,
і навпаки - для непарних
мультиплетність буде парною, бо
,
і навпаки - для непарних
мультиплетність буде парною, бо
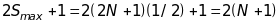 .
Таблиця 11.3 ілюструє цю властивість
термів.
.
Таблиця 11.3 ілюструє цю властивість
термів.
Таблиця 11.3. Мультиплетність термів атомів з різними (нормальні та збуджені конфігурації) |
|||||
|
1 |
2 |
3 |
4 |
5 |
елемент |
|
|
|
|
|
|
½ |
0 |
1/2 |
0 |
1/2 |
|
- |
1 |
|
1 |
3/2 |
|
2 - |
1 3 |
2
|
1 3 |
2 4 |
мультиплетність |
дублет - |
синглет триплет |
дублет
|
синглет триплет |
дублет квартет |
Вона
дозволяє знаходити терми для парних та
непарних
 мультиплетних термів для кожної трійки
квантових чисел
мультиплетних термів для кожної трійки
квантових чисел
 як це наведено у таблиці 11.4. Методика
знаходження термів для еквівалентних
електронів описані, наприклад, в задачнику
[1]
та підручнику [6].
як це наведено у таблиці 11.4. Методика
знаходження термів для еквівалентних
електронів описані, наприклад, в задачнику
[1]
та підручнику [6].
Таблиця 11.4. Терми різних мультиплетностей |
|||||||||||
|
c дублети |
||||||||||
|
0 |
1 |
2 |
3 |
4 |
|
1/2 |
3/2 |
5/2 |
7/2 |
9/2 |
0 |
1S0 |
|
|
|
|
|
2S1/2 |
|
|
|
|
1 |
|
1P1 |
|
|
|
|
2P1/2 |
2P3/2 |
|
|
|
2 |
|
|
1D2 |
|
|
|
|
2D3/2 |
2D5/2 |
|
|
3 |
|
|
|
1F3 |
|
|
|
|
2F5/2 |
2F7/2 |
|
4 |
|
|
|
|
1G4 |
|
|
|
|
2G7/2 |
2G9/2 |
|
|
||||||||||
|
0 |
1 |
2 |
3 |
4 |
|
1/2 |
3/2 |
5/2 |
7/2 |
9/2 |
0 |
|
3S1 |
|
|
|
0 |
|
4S3/2 |
|
|
|
1 |
3P0 |
3P1 |
3P2 |
|
|
1 |
4P1/2 |
4P3/2 |
4P5/2 |
|
|
2 |
|
3D1 |
3D2 |
3D3 |
|
2 |
4D1/2 |
4D3/2 |
4D5/2 |
4D7/2 |
|
3 |
|
|
3F2 |
3F3 |
3F4 |
3 |
|
4F3/2 |
4F5/2 |
4F7/2 |
4F9/2 |
|
|
|
|
|
|
|
|
|
|
|
|



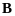
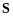
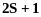
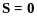 синглети
синглети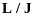
 триплети
триплети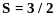 квартети
квартети