
- •1)Азотистый баланс
- •1. Синтез 5'-фосфорибозиламина
- •Реакции синтеза амф и гмф
- •4. Образование нуклеозидтрифосфатов атф и гтф.
- •1) Главные компоненты желудочного сока
- •Реакция взаимопревращения глицина и серина
- •2) Распад пуриновых оснований
- •3) Регуляция синтеза белка
- •4) Обнаружение молочной кислоты в желудочном
- •1. Метаболизм феиилаланина
- •2. Особенности обмена тирозина в разных тканях
- •Механизм реакции синтеза дезоксирибонуклеотида
- •3. Реакция фосфорилирования
- •4) Определение свободной соляной кислоты
- •Окисление аланина
- •3) Синтез амидов из карбоновых кислот
- •1. Особенности обмена метионина
- •2. Обмен цистеина
- •4) Мочевая кислота сыворотки крови
- •Реакция синтеза глутаминовой кислоты
- •Реакция синтеза глутамина
- •Реакция синтеза аспарагина
- •Переваривание белков в желудочно-кишечном тракте
Окисление аланина
Два атома углерода аланина попадают в ЦТК после того, как безазотистый остаток аланина – пируват – окислится в пируват-дегидрогеназном комплексе с образованием НАДН. Образованный ацетил-S-КоА входит в ЦТК и полностью окисляется в одном его обороте. В общей сложности в дыхательную цепь направляется 4 молекулы НАДН (3 из ЦТК и 1 из ПВК-дегидрогеназы) и 1 молекула ФАДН2.

3) Синтез амидов из карбоновых кислот
При нагревании сухих карбоксилатов аммония они отщепляют воду превращаясь в амиды:
![]() (60)
(60)
Реакция часто проводится путем пропускания паров кислот вместе с аммиаком над дегидратирующими катализаторами.
На этой реакции основан промышленный процесс получения нейлона по схеме:
![]()
адипиновая кислота гексаметилендиамин
![]() n[-OOC(CH2)4COO-
H3N+(CH2)6N+H3]
-[-OCC(CH2)4CONH(CH2)6NH-]n¾
(61)
n[-OOC(CH2)4COO-
H3N+(CH2)6N+H3]
-[-OCC(CH2)4CONH(CH2)6NH-]n¾
(61)
нейлоновая соль нейлон 6,6
В лаборатории амиды чаще всего получают действием на аммиак или амины хлорангидридами и ангидридами карбоновых кислот:
Циклические ангидриды кислот реагируя с аммиаком превращаются в аммонийные соли амидокислот:
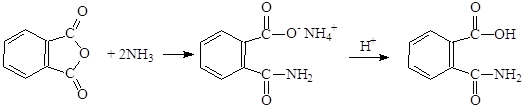 (62)
(62)
фталевый ангидрид фталамат аммония фталамовая кислота
Нагревание амидокислот вызывает их дегидратацию с образованием имидов.
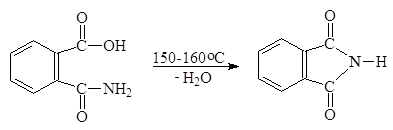 (63)
(63)
фталамовая кислота фталимид
Синтез фталимида из фталевого ангидрида, таким образом, сводится к следующей схеме:
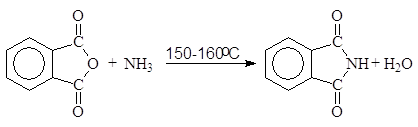 (64)
(64)
Аналогичным образом из ангидрида янтарной кислоты получают сукцинимид:
 (65)
(65)
ангидрид янтарной кислоты сукцинимид
Бромированием сукцинимида в разб. H2SO4 в присутствии NaBr в промышленности получают N-бромсукцинимид (NBS):
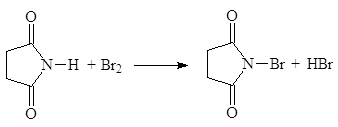 (66)
(66)
Ранее мы уже встречались с N-бромсукцинимидом (NBS), как реагентом аллильного и бензильного галогенирования.
3)
4)принцип:мочевина образуется с диацетилмонооксином в присутствии тиосемикарбазида из солей железа в кислой среде при нагревании комплекса красного цвета. Интенсивность окрашивания пропорционаольна определения мочевины.
Цель: снижение содержание мочевины в сыворотке отличается при паренхиматозтозном гипатите, циррозе, беременности. В моче при нефрите ацедозе, желтухе
Ход работы: в 3 пробирки вносят по 0,01 мл А сыворотки крови; Б-разведенная в 50 раз мочи; в- мочевина (16,65 ммоль/литр). В пробирки добавляют или по 0,2 мл рабочего раствора (ядовитый семикарбозит) и Н2SO4, перемещивают, закрывают крышкой, кипятят на водной бане больше 10 минут, охлаждают и коллометрируют при альфа=540нанометров.
Билет №12
1)
Транспортными формами аммиака являются глутамин, аланин, некоторое коли-
чество аммиака находится в крови в свободном виде. Глутамин и аланин являются
наиболее представленными, их доля среди всех аминокислот крови составляет до
50%. Большая часть глутамина поступает от мышц и мозга, аланин переносит ам-
миак от мышц и стенки кишечника.
Роль глутамина
Образование большого количества глутамина при обезвреживании аммиака
обеспечивает высокие концентрации этого вещества в крови (0,5-0,7 ммоль/л). Так
как глутамин проникает через клеточные мембраны путем облегченной диффузии,
то он легко попадает не только в гепатоциты, но и в другие клетки, где есть потреб-
ность в аминогруппах. Азот, переносимый глутамином, используется клетками для
синтеза пуринового и пиримидинового колец, гуанозинмонофосфата (ГМФ), аспара-
гина, глюкозамино-6-фосфата (предшественник всех остальных аминосахаров).
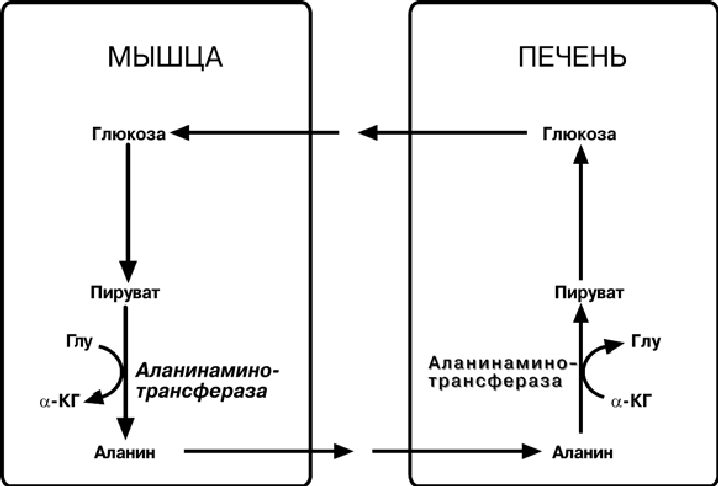
Глюкозо-аланиновый цикл
В мышцах основным акцептором лишнего аминного азота является пируват. При
катаболизме аминокислот в мышцах происходят реакции трансаминирования и об-
разуется аланин. Из мышц с кровью он переносится в печень, где передает свою
аминогруппу на глутамат. Образующийся пируват используется как субстрат в реак-
циях синтеза глюкозы. Далее глутаминовая кислота дезаминируется и аммиак ухо-
дит на синтез мочевины.
Целевыми органами для транспорта аммиака являются печень, почки и кишеч-
ник.
• в кишечнике часть глутамина дезаминируется, образованный аммиак выделяет-
ся в просвет кишечника (не более 5%), часть поступает в печень, около 90% – в
мочу;
• в печени происходит синтез мочевины;
• в почках идет образование аммонийных солей.
20
С И Н Т Е З М О Ч Е В И Н Ы
В печеночные клетки аммиак попадает в виде глутамина, глутаминовой кислоты,
аланина, в свободном виде. Кроме этого, при метаболизме он образуется в большом
количестве и в самих гепатоцитах. В печени весь аммиак используется для синтеза
мочевины. Увеличение синтеза мочевины наблюдается при распаде тканевых бел-
ков (голодание, избыточные физические нагрузки, сахарный диабет) или избыточном
белковом питании.
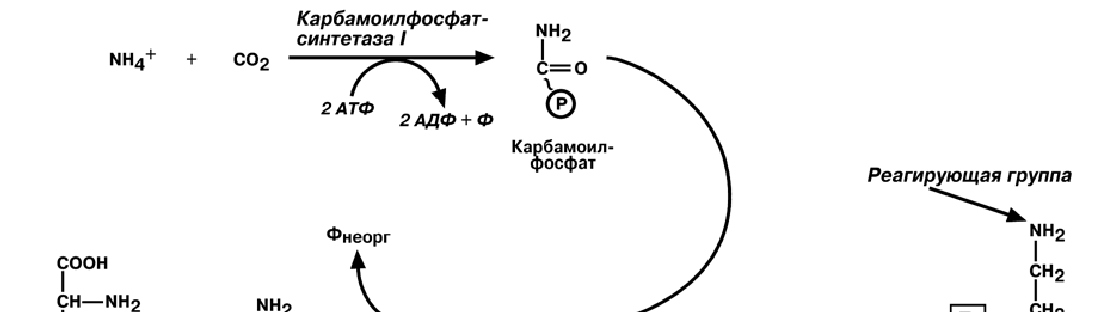
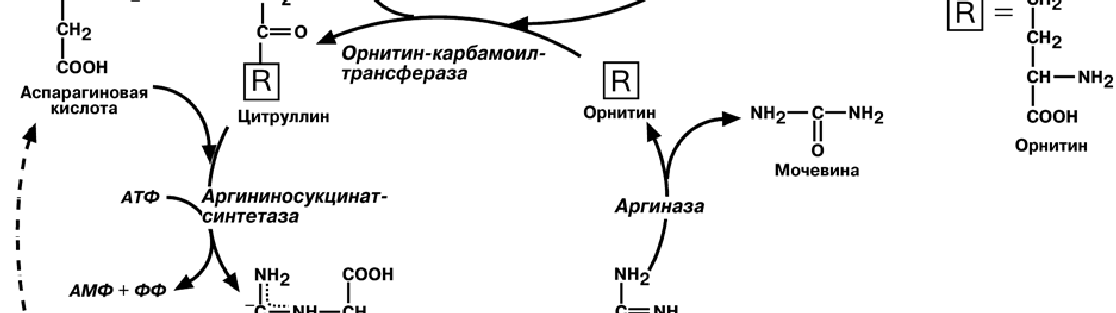
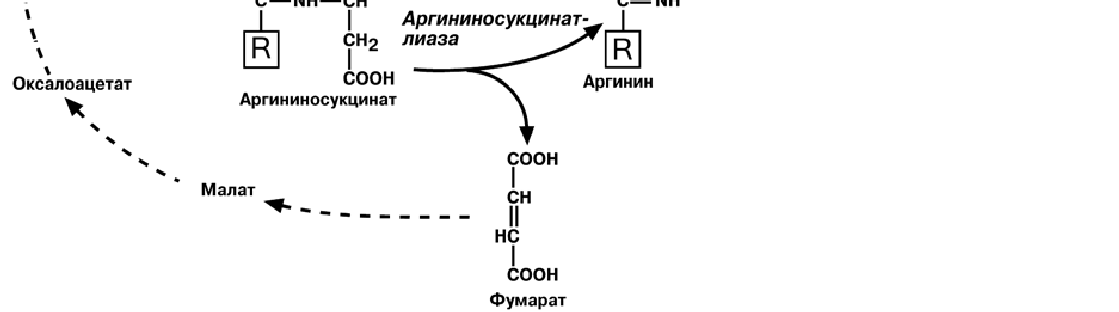
Реакции синтеза мочевины являются циклическим процессом и получили назва-
ние орнитиновый цикл.
Синтез мочевины начинается в митохондриях (первая и вторая реакции), ос-
тавшиеся три реакции идут в цитозоле. Для переноса цитруллина и орнитина через
митохондриальную мембрану существуют специальные переносчики.
В образовании одной молекулы мочевины участвует 1 молекула NH3, 1 молекула
CO2, аминогруппа 1 молекулы аспарагиновой кислоты, затрачивается 4 макроэрги-
ческих связи трех молекул АТФ.
2)
Обмен серосодержащих аминокислот
В состав белков человека входят 2 аминокислоты, содержащие серу, - метионин и цистеин. Эти аминокислоты метаболически тесно связаны между собой.
