
- •1)Азотистый баланс
- •1. Синтез 5'-фосфорибозиламина
- •Реакции синтеза амф и гмф
- •4. Образование нуклеозидтрифосфатов атф и гтф.
- •1) Главные компоненты желудочного сока
- •Реакция взаимопревращения глицина и серина
- •2) Распад пуриновых оснований
- •3) Регуляция синтеза белка
- •4) Обнаружение молочной кислоты в желудочном
- •1. Метаболизм феиилаланина
- •2. Особенности обмена тирозина в разных тканях
- •Механизм реакции синтеза дезоксирибонуклеотида
- •3. Реакция фосфорилирования
- •4) Определение свободной соляной кислоты
- •Окисление аланина
- •3) Синтез амидов из карбоновых кислот
- •1. Особенности обмена метионина
- •2. Обмен цистеина
- •4) Мочевая кислота сыворотки крови
- •Реакция синтеза глутаминовой кислоты
- •Реакция синтеза глутамина
- •Реакция синтеза аспарагина
- •Переваривание белков в желудочно-кишечном тракте
Механизм реакции синтеза дезоксирибонуклеотида
3. Реакция фосфорилирования
После образования dАДФ, dГДФ, dЦДФ фосфорилируются, а dУДФ используется для синтеза тимидилового нуклеотида.
4) Определение свободной соляной кислоты
в желудочном соке
Отклонения в составе пищеварительных соков или появление в
них компонентов, не содержащихся в физиологических условиях,
дают важную информацию о патологии пищеварения. В
клинической практике используют методы анализа желудочного
сока для диагностики и лечения заболеваний.
При анализе желудочного сока определяют его общее
количество, цвет, запах, наличие слизи, общую кислотность,
количество свободной и связанной соляной кислоты, присутствие
молочной кислоты, крови и желчных пигментов.
А. ПРИ ПОМОЩИ ИНДИКАТОРА «КОНГО КРАСНЫЙ»
Принцип
В присутствии свободной соляной кислоты в желудочном соке
индикатор «конго красный» меняет окраску на синюю, оставаясь в
нейтральной и щелочной среде красным (зона перехода рН 3,0-5,2).
Реактивы индикаторная бумага «конго красный»
Материал исследования
Нормальный и патологический желудочный сок.
Проведение анализа
На две разные полоски индикаторной бумаги наносят
стеклянной палочкой по 1 капле нормального и патологического
желудочного сока.
Б. ПРИ ПОМОЩИ ИНДИКАТОРА ДИМЕТИЛАМИНОАЗОБЕНЗОЛА
Принцип
Индикатор, п-диметиламиноазобензол, в присутствии
свободной соляной кислоты, имеет красную окраску, в щелочной
среде – желтую (зона перехода рН 2,3-4,2).
Реактивы
Индикатор п-диметиламиноазобензол.
Материал исследования
Нормальный и патологический желудочный сок.
Проведение анализа
В две пробирки вносят по 10 капель исследуемого желудочного
сока, добавляют по 2 капли п-диметиламиноазобензола.__
Билет №10
1)
Регуляция синтеза белка осуществляется на всех этапах этого процесса: транскрипции, трансляции и посттрансляционной модификации либо путем индукции, либо путем репрессии.
При отсутствии индуктора система не функционирует, поскольку "свободный" от индуктора – лактозы – репрессор соединен с оператором. В этом случае фермент РНК-полимераза не может катализировать процесс синтеза иРНК. Если в клетке оказывается лактоза (индуктор), она, взаимодействуя с репрессором, изменяет его структуру, в результате чего репрессор освобождает оператор. РНК-полимераза соединяется с промотором, начинается синтез иРНК (транскрипция структурных генов). Затем на рибосомах формируются белки по программе иРНК-лактозного оперона. У прокариотических организмов на одну молекулу иРНК переписывается информация со всех структурных генов оперона, т.е. оперон – это единица транскрипции. Транскрипция продолжается до тех пор, пока в цитоплазме клетки сохраняются молекулы лактозы. Как только все молекулы будут клеткой переработаны, репрессор закрывает оператор, синтез иРНК прекращается.
Таким образом, синтез иРНК и, соответственно, синтез белка должны строго регулироваться, поскольку у клетки недостаточно ресурсов для одновременной транскрипции и трансляции всех структурных генов. И про-, и эукариоты постоянно синтезируют только те иРНК, которые необходимы для выполнения основных клеточных функций Экспрессия остальных структурных генов осуществляется под строгим контролем регуляторных систем, запускающих транскрипцию только в том случае, когда возникает потребность в определенном белке (белках).
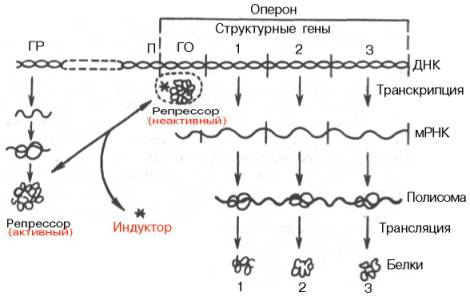 индукция
индукция
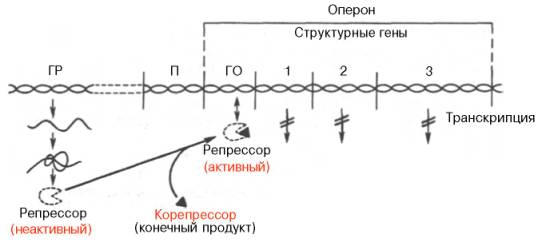 репрессия
репрессия
2)Распад пиримидинов начинается с отщепления 5’-фосфатной группы от ЦМФ, УМФ и ТМФ. Это осуществляет фермент 5’-нкуклеотидаза, локализованный на цито-плазматической мембране. Образующиеся продукты (цитидин, уридин и тимидин) включаются в ряд простых реакций, результатом которых является образование β-аланина и β-аминоизомасляной кислоты (рис.19.). Далее эти вещества вовлекаются в реакции трансаминирования, их углеродный скелет сгорает в ЦТК.
Некоторая часть β-аминоизомасляной кислоты удаляется через почки, что имеет клиническое значение: увеличение экскреции ее почками наблюдается при повыше-нии деструкции ДНК, например при лейкемии, после рентгеновского облучения.
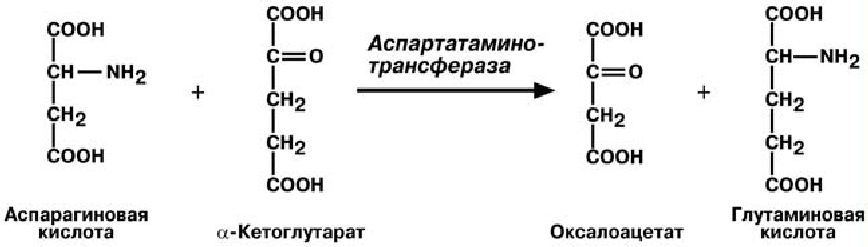
3) Более 2/3 аминоазота аминокислот приходится на долю глутамата и его производных; эти аминокислоты доминируют в количественном отношении в мозге всех изученных видов животных. В спинном мозге наблюдается аналогичная картина, а периферическая нервная система содержит значительно меньше глутамата, глутамина, N-ацетиласпартата, чем головной мозг, а ГАМК почти отсутствует в периферических нервах позвоночных. При высоком уровне этих аминокислот в головном мозге метаболизм их также чрезвычайно быстрый.
Трансаминирование
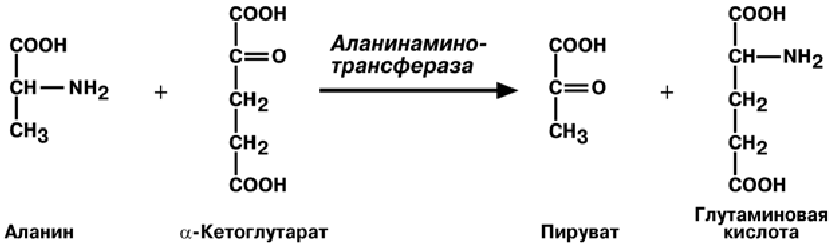
4) Нуклеопротеины можно извлечь из разрушенных дрожжевых клеток при щелочной реакции раствора и осадить при его окислении. Прилить (14 слайд) в ступку 30 мл раствора едкого натра 0,4 % и продолжать растирание в течение 15-20 мин. Перелить содержимое ступки в центрифужные пробирки, уравновесить и центрифугировать в течение 10-15 мин. Центрифугат слить в стаканчик и, непрерывно помешивая палочкой, прилить из пипетки раствор уксусной кислоты 5% (12-15 мл) до полного осаждения нуклеопротеина. Полученный нуклеопротеин используется для гидролиза. а) Биуретовая проба на полипептиды.
К 1 мл гидролизата прибавить 0,5 мл 10% едкого натра и несколько капель 1% раствора медного купороса. Жидкость окрашивается в розовый цвет.
б) Серебряная проба на пуриновые основания.
К 1 мл гидролизата прилить 5 капель 2% аммиачного раствора азотнокислого серебра. При стоянии через 3-5 минут выпадает небольшой бурый осадок серебряных соединений пуриновых оснований.
в) Качественная реакция Молиша на углевод (пентозу).
К 10 каплям гидролизата дрожжей добавить 2-3 капли 1% алкогольного раствора тимола, перемешать и по стенке пробирки осторожно спустить равный объем концентрированной серной кислоты. Образуется красное окрашивание вследствие образования продукта конденсации фурфурола с тимолом.
г) Молибденовая проба на фосфорную кислоту.
К 5 каплям гидролизата прилить 5 капель молибденового реактива (раствор молибденовокислого аммония в азотной кислоте) и кипятить несколько минут. Жидкость окрашивается в лимонно-желтый цвет. При охлаждении образуется желтый кристаллический осадок комплексного соединения фосфорно-молибденовокислого аммония.
Билет №11
1)
Нарушение обмена пиримидиновых оснований
Так как продукты катаболизма пиримидинов хорошо растворимы, то при избы-точном образовании и распаде их клинические симптомы слабо выражены. К подоб-ному нарушению можно отнести β-аминоизобутиратацидурию – дефект соответст-вующей трансаминазы. Заболевание протекает бессимптомно и встречается, в основ-ном, у японцев и китайцев (около 25%).
Большее клиническое значение имеет нарушение синтеза пиримидинов. Сюда относится оротатацидурия, которая может быть как наследственной, так и приобре-тенной.
Наследственная форма связана с одновременным дефектом оротатфосфорибо-зилтрансферазы и оротидилдекарбоксилазы, так как эти ферменты являются двумя активными центрами одного белка (рис.14) – оранжевая кристаллоурия. Заболевание проявляется мегалобластической анемией, отставанием развития, диагноз ставится при обнаружении в охлажденной моче оранжевых игольчатых кристаллов оротовой кислоты. Болезнь осложняется тем, что в отсутствие УТФ (и ЦТФ) активизируются первые реакции синтеза оротата. При отсутствии лечения гибель наступает в первые годы жизни. Однако, так как первопричиной заболевания является «пиримидиновый голод», его можно достаточно успешно корректировать с помощью приема уридина, при этом серьезно не опасаясь передозировки.
Приобретенная форма оротацидурии может наблюдаться:
при дефекте каких-либо ферментов синтеза мочевины, кроме карбамоилсинтета-зы. При этом карбамоилфосфат митохондрий (в норме идущий на образование мочевины) выходит из них и используется для избыточного синтеза оротовой ки-слоты. Заболевание обычно сопровождается гипераммониемией.
при лечении подагры аллопуринолом, который превращается в оксипуринолмо-нонуклеотид, являющийся ингибитором оротаткарбоксилазы, что опять же ведет к накоплению оротата.
Нарушение обмена пуриновых оснований
Выделяют три основных нарушения обмена пуринов: подагра (хроническая ги-перурикемия), мочекаменная болезнь и синдром Леша-Нихана.
Подагра
Если образование мочевой кислоты в организме превышает ее выведение, то развивается состояние называемое гиперурикемия. Когда гиперурикемия принимает хронический характер, говорят о наличии подагры. В крови мочевая кислота нахо-дится в форме ее солей – уратов натрия. Растворимость уратов в плазме крови неве-лика и при превышении порога растворимости в плазме образуются кристаллы. Они откладываются в мягких тканях, суставах, образуя тофусы – подагрические узлы в мелких суставах, сухожилиях, хрящах, коже. Накапливающиеся в межклеточном ве-ществе ураты некоторое время фагоцитируются, однако, фагоциты не способны раз-рушить пуриновое кольцо. В конце концов, это приводит к гибели самих фагоцитов, к выходу лизосомальных ферментов и развитию острой воспалительной реакции – раз-вивается подагрический артрит. В 50-75% случаев первым признаком заболевания яв-ляется мучительная ночная боль в больших пальцах ног.
Подагрой страдает 0,3-1,7% взрослого населения земного шара, соотношение за-болевших мужчин и женщин составляет 20 : 1.
Длительное время подагру считали «болезнью гурманов», однако в настоящее время внимание исследователей переместилось к изменению активности ферментов метаболизма пуринов:
• увеличение активности ФРПФ-синтетазы – приводит к избыточному синтезу пу-ринов
• уменьшение активности гипоксантин-гуанин-фосфорибозил-трансферазы (ГГФРТФ) – из-за этого ФРПФ не используется в связывании азотистых оснований, а уходит в первую реакцию синтеза пуринов. В результате возрастает количе-ство разрушающихся пуринов и одновременно повышается их образование.
Оба этих нарушения рецессивны и сцеплены с X-хромосомой.
Лечение подагры сводится к снижению поступления предшественников мочевой кислоты с пищей и уменьшению ее образования в организме. Это подразумевает со-блюдение строжайшей диеты на протяжении весьма длительного времени, исключе-ния из рациона продуктов, содержащих много пуриновых оснований – кофе, чай, шо-колад, мясные продукты, печень, красное вино. К лекарственным средствам лечения подагры относят аллопуринол, по струк-туре схожий с гипоксантином. Ксанти-ноксидаза окисляет аллопуринол в аллок-сантин, а последний остается прочно свя-занным с ферментом и подавляет его ак-тивность. Происходит, образно говоря, самоубийственное ингибирование. Как след-ствие, ксантин не превращается в мочевую кислоту, а гипоксантин и ксантин лучше растворимы в воде, и они более легко выводятся из организма с мочой.
Кроме аллопуринола используют препараты, увеличивающие выведение моче-вой кислоты почками – антуран, цинхофен.
Мочекаменная болезнь
Мочекаменная болезнь заключается в образовании кристаллов (камней) в моче-выводящих путях. Вообще кристаллы могут иметь различную природу: 70-75% боль-ных мочекаменной болезнью имеют камни щавелевой кислоты (оксалаты), 15% – мо-чевой кислоты, 10% – кальций-фосфатные, карбонатные, цистиновые камни.
Примерно у половины больных подагрой в мочевыводящих путях откладывают-ся мочевые камни. Особенно они представлены в дистальных канальцах и собира-тельных трубочках. Причиной отложения кристаллов мочевой кислоты является ги-перурикемия и повышенное выведение уратов с мочой. Особенно возрастает количе-ство камней при закислении мочи в результате питания животной пищей, которая со-держит большое количество неорга-нических кислот и является «ки-слой». Дело в том, что при ней-тральных и щелочных значениях рН мочевая кислота находятся в форме уратов (енольная форма), а при сни-жении рН до 5,75 переходят в кето-форму мочевой кислоты, которая в 17 раз хуже растворима по сравнению с ее солями. Учитывая, что даже нормальная рН мочи лежит в диапазоне 5,3-6,5 легко представить, сколько мочевой кислоты спо-собно кристаллизоваться в почечных канальцах.
Лечение заболевания, как при подагре сводится к ограничению поступления пу-риновых оснований и предовращению образования мочевой кислоты. В дополнение рекомендуется растительная диета, приводящая к защелачиванию мочи, что увеличи-вает долю более растворимых в воде уратов.
Синдром Леша-Нихана
Болезнь Леша-Нихана – это полное врожденное отсутствие активности гипок-сантин-гуанин-фосфорибозил-трансферазы, фермента отвечающего за реутилизацию пуриновых оснований. Признак рецессивный и сцеплен с Х-хромосомой. Впервые его описали в США студент-медик Майкл Леш и педиатр Уильям Нихан в 1964 г.
Дети рождаются клинически нормальными, только к 4-6 месяцу обнаруживают-ся отклонения в развитии, а именно отставание физического развития (с трудом дер-жит голову), повышенная возбудимость, рвота, периодическое повышение тмперату-ры. Выделение мочевой кислоты можно обнаружить еще раньше по оранжевой окра-ске пеленок. К концу первого года жизни симптомы драматически нарастают, разви-вается нарушение координации движений, хореоатеоз, корковый паралич, спазм мышц ног. Наиболее характерный признак заболевания проявляется на 2-3-м году жизни – аутоагрессия, самокалечение – неодолимое стремление детей кусать себе гу-бы, язык, суставы пальцев на руках и ногах
2) Когда в пищеварительном тракте или в эксперименте белки расщепляются на более простые соединения, то через ряд промежуточных стадий (альбумоз и пептонов) они расщепляются на полипептиды и, наконец, на аминокислоты. Аминокислоты в отличие от белков легко всасываются и усваиваются организмом. Они используются организмом для образования собственного специфического белка. Если же вследствие избыточного поступления аминокислот их расщепление в тканях продолжается, то они окисляются до углекислого газа и воды. В митохондриях пировиноградная кислота - промежуточный продукт, образовавшийся в анаэробной фазе - окисляется до СО2 в шести последовательных реакциях, в каждой из которых пара электронов переносится на общий акцептор - кофермент никотинамидадениндинуклеотид (НАД). Эту последовательность реакций называют циклом трикарбоновых кислот, циклом лимонной кислоты или циклом Кребса. Из каждой молекулы глюкозы образуется 2 молекулы пировиноградной кислоты; 12 пар электронов отщепляется от молекулы глюкозы в ходе ее окисления, описываемого уравнением:
![]() <=""
div="">
<=""
div="">
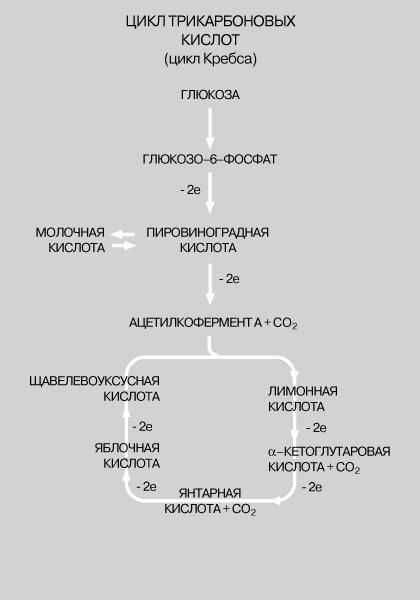 У
ЧЕЛОВЕКА И ДРУГИХ ЖИВОТНЫХ главным
источником энергии служит окисление
глюкозы в тканях. Расщепление глюкозы,
протекающее через ряд этапов, приводит
к образованию соединения, называемого
ацетилкоферментом А. С него начинается
цикл реакций, непрерывно подпитываемый
новыми порциями ацетилкофермента А. В
ключевых точках этого процесса происходит
выделение энергии с переносом двух
электронов (на схеме -2e означает, что
данная реакция идет с выделением
энергии).
У
ЧЕЛОВЕКА И ДРУГИХ ЖИВОТНЫХ главным
источником энергии служит окисление
глюкозы в тканях. Расщепление глюкозы,
протекающее через ряд этапов, приводит
к образованию соединения, называемого
ацетилкоферментом А. С него начинается
цикл реакций, непрерывно подпитываемый
новыми порциями ацетилкофермента А. В
ключевых точках этого процесса происходит
выделение энергии с переносом двух
электронов (на схеме -2e означает, что
данная реакция идет с выделением
энергии).
