
- •Карбоксильная группа
- •Реакции подлинности
- •Количественное определение
- •Сложноэфирная и амидная группы
- •Химические свойства
- •Реакции подлинности
- •Количественное определение
- •Азометиновая группа
- •Первичная алифатическая аминогруппа
- •Количественное определение
- •Ароматическая нитрогруппа Химические свойства
- •Количественное определение
- •Вторичная аминогруппа Химические свойства
- •Реакции подлинности
- •Количественное определение
- •Вторичная аминогруппа в составе имидной, сульфамидной, гидразидной функциональных групп и в некоторых гетероциклических соединениях
- •Химические свойства
- •Реакции подлинности
- •Количественное определение
- •Третичный и четвертичный атом азота
- •Химические свойства
- •Реакции подлинности
- •Количественное определение
- •Ковалентно связанный галоген
- •Подлинность
- •Количественное определение
- •Ковалентно связанная сера
- •Подлинность
- •Ковалентно связанный азот
Ковалентно связанный галоген
Ковалентно связанный галоген – это галоген, входящий в структуру молекулы органического вещества и связанный ковалентной связью с атомом углерода. По природе галогена различают фтор – (галотан (фторотан), фторурацил и др. ); хлор – ( хлорэтил, хлоралгидрат), бром – (бромизовал, бромкамфора и др.) и йодсодержащие ЛВ (йодоформ, тиреоидин, лиотиронин (трийодтиронин).
Поскольку атомы галогенов с органической частью молекулы связаны не ионогенно, для их обнаружения вещество необходимо минерализировать, то есть разрушить связь галогена с углеродом и перевести ковалентно связанный галоген в ионогенное состояние. Выбор метода минерализации определяется прочностью связи углерод - галоген (она падает от фтора к йоду), строением галогенсодержащего ЛВ (алифатического, ароматического, гетероциклического ряда) и может осуществляться несколькими способами:
непосредственное взаимодействие с реагентом (йодоформ с раствором серебра нитрата в азотнокислой среде);
гидролитическое расщепление водным (бромизовал) или спиртовым (хлорэтил) раствором щелочи (галогенсодержащие ЛВ алифатического ряда);
восстановительная минерализация водородом в момент выделения (Zn + NaOH, Zn + CH3COOH) или металлическим натрием (для фторпроизводных):
сжигание в колбе с кислородом (для всех галогенсодержащих веществ);
прокаливание со смесью для спекания (для всех, кроме фторсодержащих);
проба Бейльштейна;
4) окислительная минерализация (только для йодсодержащих веществ);
“сухая” (нагревание без реактивов);
”мокрая” (нагревание с концентрированной серной кислотой);
Подлинность
Состоит из двух стадий:
минерализация ковалентно связанного галогена;
доказательство галогенид-иона или галогена обычными аналитическими реакциями.
П
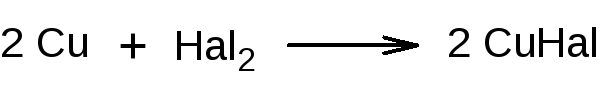
 роба
Бейльштейна.
Основана на образовании летучих
галогенидов меди, окрашивающих пламя
горелки в зеленый (йод) или голубовато-зеленый
(хлор, бром) цвет.
роба
Бейльштейна.
Основана на образовании летучих
галогенидов меди, окрашивающих пламя
горелки в зеленый (йод) или голубовато-зеленый
(хлор, бром) цвет.
Проба Бейльштейна очень чувствительна, но является косвенным методом доказательства галогена, т.к. не позволяет определить природу галогена и анализировать фторсодержащие ЛВ, поскольку фторид меди не летуч.
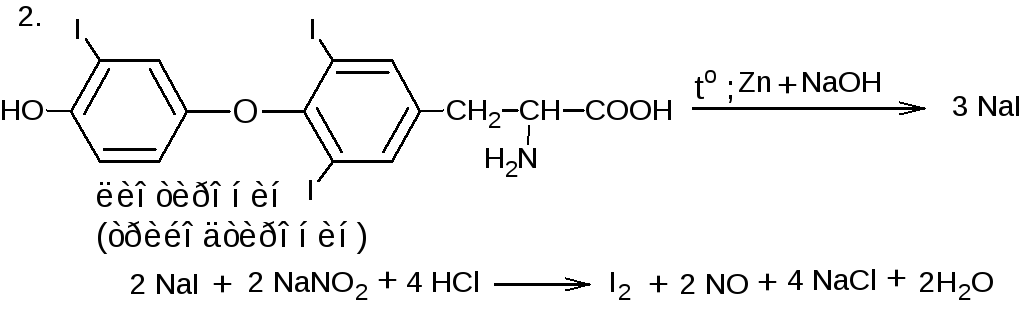
Ковалентно связанный йод доказывают методом окислительной минерализации (“сухой” или “мокрой”); выделяются фиолетовые пары йода.
Методика. 1.Нагревают 0,1 г йодоформа в сухой пробирке.
2.Нагревают 0,1г лиотиронина (трийодтиронина) или тиреоиодина в пробирке с 1 мл концентрированной серной кислоты.
Методы восстановительной минерализации:
3.1. Металлическим натрием для фторсодержащих ЛВ.
Вследствие высокой прочности связи фтор-углерод минерализацию проводят действием сильного восстановителя – металлического натрия при нагревании. Образующийся фторид-ион доказывают косвенно по разрушению цирконий - ализаринового красителя вследствие связывания Zr+4 в более прочный комплекс с фторидом, при этом окраска раствора изменяется от красно-фиолетовой до желтой. Способ используется для обнаружения фтора в галотане (фторотане), фторурациле, тегафуре (фторафуре), фторхинолонах и др.
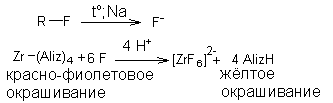
3.2. Прокаливание со смесью для спекания (KNO3, Na2CO3)
3.3. Водородом в момент выделения (Zn + NaOH, Zn + CH3COOH)
Варианты 3.2. и 3.3. используются для алифатических, алициклических, ароматических и гетероциклических ЛВ, содержащих йод, бром и хлор. Образующиеся галогенид - ионы доказывают реакциями:
а) реакцией осаждения серебра нитратом в азотнокислой среде;
б) окислением бромидов (хлорамином Б в кислой среде) и йодидов (натрия нитритом или железа (Ш) хлоридом в кислой среде соответственно до брома и йода, которые извлекают в хлороформный слой. Бром окрашивает хлороформ в желто-бурый цвет, йод в розовый или фиолетовый.
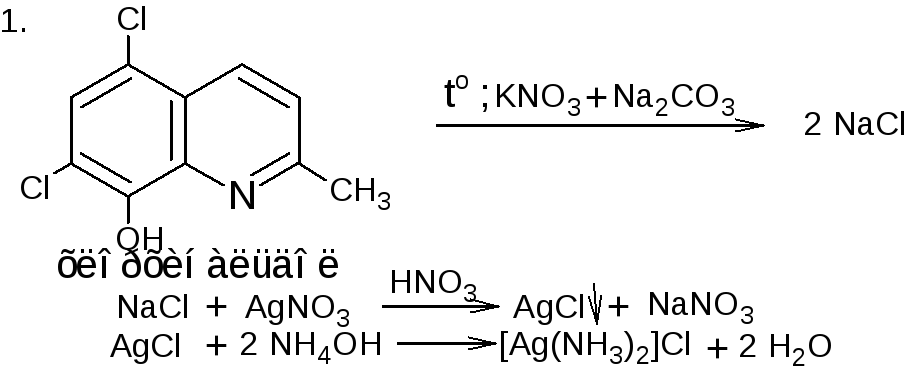
Методика. 0,1 г хлорхинальдола кипятят с 2 мл раствора натрия гидроксида и 0,2 г цинковой пыли в течение 3 мин., охлаждают, фильтруют. К фильтрату прибавляют разв. азотную кислоту до кислой реакции среды, 0,5 мл раствора серебра нитрата; образующийся белый творожистый осадок растворим в растворе аммония гидроксида.
4. Гидролитическое разложение для ЛВ, содержащих галоген в алифатической цепи (кроме фтора) проводят при нагревании с водным (бромизовал) или спиртовым (хлорэтил) раствором щелочи, образующийся галогенид-ион доказывают обычными аналитическими реакциями.
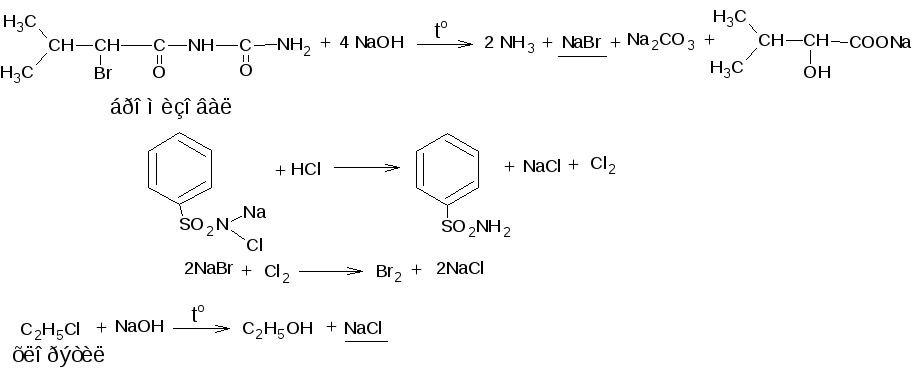
Методика. 0,1 г бромизовала кипятят с 3 мл раствора натрия гидроксида в
течение 3 мин., охлаждают, прибавляют разведенной хлороводородной кислоты до кислой реакции среды, 0,5 мл раствора хлорамина, 1 мл хлороформа и взбалтывают. Хлороформный слой окрашивается в желто-бурый цвет.
