
Frantzajdes_K._Laparoskopicheskaya_i_torakoskopicheskaya_xirurgiya_(BINOM,_2000)(ru)(ISBN_5798901718)(317s)
.pdf
^ ^ ^ ^
222 |
Глава 13 |
Таблица 13.1. Частота развития инфекционно-гнойных осложнений после «открытой» холецистэктомии в тех случаях, когда антибиотикопрофилактика не проводилась (данные рассчитаны в зависимости от наличия факторов риска)
Факторы риска * |
Число пациентов |
Абсолютное число |
Частота развития |
|
|
инфекционно- |
инфекционно- |
|
|
гнойных осложнений |
гнойных осложнений |
|
|
|
|
Точно не определены |
931 |
119 |
12,8% |
Имеются |
97 |
20 |
20,6% |
Отсутствуют |
81 |
10 |
12,3% |
*В группу риска входят пациенты старше 65—70 лет с осложненной желчно-каменной болезные
Таблица |
13.2. Проспективные |
исследования, |
посвященные |
антибиотикопрофилактике |
||||
|
в хирургии желчевыводящих путей: частота возникновения |
|||||||
|
инфекционно-гнойных осложнений в группах пациентов, получающих |
|||||||
|
плацебо (пациенты не разделены |
на группы |
в зависимости |
|||||
|
от |
наличия или |
отсутствия |
факторов риска) |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Инфекционно- |
|
|
|
|
|
|
|
|
гнойные осложнениям |
|
|
|
|
|
|
|
|
|
|
|
Автор |
Год |
Антибиотик |
Количество |
|
|
Абсолют |
Частота |
Факторы |
|
|
|
обследованных |
|
ное число |
|
риска* |
|
|
|
|
пациентов |
|
|
случаев |
|
|
|
|
|
|
|
|
|
|
|
Keighley |
1975 |
Плацебо |
50 |
|
|
И |
22,0% |
Смешанная |
|
|
|
|
|
|
|
|
группа |
Strachan |
1977 |
Плацебо |
65 |
|
6 |
9,2% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
Morran |
1978 |
Плацебо |
47 |
|
10 |
21,3% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
Halsam |
1980 |
Плацебо |
59 |
|
3 |
5,1% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
Karran |
1981 |
Плацебо |
20 |
|
3 |
15,0% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
Elke |
1983 |
Плацебо |
165 |
|
17 |
10,3% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
McArdle |
1983 |
Плацебо |
98 |
|
13 |
13,3% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
Sykes |
1984 |
Плацебо |
33 |
|
2 |
6,1% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
Kaufman |
1984 |
Плацебо |
50 |
|
12 |
24,0% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
Kune |
1985 |
Плацебо |
92 |
|
2 |
2,2% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
KauiTman |
1986 |
Плацебо |
74 |
|
10 |
13,5% |
Смешанная |
|
|
|
|
|
|
|
|
|
группа |
см. продолжение

Антибиотикопрофилактика в лапароскопической хирургии |
223 |
Таблица 13.2. (продолжение)
*В группу риска входят пациенты старше 65—70 лет с осложненной желчно-каменной болезнью. Утверждение «факторы риска отсутствуют» указывает на то, что в исследуемую группу включены только те пациенты, у которых перечисленные факторы риска отсутствуют. В смешанные группы входят все пациенты (без разделения по категориям)
Таблица 13.3. Проспективные исследования, посвященные антибиотикопрофилактике в хирургии желчных путей: частота возникновения инфекционногнойных осложнений в группах пациентов, получающих плацебо (только у пациентов группы риска)*
|
|
|
|
Инфекционно-гнойные |
|
|
|
|
|
осложнения |
|
|
|
|
|
|
|
Автор |
Год |
Антибиотик |
Количество |
Число |
Процент |
|
|
|
обследованных |
случаев |
|
|
|
|
пациентов |
|
|
|
|
|
|
|
|
Cainzos |
1985 |
Плацебо |
25 |
7 |
28,0% |
Lewis |
1987 |
Плацебо |
42 |
9 |
21,4% |
Bolufer |
1987 |
Плацебо |
30 |
4 |
13,3% |
|
|
|
97 |
20 |
20,6% |
|
|
|
|
|
|
* В группу риска входят пациенты старше 65 лет с осложненной желчно-каменной болезнью.
Недостаток публикаций, посвященных инфекционно-гнойным осложнениям в лапа роскопической хирургии, объясняется тем, что в процессе развития этой новой методики основное внимание уделялось технической стороне проблемы, а не редким случаям воз никновения раневой инфекции. Как показали исследования, целью которых являлось изу чение инфекционно-гнойных осложнений, частота развития раневой инфекции обычно оказывалась заниженной, если не производилась проспективная оценка результатов не зависимым исследователем [19,20]. Обычно врачи не сообщают о 30-50% развивающихся инфекционно-гнойных осложнений [20].
Все вышеперечисленные факторы позволяют поднять вопрос о различиях между 1«открытыми» и лапароскопическими операциями в том, что касается возможности бак-
224 |
Глава 13 |
териального загрязнения тканей. Не возникает сомнений, что короткий период выздо ровления после лапароскопических операций (в отличие от «открытых») обусловлен ми нимальной травматичностью этих вмешательств. Степень травматичности операции не посредственно связана с частотой возникновения инфекционно-гнойных осложнений в послеопрационном периоде [21]. «Открытые» операции характеризуются большими раз резами, которые приводят к бактериальному инфицированию обширных участков в норме стерильных тканей. Лапароскопические операции, напротив, характеризуются маленьки ми разрезами; следовательно, площадь контакта тканей с внешней средой уменьшается, и вероятность инфицирования снижается. Однако иногда во время лапароскопических операций из брюшной полости через очень маленькие разрезы с усилием извлекают ин фицированные препараты, что является потенциальным фактором риска загрязнения ран.
Было бы интересным провести проспективные исследования, чтобы выявить, при каких из многочисленных разрезов, используемых во время лапароскопических операций, раневая инфекция развивается наиболее часто. Существуют доказательства, что после лапароскопической холецистэктомий чаще всего возникает нагноение околопупочного разреза.
В отличие от тканей брюшной стенки, на органы и ткани брюшной полости во время лапароскопических операций оказывается воздействие, аналогичное воздействию во время «открытых» операций. При этом благодаря увеличивающему эффекту лапароско пической оптики возможен даже более тщательный гемостаз. Мелкие сосуды, на которые во время «открытых» операций обычно не обращают внимания, во время лапароскопии тщательно коагулируют. Тем не менее, не все отделы брюшной полости (а особенно забрюшинное пространство) можно осмотреть с помощью лапароскопа так же хорошо, как и при «открытой» операции. Поэтому можно сделать заключение, что риск развития внутрибрюшинных инфекционно-гнойных осложнений после лапароскопических и «от крытых» операций приблизительно одинаков; например, после «открытой» резекции тол стой кишки внутрибрюшные гнойные осложнения развиваются в 6,5% случаев (при от сутствии антибиотикопрофилактики) [22].
По данным исследования Смита (Smith E.B.) [1], который проанализировал резуль таты 1009 лапароскопических холецистэктомий, частота развития перитонита после этих операций более чем в два раза превысила частоту развития раневой инфекции (рис. 13.1). Несмотря на то, что применение антибиотиков может уменьшить частоту возникновения раневых инфекций, профилактика перитонита в большей степени относится к техничес кой стороне выполнения операции, а не к антимикробному воздействию в послеопера ционном периоде. Брюшная полость обладает высокоэффективной системой защиты, ко торая позволяет противостоять даже выраженному бактериальному обсеменению, если оно не сопровождается постоянным поступлением бактерий из кишки (например, при несостоятельности межкишечного анастомоза) [23].
К другим проблемам лапароскопических операций относится слишком частое или неправильное использование протезов, например, сетки Марлекса (Marlex) для грыжепластики [24]. Наличие инородных тел в операционной ране благоприятствует развитию инфекции, так как в таких случаях для подавления защитных механизмов реципиента требуется значительно меньшее бактериальное обсеменение. Инфицирование марлексных протезов приводит к развитию хирургических осложнений, которые трудно поддаются лечению и характеризуются тяжелым течением и высокой летальностью [3, 5, 21]. Чаще всего на инородных телах в ранах вегетируют стафиллококки, вырабатывающие и не вырабатывающие коагулазу. В настоящее время профилактика стафиллококковой инфек ции осуществляется во всех случаях, когда производится имплантация инородного ма териала, хотя убедительные проспективные контролируемые исследования, посвященные этой проблеме, пока еще не проводились.

Антибиотикопрофилактика в лапароскопической хирургии |
225 |
|
|
|
|
Осложнения
Повреждение |
Перитонит |
Раневая |
Кровотечение |
желчных |
|
инфекция |
|
протоков |
|
|
|
Рис. 13.1. Осложнения, развивающиеся после лапароскопической холецистэктомии (по данным обследования 1009 пациентов, выполненного Earl Smith [1]). Частота развития раневой инфекции оказалась ниже, чем частота повреждений желчных протоков или развития перитонита; это позволяет предположить, что частота развития раневой инфекции либо была занижена, либо ей не придавали большого значения
ОСНОВНЫЕ ПРИНЦИПЫ АНТИБИОТИКОПРОФИЛАКТИКИ
Основные принципы антибиотикопрофилактики при лапароскопических и традици онных открытых операциях одинаковы. Они основаны на определении так называемого «уязвимого периода» (по Мэйлсу [Males] и Бурке [Burke]), на протяжении которого при менение антибиотиков с профилактической целью оказывается наиболее эффектив ным [25, 26]. Такая точка зрения была подтверждена в ходе многих проспективных ран домизированных исследований. Антибиотики следует назначать до начала операции, что дает им время для проникновения из крови в периферические ткани, в частности, в тка невую жидкость, поступающую в операционную рану. При этом необходимо создать такую концентрацию антибиотиков в тканях, которая оказывала бы бактерицидный эф фект, т. е. препятствовала выживанию и размножению бактерий. Практически это озна чает, что к началу операции концентрация антибиотиков в тканях должна превышать минимальную бактерицидную концентрацию. Если антибиотики ввести раньше, чем сле дует, то в самый необходимый момент они могут быть уже выведенными из организма и отсутствовать в тканях во время «уязвимого периода» (когда стерильные ткани после разреза подвергаются воздействию загрязненной окружающей среды) (рис. 13.2). Если антибиотики назначают за 1 час до начала операции, то после введения их в кровь они в течение 30-60 минут попадают в периферические ткани (тканевую жидкость), где их концентрация увеличивается по мере снижения их концентрации в крови. Когда концент-
8 Зак. 799

226 |
I лава 13 |
Рис. 13.2. Во время «открытой» операции «уязвимый период» представляет собой то время, когда стерильные ткани подвергаются воздействию загрязненной окружающей среды. Время назначения антибиотиков с профилактической целью следует подбирать таким образом, чтобы к началу операции в периферических тканях концентрация препарата достигала максимального уровня, что происходит через 30-60 минут после его введения в кровь. По мере насыщения антибиотиком крови он начинает поступать в периферические ткани (или раневую жидкость). Когда концентрация препарата в раневой жидкости достигает своей «точки насыщения», он начинает всасываться обратно в кровь, откуда удаляется почками пли печенью. В идеальном варианте разрез не следует выполнять до тех пор, пока не произойдет накопления антибиотика в периферических тканях (что обычно происходит через 30-60 минут после его введения в кровь)
рация антибиотиков в тканевой жидкости достигает своей «точки насыщения», они на чинают всасываться обратно в кровь, откуда удаляются почками или печенью. Таким образом, операцию следует выполнять в то время, когда концентрация антибиотиков в периферических тканях (раневой жидкости) наибольшая [27].
Для операций, продолжающихся менее 2 часов, достаточным оказывается предопе рационное введение одной дозы антибиотиков. Многократное введение антибиотиков повышает частоту развития инфекционных осложнений, так как подавляет раннюю ре акцию воспаления в тканях, необходимую для очищения раны [28]. Это было продемон стрировано в исследованиях, сравнивающих эффективность однократного и многократ ного введения антибиотиков: раневая инфекция развилась у 30 из 459 (6,6%) пациентов, которым до операции было введено более одной дозы антибиотиков, в отличие от 5,4% пациентов (26 из 486) из контрольной группы, антибиотикопрофилактика у которых ог раничивалась введением одной дозы препарата [27]. Для тех хирургов, которые не убеж дены в преимуществе однократного введения антибиотиков, следует подчеркнуть, что инъекция одной дозы препарата, по меньшей мере, так же эффективна, как и нескольких. Так зачем же зря тратить деньги и препараты? Антибиотики с длинным периодом полу выведения, такие как цефтриаксон, обычно не подходят для использования с профилак тической целью, так как их введение фактически эквивалентно инъекции нескольких доз антибиотиков с коротким периодом полувыведения [29].
При использовании антибиотиков с коротким периодом полувыведения введение второй дозы является целесообразным только в том случае, если операция продолжается более 4 часов. Короткий период полувыведения означает, что антибиотик выводится из организма быстро, поэтому по прошествии 4 часов его концентрация в тканях может быть уже недостаточной. Короткий период полувыведения имеют ампициллин/сульбактам, цефокситин, цефотаксим и все препараты пенициллинового ряда. С целью создания

Антибиотикопрофилактика в лапароскопической хирургии |
227 |
оптимальной концентрации препарата в тканях во время длительных операции повторная доза антибиотика вводится через 1-2 часа после первой, что вновь приводит к повышению его концентрации в тканевой жидкости (рис. 13.3) [29].
Бремя (в часах)
Рис. 13.3. Если операция длится более 4 часов, максимальная концентрация антибиотика в тканевой жидкости достигается путем последовательного введения двух доз препарата с коротким периодом полувыведения. На рисунке не указана концентрация антибиотика в сыворотке. Следует отметить, что вторая доза препарата вводится через 2 часа после первой для повышения его концентрации в тканях. Максимальное насыщение тканей при использовании антибиотика, период полувыведения которого составляет примерно 1 час (большинство бета-лактамных антибиотиков), происходит через 1-2 часа после введения ударной дозы препарата. Если вторая доза вводится через 6-8 часов после первой, то практически весь антибиотик оказывается уже выведенным из тканевой жидкости, что препятствует достижению в ней высокой концентрации препарата, как это происходит в случае введения поддерживающей дозы антибиотика через 2 часа
Бактерии
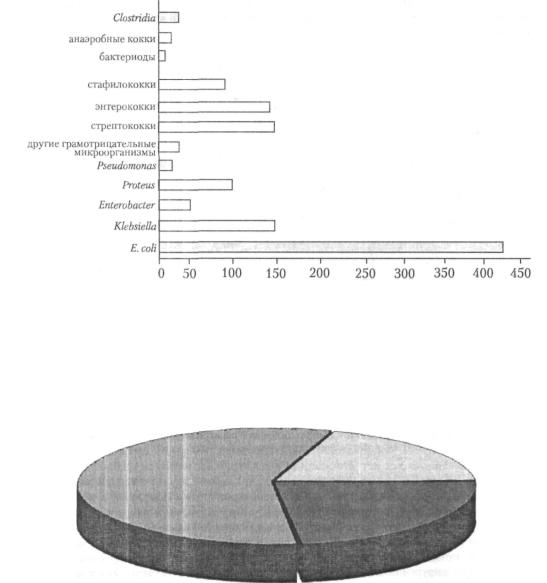
Как правило, антибиотики используются для профилактики развития раневой ин фекции. Их мишенью являются бактерии, попадающие в рану и вызывающие развитие воспалительного процесса. К сожалению, точная статистическая информация, касающая ся микроорганизмов, наиболее часто вызывающих развитие раневой инфекции, отсутст вует. Поэтому хирурги обычно ищут источник бактериального обсеменения раны и назна чают антибиотики широкого спектра действия. Результаты, полученные при бактериологи ческом исследовании желчи (всего было обследовано 3062 пациента) представлены на рисунке 13.4 и в табл. 13.4 [30-35]. В последующем не все эти микроорганизмы были высеяны из ран при развитии раневой инфекции. Пока еще остается неясным, в каких случаях микроорганизмы, выделенные из желчи, могут стать причиной развития раневой инфекции. Это зависит от многих факторов, в частности, патогенности бактерий, эффек тивности антибактериальной терапии в каждом конкретном случае, методики проведения бактериологических исследований и, наконец, наличия факторов риска. При обследова нии пациентов, которые умерли от сепсиса, причиной которого была инфекция желчевыводящей системы, установлено, что клиническое значение имеют только три микро организма — Е. coli, Clostridium perfringens и Pseudomonas aerugenosa (рис. 13.5).
228 |
Глава 13 |
Рис. 13.4. На рисунке представлены микроорганизмы, высеянные из желчи 3062 пациентов (обобщенные данные 6 крупных исследованияй). Этим пациентам были выполнены «открытые» операции на желчных путях. Три микроорганизма (заштрихованные прямоугольники на рисунке) можно назвать бактериями-убийцами (или наиболее агрессивными бактериями), так как они были выделены у пациентов, которые умерли от сепсиса. К ним относятся: Е. coli, Clostridium perfiingens И Pseudomonas aerugenosa. Наиболее часто у пациентов с раневой инфекцией и у пациентов, которые умерли от сепсиса, выделяли Е. coli
Е. coli |
Pseudomonas |
Clostridium perfringens
Рис. 13.5. Частота распределения бактерий-убийц (наиболее агрессивных бактерий)

Антибиотикопрофилактика в лапароскопической хирургии |
229 |
Таблица 13.4. Штаммы факультативных (аэробных) и облигатных (анаэробных) бактерий, наиболее часто высеваемых из желчи пациентов, перенесших «открытую» холецистэктомию
Микроорганизмы |
Количество |
Процент |
||
|
бактериологических |
|
|
|
|
исследований |
|
|
|
|
|
|
|
|
Аэробные |
|
|
|
|
Е. coli |
434 |
|
35% |
|
Klebsiella |
154 |
|
12% |
|
Enterobacter |
45 |
|
4% |
|
Proteus |
99 |
|
8% |
|
Pseudomonas |
19 |
|
2% |
|
Различные |
36 |
|
3% |
|
грамотрицательные |
|
|
|
|
факультативные бактерии |
|
|
|
|
Streptococcus |
162 |
|
13% |
|
Enterococcus |
159 |
|
13% |
|
Staphylococcus |
75 |
|
6% |
|
Всего аэробных |
1183 |
|
95% |
|
микроорганизмов |
|
|
|
|
Анаэробные |
|
|
|
|
В. fragilis |
9 |
|
1% |
|
Peptococcus |
9 |
|
1% |
|
Peptostreptococcus |
11 |
|
1% |
|
Clostridia |
29 |
|
2% |
|
Различные облигатные |
1 |
|
|
|
анаэробные бактерии |
|
|
|
|
Всего анаэробных |
65 |
|
5% |
|
микроорганизмов |
1248 |
|
|
|
Всего исследований |
|
100% |
|
|
|
|
|
|
|
ЛАПАРОСКОПИЧЕСКАЯ ХОЛЕЦИСТЭКТОМИЯ
Лапароскопическая холецистэктомия — это наиболее частая лапароскопическая опе рация, выполняемая в общей хирургии. Точная частота возникновения инфекционных ос ложнений после этой операции неизвестна, или значение этих осложнений недооценива ется. Источник бактериального загрязнения при развитии инфекционных осложнений может быть как эндогенным, так и экзогенным. В желчи у 56% пациентов с осложненной желчекаменной болезнью обнаруживаются различные бактерии. При неосложненной желчекаменной болезни эти цифры ниже и составляют 10-20% [30, 31, 34]. Бактерии высева ются из желчи 56% пациентов старше 65 лет, которым выполняется холецистэктомия; у 72% пациентов с холедохолитиазом в желчи, полученной из протоков, также имеются бактерии (рис. 13.6). При извлечении желчного пузыря из брюшной полости через околопупочный разрез может произойти бактериальное обсеменение раневого канала (это так называемый эндогенный источник инфекции). Клиническое значение эндогенного источ ника инфекции отражено на рис. 13.7. Уровень смертности среди пациентов, в желчи которых были обнаружены бактерии, в 3-4 раза превышает уровень смертности среди пациентов со стерильной желчью. По результатам 3 исследований, в которых было об-

230 |
Глава 13 |
Антибиотикопрофилактика и лапароскопической хирургии |
231 |
следовано 97 пациентов, развитие раневой инфекции наблюдалось у 20,6% пациентов с дополнительными факторами риска, такими как камни общего желчного Чфотока, камни внутрипеченочных протоков, возраст пациентов более 65 лет и различные осложнения желчно-каменной болезни (табл. 13.3) [16, 17, 18]. При отсутствии факторов риска частота возникновения послеоперационных инфекционных осложнений заметно ниже.
Во время лапароскопических операций возможно также инфицирование раневых ка налов, через которые вводятся троакары, из экзогенного очага. Это наиболее частый ме ханизм инфицирования ран при лапароскопической холецистэктомии. В двух недавно проведенных исследованиях из инфицированных ран пациентов, перенесших лапароско пическую холецистэктомию, были выделены грамположительные кокки, аналогичные тем, которые обнаруживаются на коже [2,36].
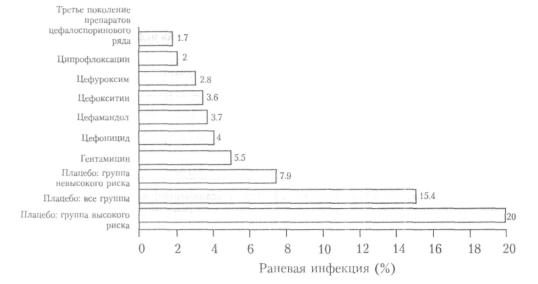
Поскольку убедительных исследований, позволяющих определить наиболее эффек тивные антибиотики, которые можно было бы применять для профилактики инфекци^ онных осложнений после лапароскопической холецистэктомии, пока еще не существует, следует использовать данные, которые были получены для «открытых» операций. Франтзайдес (Frantzides С. Т.) [36] показал, что пациентам, входящим в группу невысокого риска по развитию инфекционных осложнений, внутривенное введение антибиотиков с профилактической целью не показано; им бывает вполне достаточно хорошо обработать кожу раствором антисептика. Стандартная схема антибиотикопрофилактики при выполнении «открытых» холецистэктомии включает однократное введение 2 г цефазолина за 30-60 минут перед операцией; такой тактики придерживаются у всех пациентов, независимо от того, входят ли они в группу высокого риска по развитию послеоперационных инфекционных осложнений или нет. Во многих рандомизированных исследованиях сравнивались раз личные схемы антибиотикопрофилактики раневой инфекции после «открытых» холецист эктомии (табл. 13.5-13.11) (рис. 13.8). Результаты этих исследований применимы также и к лапароскопическим операциям, так как патогенез развития инфекции в обоих случаях практически одинаков (как упоминалось ранее).
Рис. 13.8. Обобщение результатов проспективных рандомизированных исследований, посвященных использованию в предоперационном периоде антибиотиков для профилактики развития инфекционных осложнений после операций на желчных путях. Для сравнения приведены данные по пациентам, получавшим плацебо и входившим в группы разной степей" риска
