
- •Міністерство освіти і науки україни
- •І. Обробка та оформлення результатів лабораторних робіт
- •Іі. Правила роботи в лабораторії з фізичної хімії і техніка безпеки
- •Ліквідація нещасних випадків і надання першої допомоги
- •Ііі. Агрегатний стан речовин
- •1. Визначення маси моля речовини вимірюванням її об’єму в газоподібному стані
- •2. Визначення в’язкості системи етиловий спирт – вода
- •I. Хімічна термодинаміка
- •1. Визначення теплоти згоріння речовин за допомогою калориметра юнкерса
- •Експериментальна частина
- •2. Визначення теплоти розчинення і теплоти гідратації солі
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •1. Визначення поверхневого натягу розчинів методом відліку крапель (сталагмометричним методом)
- •Поверхневий натяг води в залежності від температури
- •Густина води в залежності від температури
- •Густина розчинів NaCl при 293 к
- •2. Визначення площі та довжини молекули поверхнево-активної речовини
- •3. Адсорбція оцтової кислоти на активованому вугіллі
- •Методика експерименту
- •4. Дослідження адсорбції забарвлених речовин із розчинів
- •5. Дослідження адсорбції ізоамілового спирту із розчину за допомогою активованого вугілля
- •6. Визначення повної обмінної ємності (оє) катіоніту
- •7. Визначення вмісту лікарської речовини (глюконату кальцію) в розчині методом йонообмінної адсорбції
- •8. Обезсолювання води за допомогою йонітів
- •VI. Розчини неелектролітів
- •1. Визначення критичної температури взаємного розчинення рідин
- •2. Визначення молекулярної маси розчиненої речовини кріоскопічним методом
- •VII. Розчини електролітів
- •1. Визначення електропровідності електролітів і обчислення ступеня дисоціації
- •Експериментальна частина
- •Робота на змінному струмові
- •2. Bизначення розчинності малорозчинних сполук
- •3. Визначення іонного добутку води
- •4.Визначення концентрації кислоти методом кондуктометричного титрування
- •5. Визначення вмісту лікарської речовини в розчині
- •Хід роботи
- •Обробка результатів експерименту
- •VIII. Гальванічні елементи та електродні потенціали
- •1. Вимірювання електрорушійних сил гальванічних елементів
- •2. Визначення водневого показникa потенціометричним методом
- •3. Потенціометричне визначення рН, розрахунок константи дисоціації слабкої кислоти
- •Іх. Хімічна кінетика і каталіз
- •1. Визначення швидкості розкладу тіосульфатної кислоти
- •Дослід 1. Залежність швидкості розкладу тіосульфатної кислоти від її молярної концентрації
- •Дослід 2. Залежність швидкості розкладу тіосульфатної кислоти від температури
- •Виконання роботи
- •Склад реакційної суміші
- •Результати титрування
- •3. Дослідження гідролізу крохмалю в присутності соляної кислоти
- •4. Дослідження гідролізу крохмалю в присутності ферментів і соляної кислоти при температурі 310 к
- •5. Визначення швидкості розкладу пероксиду водню газометричним методом
- •6. Фотохімічний розклад н2о2
- •Послідовність виконання роботи
- •Х. Фізикохім ія дисперсних систем.
- •1. Методи одержання колоїдних розчинів
- •2. Коагуляція колоїдних розчинів електролітами
- •3. Визначення величини електрокінетичного потенціалу методом електрофорезу
- •4. Вивчення ізоелектричної точки білків
- •5. Набухання гелів
- •Хід виконання роботи
- •Хі. Біогенні елементи
- •1. Аналітичні реакції на йони s-елементів
- •Визначення хлор-йонів Cl– в питних водах за методом Фольгарда
- •2. Аналітичні реакції на р-елементи та їх сполуки
- •Реакція на бор (ііі) по кольору полум’я
- •Реакція на йон з розведеними кислотами
- •Реакція на йон з реактивом Несслера
- •Реакція на йон із розчином хлориду барію
- •(Реакція л.А. Чугаєва)
- •Контрольні питання до колоквіумів іii. Агрегатний стан речовин
- •Іv. Хімічна термодинаміка та біоенергетика
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •Vі. Розчини неелектролітів
- •Vіі. Розчини електролітів
- •Vііі. Гальванічні елементи та електродні потенціали
- •IX. Хімічна кінетика і каталіз
- •Х. Фізикохімія дисперсних систем
- •Хі. Біогенні елементи
- •Додатки
- •Деякі фізичні константи
- •Густина деяких речовин
- •Густина деяких газів (н.У.)
- •Співвідношення між позасистемними одиницями
- •Пояснювальна записка
- •Зміст дисципліни
- •Тема 1. Предмет фізичної хімії та її значення. Розділи фізичної хімії. Методи дослідження. Розвиток фізичної хімії в Україні.
- •Тема 7.
- •Тема 8.
- •Тема 9.
- •Тема 10.
- •Тема 11.
- •Тема 12.
- •Тема 13.
- •Тема 14.
- •Орієнтовний перелік питань до підсумкового контролю знань з дисципліни.
- •Cписок літератури
- •І. Обробка та оформлення результатів
- •Гомонай Василь Іванович
Ііі. Агрегатний стан речовин
1. Визначення маси моля речовини вимірюванням її об’єму в газоподібному стані
Для роботи необхідно: прилад для випаровування речовини і замірю- вання об’єму пари даної речовини; аналітичні терези; плитка електрична; ампули, що заповнюються досліджуваною речовиною; термометр кімнат- ний; барометр – анероїд.
Метод визначення густини пари і молекулярного об’єму речовини в па-роподібному стані при нормальних умовах, тобто при 273 К і 1,013105 Па, ґрунтується на застосуванні газових законів для твердих і рідких речовин, переведених у газоподібний стан.
Для знаходження густини пари по вищезгаданому методу визначають об’єм відомої маси речовини, переведеної в газоподібний стан.
Знаючи масу пари, яка при температурі Т і тиску Р займає об’єм V, можна вирахувати густину do. Для цього виміряний об’єм приводять до нормальних умов, користуючись рівнянням Клапейрона:
|
|
|
|
звідки
![]() .
.
При нормальних умовах одержують густину пари:
![]() ,
,
де g – наважка речовини, кг.
Т,V,Р – температура, об’єм і тиск пари речовини в умовах досліду.
Користуючись рівнянням Менделєєва – Клапейрона, можна вираху- вати молекулярну вагу речовини
![]() .
.
По молекулярній вазі речовини і густині його пари при нормальних умовах обчислюють молекулярний об’єм речовини в пароподібному стані за формулою
![]() .
.
Точність розглянутого методу не перевищує 1, так як при розрахунках користуються газовими законами, справедливими лише для ідеальних газів.
Досліджувані пари значно відхиляються від цих законів при темпе- ратурах, близьких до точок кипіння досліджуваних речовин.
Суть методу полягає в наступному.
Точно відважену кількість речовини (не більше 0,1–0,2 г) випаро- вують в особливому приладі при температурі, що не менше ніж на 293 К перевищує її температуру кипіння. Пари досліджуваної речовини витіс- няють з приладу в газовимірювальну бюретку об’єм повітря V, рівний об’є-му парів досліджуваної речовини. Даний об’єм знаходиться під тиском Р і кімнатній температурі Т.
Таким чином, експериментально визначають не об’єм пари дослід- жуваної речовини, а рівний йому об’єм повітря, витісненого цими парами з приладу, причому вимірювання об’єму проводять при кімнатній темпера- турі і під атмосферним тиском.
Прилад для визначення молекулярної маси схематично зображений на ри-сунку 1. Він уявляє собою циліндричний посуд 1, до якого припаяна трубка 2. До верх-ньої частини приладу припаяний відросток, кінець трубки під час досліду закривається гумовим корком 6. Посуд занурюється в металічну баню 3, заповнену водою в такій кількості, щоб його розширена частина була у воді. Воду нагрівають до кипіння для обігріву розширеної частини посуду.
Я
Рис. 1.Прилад
для визначення молекулярної маси
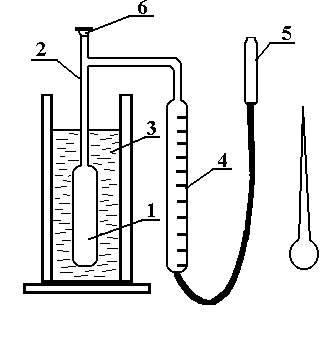
Перед початком роботи вклю- чають електроплитку для нагрівання водяної бані.
Робота починається з очистки посу- ду від речовини, яка досліджувалась раніше, і продуванням його повітрям.
У чергового лаборанта одержують три ампули, які зважують з точністю до 0,0001 г і повертають для заповнення їх досліджуваною речовиною. Заповнені ампули знову зважують з поперед- ньою точністю. Різниця у масі заповненої і порожньої ампули дає масу взятої для досліду речовини.
Після інтенсивного кипіння води протягом деякого часу ампули мож- на опустити в прилад, попередньо встановивши за допомогою зрівню- вальної склянки 5 рівень води в газовимірювальній бюретці на нулеві.
Відломивши частину капіляру, ампулу головкою вниз кидають через верхній отвір приладу разом з відламаною частиною. При цьому швидко і старанно закривають отвір гумовим корком.
Речовина, що містилася в ампулі, випаровується. Пара витісняє з посуду 1 в газовимірювальну бюретку 4 об’єм повітря, рівний об’єму утвореної пари досліджуваної речовини. В результаті цього рівень води в бюретці понижується. Коли об’єм повітря в бюретці перестає змінюватися, що вказує на кінець випаровування, встановлюють рівні в бюретці і в зрівнюваній склянці точно по одній висоті. Відраховують об’єм витісне- ного повітря, який відповідає об’єму речовини, переведеної в пару.
Відмічають температуру по кімнатному термометру і атмосферний тиск по барометру, що знаходиться в даній лабораторії.
Закінчивши один дослід, приступають до другого, третього. З одержа- них даних знаходять середнє значення. Перед кожним дослідом проду- вають прилад повітрям і очищають від уламків ампул, не припиняючи нагрівання водяної бані. Як вказано вище, густина пари при нормальних умовах дорівнює
![]() .
.
Повітря, яке знаходиться в бюретці над водою, насичується парами води. Вимірюваний атмосферний тиск Н урівноважується сумою парціаль- ного тиску Р повітря, витісненого в бюретку, та пружності парів води, які насичують простір при температурі досліду:
![]() .
.
Повітря, що міститься в приладі, це кімнатне повітря, відносна вологість якого в лабораторних умовах коливається в межах 50%. Для свого насичення воно потребує тільки половину максимальної кількості води і, отже, створений ним парціальний тиск буде дорівнювати h/2.
Таким чином, витіснене в бюретку напіввологе повітря, займаючи весь об’єм V при кімнатній температурі Т, має тиск
![]() .
.
де h береться з таблиці, що подається в кінці опису.
Підставляючи значення тиску у вираз для густини пари, одержуємо:
 .
.
З рівняння
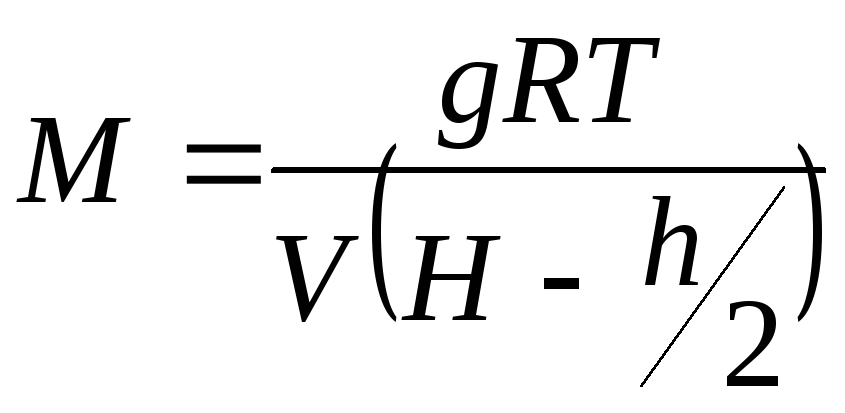 ,
де
,
де
![]()
розраховують молекулярну масу речовини. Знаючи do і молекулярну масу речовини, визначають молекулярний об’єм досліджуваної речовини в газоподібному стані
![]() .
.
Коефіцієнти при змінних величинах g і V
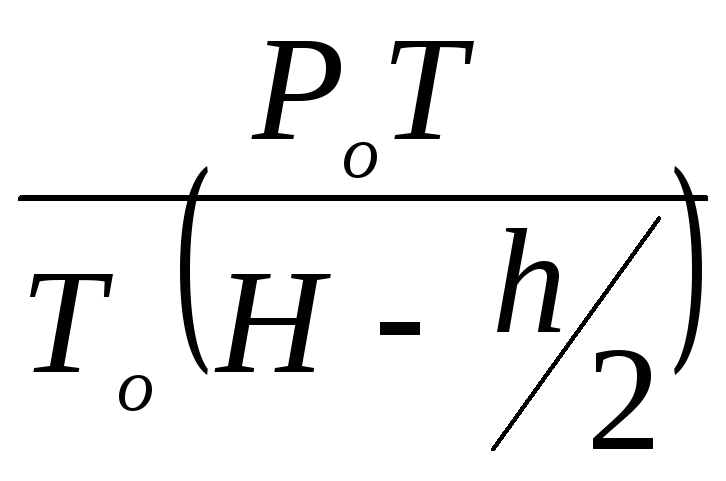 і
і
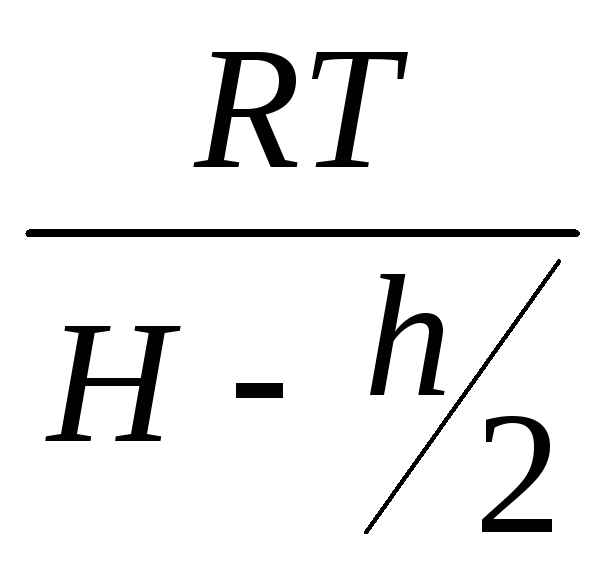
будуть однакові для всіх трьох вимірів і тому рекомендується, знаючи умови досліду, попередньо підрахувати значення цих коефіцієнтів і корис- туватися ними при розрахунках густини і молекулярної маси.
Дослідні і розрахункові дані заносяться в табл. 1.
Таблиця 1
|
№ п/п |
Вага порожньої ампули,10-3кг |
Вага ампули з рідиною, 10-3кг |
Наважка рідини, 10-3кг |
Об’єм, 10-6м3 |
Темпера-тура,К |
Тиск по барометру, 1,0133·105Па |
Пружність парів води |
Тиск, 1,0133·105Па |
Густина, кг/м3 |
Мол. маса, кг/кмоль |
Мол. об’єм, 10-6м3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Пружність парів води в залежності від температури наведено в табл. 2.
Таблиця 2
|
Т, К |
h |
Т, К |
h |
|
287,0 |
11,987 |
292,5 |
16,99 |
|
287,5 |
12,382 |
293,0 |
17,535 |
|
288,0 |
12,783 |
293,5 |
18,085 |
|
288,5 |
13,205 |
294,0 |
18,650 |
|
289,0 |
13,634 |
294,5 |
19,231 |
|
289,5 |
14,076 |
295,0 |
19,827 |
|
290,0 |
14,530 |
295,5 |
20,440 |
|
290,5 |
14,997 |
296,0 |
21,068 |
|
291,0 |
15,477 |
296,5 |
21,714 |
|
291,5 |
15,971 |
297,0 |
22,377 |
|
292,0 |
16,477 |
298,0 |
23,765 |
