
- •Міністерство освіти і науки україни
- •І. Обробка та оформлення результатів лабораторних робіт
- •Іі. Правила роботи в лабораторії з фізичної хімії і техніка безпеки
- •Ліквідація нещасних випадків і надання першої допомоги
- •Ііі. Агрегатний стан речовин
- •1. Визначення маси моля речовини вимірюванням її об’єму в газоподібному стані
- •2. Визначення в’язкості системи етиловий спирт – вода
- •I. Хімічна термодинаміка
- •1. Визначення теплоти згоріння речовин за допомогою калориметра юнкерса
- •Експериментальна частина
- •2. Визначення теплоти розчинення і теплоти гідратації солі
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •1. Визначення поверхневого натягу розчинів методом відліку крапель (сталагмометричним методом)
- •Поверхневий натяг води в залежності від температури
- •Густина води в залежності від температури
- •Густина розчинів NaCl при 293 к
- •2. Визначення площі та довжини молекули поверхнево-активної речовини
- •3. Адсорбція оцтової кислоти на активованому вугіллі
- •Методика експерименту
- •4. Дослідження адсорбції забарвлених речовин із розчинів
- •5. Дослідження адсорбції ізоамілового спирту із розчину за допомогою активованого вугілля
- •6. Визначення повної обмінної ємності (оє) катіоніту
- •7. Визначення вмісту лікарської речовини (глюконату кальцію) в розчині методом йонообмінної адсорбції
- •8. Обезсолювання води за допомогою йонітів
- •VI. Розчини неелектролітів
- •1. Визначення критичної температури взаємного розчинення рідин
- •2. Визначення молекулярної маси розчиненої речовини кріоскопічним методом
- •VII. Розчини електролітів
- •1. Визначення електропровідності електролітів і обчислення ступеня дисоціації
- •Експериментальна частина
- •Робота на змінному струмові
- •2. Bизначення розчинності малорозчинних сполук
- •3. Визначення іонного добутку води
- •4.Визначення концентрації кислоти методом кондуктометричного титрування
- •5. Визначення вмісту лікарської речовини в розчині
- •Хід роботи
- •Обробка результатів експерименту
- •VIII. Гальванічні елементи та електродні потенціали
- •1. Вимірювання електрорушійних сил гальванічних елементів
- •2. Визначення водневого показникa потенціометричним методом
- •3. Потенціометричне визначення рН, розрахунок константи дисоціації слабкої кислоти
- •Іх. Хімічна кінетика і каталіз
- •1. Визначення швидкості розкладу тіосульфатної кислоти
- •Дослід 1. Залежність швидкості розкладу тіосульфатної кислоти від її молярної концентрації
- •Дослід 2. Залежність швидкості розкладу тіосульфатної кислоти від температури
- •Виконання роботи
- •Склад реакційної суміші
- •Результати титрування
- •3. Дослідження гідролізу крохмалю в присутності соляної кислоти
- •4. Дослідження гідролізу крохмалю в присутності ферментів і соляної кислоти при температурі 310 к
- •5. Визначення швидкості розкладу пероксиду водню газометричним методом
- •6. Фотохімічний розклад н2о2
- •Послідовність виконання роботи
- •Х. Фізикохім ія дисперсних систем.
- •1. Методи одержання колоїдних розчинів
- •2. Коагуляція колоїдних розчинів електролітами
- •3. Визначення величини електрокінетичного потенціалу методом електрофорезу
- •4. Вивчення ізоелектричної точки білків
- •5. Набухання гелів
- •Хід виконання роботи
- •Хі. Біогенні елементи
- •1. Аналітичні реакції на йони s-елементів
- •Визначення хлор-йонів Cl– в питних водах за методом Фольгарда
- •2. Аналітичні реакції на р-елементи та їх сполуки
- •Реакція на бор (ііі) по кольору полум’я
- •Реакція на йон з розведеними кислотами
- •Реакція на йон з реактивом Несслера
- •Реакція на йон із розчином хлориду барію
- •(Реакція л.А. Чугаєва)
- •Контрольні питання до колоквіумів іii. Агрегатний стан речовин
- •Іv. Хімічна термодинаміка та біоенергетика
- •V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
- •Vі. Розчини неелектролітів
- •Vіі. Розчини електролітів
- •Vііі. Гальванічні елементи та електродні потенціали
- •IX. Хімічна кінетика і каталіз
- •Х. Фізикохімія дисперсних систем
- •Хі. Біогенні елементи
- •Додатки
- •Деякі фізичні константи
- •Густина деяких речовин
- •Густина деяких газів (н.У.)
- •Співвідношення між позасистемними одиницями
- •Пояснювальна записка
- •Зміст дисципліни
- •Тема 1. Предмет фізичної хімії та її значення. Розділи фізичної хімії. Методи дослідження. Розвиток фізичної хімії в Україні.
- •Тема 7.
- •Тема 8.
- •Тема 9.
- •Тема 10.
- •Тема 11.
- •Тема 12.
- •Тема 13.
- •Тема 14.
- •Орієнтовний перелік питань до підсумкового контролю знань з дисципліни.
- •Cписок літератури
- •І. Обробка та оформлення результатів
- •Гомонай Василь Іванович
(Реакція л.А. Чугаєва)
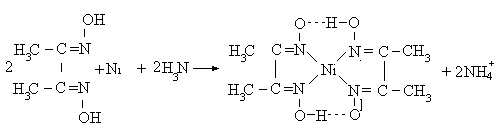
У пробірку налити краплю розчину солі нітрату нікелю (ІІ), додати 3–6 крапель водного розчину аміаку та 2–3 краплі спиртового розчину диметилгліоксимату. Спостерігають випадання яскраво-червоного осаду диметилгліоксимату нікелю (внутрішньокомплексна сполука). Реакція ду- же чутлива! Використовується для виявлення йонів Ni2+ у стічних водах.
Аналітичні реакції на йон Со2+ з нітратом калію
2–3 краплі розчину нітрату кобальту (ІІ) налити у пробірку, додати декілька крапель розчину СН3СООН до рН=3 (проба універсальним індикатором) та 1–2 краплі розчину нітрату калію. Випадає жовтий кристалічний осад K3[Co(NO2)6].
Co(NO3)2 + 7KNO2 + 2СН3СООН = K3[Co(NO2)6]↓ + NO +
+ 2KNO3 + 2СН3СООK + H2O
Co+2
+
![]() + 3K+
+ 2СН3СООН
=
K3[Co(NO2)6]↓
+ NO + 2СН3СОО-
+ H2O
+ 3K+
+ 2СН3СООН
=
K3[Co(NO2)6]↓
+ NO + 2СН3СОО-
+ H2O
Реакція на йон Hg2+ із SnCl2
У пробірку до 0,5 мл розчину хлориду меркурію (ІІ) (сулеми) додати по краплям розчин SnCl2. Утворюється білий осад каломелю (Hg2Cl2), який поступово чорніє.
а) 2HgCl2 + SnCl2 = Hg2Cl2↓ + SnCl4
2HgCl2 + Sn2+ = Hg2Cl2↓+ Sn4+ + 2Cl–
б) Hg2Cl2 + SnCl2 = 2Hg + SnCl4
Hg2Cl2 + Sn2+ = 2Hg + Sn4+ + 2Cl–
Контрольні питання до колоквіумів іii. Агрегатний стан речовин
Робота: III. 1.
Визначення маси моля речовини вимірюванням її об’єму в газо-подібному стані.
Робота: III. 2.
Визначення в’язкості системи етиловий спирт – вода.
Ідеальний газ, умови його існування. Основні газові закони і умови їх застосування. Рівняння стану ідеального газу. Практичне застосування рівняння Менделєєва–Клапейрона. Реальні гази та умови їх існування. Рівняння стану реальних газів. Методика роботи і оформлення дослідних даних.
Загальна характеристика рідкого стану. В’язкість і текучість рідини. Одиниці вимірювання в’язкості. Основні рівняння гідродинаміки потоку Ньютона і Пуазейля, умови їх застосування. Причини відхилення від ламі-нарного потоку. Методи визначення в’язкості і фактори, що впливають на в’язкість. В’язкість розчинів високомолекулярних речовин. Методика робо- ти і оформлення дослідних даних.
Іv. Хімічна термодинаміка та біоенергетика
Робота: IV. 1.
Визначення теплоти горіння газів за допомогою калориметра Юнкерса.
Робота: IV. 2.
Визначення теплоти розчинення і теплоти гідратації солі.
Основні поняття і термінологія. Перший закон термодинаміки, його математичний вираз. Застосування першого закону термодинаміки до біологічних систем. Термохімія. Закон Гесса і висновки з нього. Стандарт- ні теплоти (ентальпії) утворення, нейтралізації, згорання, розчинення. Термохімічні розрахунки. Методика виконання роботи та оформлення результатів.
V. Поверхневі явища (поверхнева енергія, поверхневий натяг та адсорбція на межі розділу фаз)
Робота: V. 1.
Визначення поверхневого натягу розчинів методом відліку кра- пель (сталагмометричним методом)
Робота: V. 2.
Визначення площі та довжини молекули поверхнево-активної речовини
Робота: V. 3.
Адсорбція оцтової кислоти на активованому вугіллі
Робота: V. 4.
Дослідження адсорбції забарвлених речовин із розчинів
Робота: V. 5.
Дослідження адсорбції ізоамілового спирту із розчину за допомогою активованого вугілля
Робота: V. 6.
Визначення повної обмінної ємності (оє) катіоніту
Робота: V. 7.
Визначення вмісту лікарської речовини (глюконату кальцію) в розчині методом йонообмінної адсорбції
Робота: V. 8.
Обезсолювання води за допомогою йонітів
Робота: V. 9.
Розділення йонів Fe3+, Cu2+, Co2+ методом хроматографії на оксиді алюмінію
Поверхневий натяг як питома поверхнева енергія на межі розділу двох фаз. Одиниці вимірювання поверхневого натягу. Фактори, що впливають на поверхневий натяг чистої рідини. Поверхнево-активні і поверхнево-неактивні речовини. Особливості будови їх молекул, приклади. Вплив по- верхнево-активних речовин на величину поверхневого натягу води. Ізо- терма поверхневого натягу. Зв’язок поверхневого натягу і адсорбції на межі розділу рідина – газ. Рівняння Гіббса. Позитивна і негативна адсорбція. Методи визначення поверхневого натягу. Фізико-хімічна суть йонооб- мінної адсорбції. Вибіркова адсорбція. Правило Пескова – Панета – Фаянса. Йоніти. Обмінна ємність йонітів. Використання йонітів у медицині. Поняття про хроматографію. Методика визначення поверхневого натягу методом відліку крапель. Оформлення дослідних даних.
