
- •Фізико-хімічні методи аналізу
- •Оптичні методи аналізу
- •Атомно-емісійна спектроскопія
- •Загальна схема спектральних приладів
- •Фотометрія полум’я
- •Люмінесцентний аналіз
- •Походження люмінесценції
- •Характеристики і закономірності люмінесценції
- •Якісний і кількісний аналіз
- •Можливості і практичне застосування
- •Абсорбційні методи аналізу
- •Електрохімічні методи аналізу
- •Кількісний аналіз проводять :
- •Практичне використання
- •Вольтамперометрія (полярографія)
- •Кулонометрія
- •Сорбційні (хроматографічні) методи аналізу
- •Рідинна хроматографія
- •Іонообмінна хроматографія
- •Гель-проникаюча хроматографія (молекулярне сито)
- •Газова хроматографія
- •Список літератури
Кількісний аналіз проводять :
прямими методами,
- скориставшись
наведеним вище рівнянням для розрахунку
концентрації електроліту. При невідомому
ступені дисоціації, можна скористатися
зако--ном Оствальда
![]() ,
деКдис – константа
дисоціації електроліту;
,
деКдис – константа
дисоціації електроліту;
- використовуючи градуювальний графік, побудований в координатах
R - c(B) або G - c(B).
Кондуктометрія не є селективним методом оскільки всі кондуктометричні параметри – величини адитивні (сумарні). Тому прямими методами можна аналізувати тільки однокомпонентні об’єкти або визначати загальну кількість електролітів в розчині.
2) кондуктометричним титруванням. Титрування проводять , додаючи розчин реагенту порціями певного об’єму, і фіксують величини R (або G) після кожної порції. По отриманим даним будують криву титрування в координатах: R (або G) -- V(реагенту). В точці еквівалентності спостерігається злам кривої титрування (рис. 15). Форма кривої титрування залежить від рухомості іонів, які приймають участь в реакції. В кондуктометричному титруванні найчастіше використовують реакції: кислотно-основні; осадження, комплексоутворення і рідше окислення-відновлення. Реакції повинні відповідати наступним вимогам: велика константа рівноваги; практично миттєве встановлення хімічної рівноваги; велика швидкість реакції; відсутність побічних процесів; значна різниця в величинах рухомостей іонів, які приймають участь в реакції. При задоволені цих вимог використовують прямий спосіб титрування. В інших випадках можливо проводити аналіз способама титрування по залишку (зворотнє титрування) і по заміщенню.




 G
G
G
G

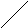 а)
б)
а)
б)
т.е т.е т.е.



![]()
V(реагенту) V(реагенту)
Рис. 15. Криві титрування однокомпонентної (а) та
двокомпонентної систем (б); т.е. точка еквівалентності.
Електричну провідність розчинів визначають за допомогою кондуктометрів різноманітних конструкцій, вимірюючи електричний опір шару рідини, який знаходиться між двома паралельними електродами площею 1 см2кожний при відстані між ними 1 см, які занурені в розчин, що аналізують.
В прямій кондуктометрії звичайно використовують ячейки з жорстко закріпленими електродами. В методах кондуктометричного титрування часто використовують так звані занурювальні електроди , які дозволяють проводити титрування в любих ємкостях, в яких можна розмістити електроди. Величина опору розчину, яка вимірюється експериментально, залежить не тільки від розміру електродів і відстані між ними, але і від їх форми і взаємного розташу-вання, об’єму розчину та інших факторів. Істинна електрична провідність розчину γіст пропорційна величині γексп , яка експериментально вимірена: γіст = k · γексп, де k - константа ячейки .
Константа ячейки дуже важлива характеристика і її знаходять експериментально по электричній провідності стандартних водних розчинів хлориду калию.
Низькочастотна кондуктометрія непридатна для аналізу агресивних середовищ (небезпека корозії електродів), емульсій, суспензій (небезпека забруднення електродів).
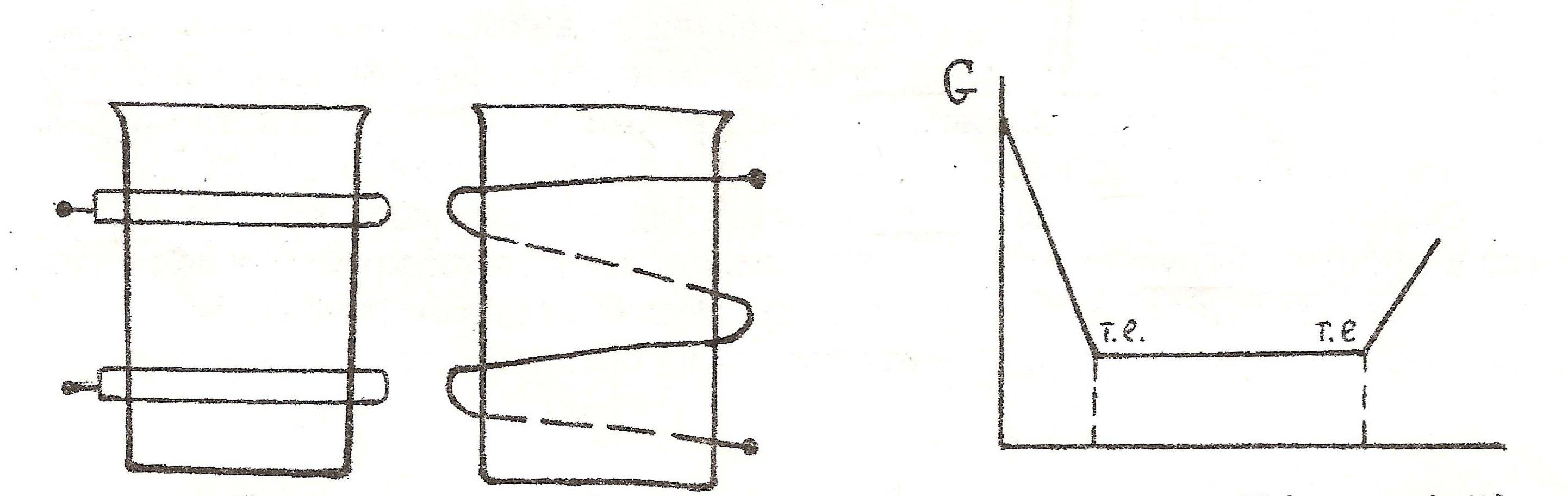
Високочастотна кондуктометрія заснована на використанні змінних струмів високої частоти (десятки мегагерц). Конструкція ячейок виключаєбезпосередній контакт електродів з розчином і це є одним з суттєвих переваг методу.. Ячейку з розчином, що аналізують, при високочастотному титруванні поміщають або між пластинкамиконденсатора (конденсаторна абоємкістна, або С – ячейка), або всередині індукційної катушки (індуктина абоLячейка) (рис.16).
В електричному полі високої частоти відсутній поступальний рух іонів в напрямку поля через їх велику інерційність. В такому полі іони деформуються (деформаційна поляризація) і обертаються навколо своєї осі (орієнтаційна поляризація). Електрична провідність розчинів обумовлена наявністю в розчині струму провідності і струму зміщення. Електричні параметри розчинів залежать від багатьох факторів і ці залежності неможливо однозначно описати математичним рівнянням. Тому високочастотну
а б V (реагенту)
Рис.16. Ячейки для високочастотного Рис.17. Крива кондуктометричного
титрування: а – ємкістна титрування суміші сильної
(С- ячейка); б – індуктивна і слабкої кислот сильною
(L - ячейка) основою
кондуктометрію використовують тільки в титриметричному варіанті (високочастотне титрування, ВЧТ). Криві ВЧТ аналогічні кривим титрування в низькочастотній кондуктометрії, їх будують в координатах I - V(реагенту), де I - сила електричного струму в ланцюзі титратора(рис. 17). Промисловість випускає стандартні високочастотні титратори.
Основним достоїнством ВЧТ є можливість аналізу любих агресивних середовищ, оскільки електроди не мають контакту з розчином, що аналізується.
