
- •Фізико-хімічні методи аналізу
- •Оптичні методи аналізу
- •Атомно-емісійна спектроскопія
- •Загальна схема спектральних приладів
- •Фотометрія полум’я
- •Люмінесцентний аналіз
- •Походження люмінесценції
- •Характеристики і закономірності люмінесценції
- •Якісний і кількісний аналіз
- •Можливості і практичне застосування
- •Абсорбційні методи аналізу
- •Електрохімічні методи аналізу
- •Кількісний аналіз проводять :
- •Практичне використання
- •Вольтамперометрія (полярографія)
- •Кулонометрія
- •Сорбційні (хроматографічні) методи аналізу
- •Рідинна хроматографія
- •Іонообмінна хроматографія
- •Гель-проникаюча хроматографія (молекулярне сито)
- •Газова хроматографія
- •Список літератури
Люмінесцентний аналіз
Люмінесцентним аналізом називається сукупність методів аналізу, заснованих на спостереженні явища люмінесценції. За визначенням, даним В. Л. Левшиним, люмінесценція – це світіння атомів, молекул, іонів і інших більш складних комплексів, яке виникає в результаті електронного переходу в цих частках при їхньому поверненні зі збудженого стану в нормальний.
Звідси випливає, що для збудження люмінесценції необхідно підводити енергію ззовні, оскільки вона втрачається при випромінюванні, тому види люмінесценції можна класифікувати за зовнішнім джерелом збудження енергії (табл. 2). Найчастіше в аналітичній хімії використовують фотолюмінесценцію і хемілюмінесценцію.
Висока чутливість визначення, великий діапазон обумовлених вмістів
(іноді до 4 порядків величин концентрацій) при високій відтворюваності результатів аналізу і визначили розвиток люмінесцентного методу аналізу.
Люмінесценцію часто спостерігають у повсякденному житті. Здатністю до люмінесценції володіють деякі види глибоководних риб, мікроорганізмів. На сонячному світлі люмінесціюють деякі тонізуючі напої (через добавки хініну); бензин, що містить поліциклічні ароматичні вуглеводні (нафталін, антрацен і ін.); деякі ліки та наркотики. Світяться деякі мінерали і руди (наприклад, уранові). Щодня ми бачимо екрани телевізорів, що світяться.
Таблиця 2 - Класифікація методів люмінесценції за способами збудження
|
Джерело збудження |
Вид люмінесценції |
|
Електромагнітне випромінювання УФ- і видимого спектрального діапазону |
Фотолюмінесценція |
|
Потік електронів (катодні промені) |
Катодолюмінесценція |
|
Потік іонів лужних металів у вакуумі |
Іонолюмінесценція |
|
Рентгенівське випромінювання |
Рентгенолюмінесценція |
|
Радіоактивне випромінювання |
Радіолюмінесценція |
|
Теплова енергія |
Термолюмінесценція, або кандолюмінесценція |
|
Ультразвук |
Сонолюмінесценція |
|
Механічний вплив |
Триболюмінесценція |
|
Енергія хімічних реакцій |
Хемілюмінесценція |
Походження люмінесценції
Молекула, поглинаючи квант світла, переходить з основного (незбудже-ного) стану S0 у збуджений електронний стан, наприклад S1 (рис. 3). При кім-натній температурі молекули перебувають в основному коливальному стані. Переходячи в збуджений стан, молекула потрапляє на один з його коливальних рівнів. Поглинання молекулою кванта світла здійснюється за дуже короткий час (10-15 с). Потім за 10-12 с відбувається перехід електрона на нижній коли-вальний підрівень збудженого стану (див. рис. 3а – коротка хвиляста стрілка). Цей процес називають коливальною релаксацією. Повернення молекули з нижнього коливального стану S1 у незбуджений стан S0 може відбутися трьома шляхами:
1) втрата молекулою енергії у виді теплоти в результаті зіткнень з іншими част-ками (процес внутрішньої конверсії, зображений на рис. 3а, довга хвиляста стрілка);
2) повернення молекули на будь-який коливальний підрівень основного стану з випущенням енергії у виді кванта світла без зміни спину електрона (флуоресценція);
3) перехід молекули зі збудженого стану S1 у метастабільний Т1, а потім в основний S0 або в результаті внутрішньої конверсії з виділенням теплоти (рис. 3б – довга хвиляста стрілка), або з виділенням кванта світла (фосфоресценція).
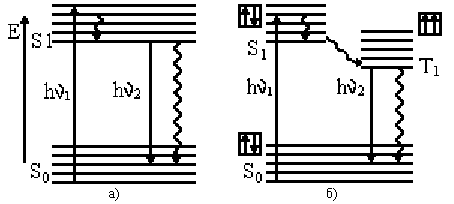
Рис. 3- Схема енергетичних переходів молекули, що ілюструє виникнення
флуоресценції (а) і фосфоресценції (б) (схема Яблонського)
