
- •Глава 1. Основні поняття та закони хімії
- •1.1. Основні поняття хімії
- •1.2. Фундаментальні та стехіометричні закони хімії
- •1.2.1. Закон збереження маси речовини
- •1.2.2. Закон сталості складу речовин
- •1.2.3. Закон кратних відношень
- •1.2.4. Закон еквівалентів.
- •1.3. Закони газового стану
- •1.3.1. Закон об’ємних відношень гей-люсака
- •1.3.2. Закон авогадро
- •1.3.3. Закон бойля – маріотта
- •Контрольні завдання
- •Б) Із закону Авогадро випливає, що об’єм 0,025 моль h2s за нормальних умов
- •В) Відомо, що 1 моль будь-якої речовини містить 6,02 · 1023 молекул. Молярний об’єм газу за нормальних умов складає 22,4 л. Тому справедливо
- •Приклад 3. Який об’єм за нормальних умов займуть 4 10-4 м3 газу, що знаходиться при 50оС й тиску 9,54 104 Па?
- •Приклад 4. При згорянні 5 г металу утворилося 9,44 г оксиду металу. Визначити еквівалентну масу металу.
- •Приклад 5. Деяка кількість металу, еквівалентна маса якого дорівнює 28 г/моль, витісняє з кислоти 1,4 л водню, виміряного за нормальних умов. Визначити масу металу.
- •Розв’язання. Відповідно до закону еквівалентів (1.1), маси взаємодіючих речовин пропорційні їхнім еквівалентним масам:
- •Зі співвідношення (1.8) знаходимо еквівалентну масу h3ро4:
- •Приклад 8. Обчислити точну атомну масу металу, якщо питома теплоємність металу дорівнює 0,23 кДж/(кг к), а хлорид цього металу містить 61,2% металу.
- •Приклад 10. Визначити формулу речовини, якщо відомо, що її густина за воднем дорівнює 29, а масові частки елементів наступні: с – 82,76%, н – 17,24%.
- •Глава 2. Класи неорганічних сполук
- •2.1. Оксиди.
- •2.1.1. Способи одержання оксидів
- •2.1.2. Класифікація та хімічні властивості оксидів
- •2.2. Гідроксиди металів
- •2.2.1. Способи одержання гідроксидів
- •2.2.2. Хімічні властивості гідроксидів металів
- •2.3. Кислоти
- •2.3.1. Способи одержання кислот
- •2.3.2. Хімічні властивості кислот
- •2.4.1.Основні способи одержання солей
- •Контрольні завдання
- •Приклади виконання завдань і розв’язання задач
- •3.2. Корпускулярно-хвильова природа електрона
- •3.3. Принцип невизначеності
- •3.4. Періодичний закон
- •3.5. Періодична система елементів
- •3.6. Електронні хмари
- •3.7. Квантові числа
- •3.8. Принцип паулі
- •3.9. Послідовність заповнення електронами енерґетичних рівнів у багатоелектронних атомах
- •Контрольні завдання
- •Приклади виконання завдань і розв’язання задач
- •Приклад 8. Які найвищий та найнижчий ступені окислення у фосфору, сульфуру та хлору? Скласти формули сполук даних елементів, що відповідають цим ступеням окислення.
- •Приклад 12. Як залежать кислотно-основні властивості оксидів і гідроксидів від ступеня окиснення атомів елементів, що їх утворюють?
- •Приклад 13. Відомо, що кремній є неметалом з напівпровідниковими властивостями. Які властивості будуть виявляти алюміній і фосфор?
- •Приклад 15. Як змінюються властивості вищих оксидів елементів третього періоду?
- •4.1.1. Характерні властивості ковалентного зв’язку
- •4.1.1.1. Насиченість ковалентного зв’язку
- •Мал. 4.3. Різновиди σ-зв’язків.
- •Мал. 4.3. Різновиди π-зв’язків.
- •4.1.1.3. Полярність і поляризованість ковалентного зв’язку.
- •4.3. Водневий зв’язок
- •4.5. Міжчастинкові взаємодії
- •Контрольні завдання
- •Приклади виконання завдань і розв’язання задач Приклад 1. Довжина диполя молекули дорівнює 2,2 10-11 м. Обчисліть дипольний момент молекули.
- •Приклад 2. Обчислити довжину зв’язку в молекулі hBr, якщо між’я-дерні відстані у молекулах h2 та Br2 відповідно дорівнюють 7,4 · 10-11 м та 2,28 10-10 м.
- •Приклад 3. Яка гібридизація електронних хмар має місце в атомі карбону при утворенні молекули cf4? Якою є просторова конфігурація цієї молекули?
- •Приклад 4. Якими є валентні можливості атома фосфору в основному та збудженому станах?
- •Приклад 5. Визначте, що є донором електронної пари при утворенні йона bh4-.
- •Глава 5. Основи хімічної термодинаміки
- •5.2. Перший закон термодинаміки
- •5.3. Закони термохімії
- •5.4. Поняття про ентропію
- •5.5. Другий закон термодинаміки
- •5.6.Третій закон термодинаміки
- •5.7. Вільна енергія Ґіббса
- •Приклад 1. Складіть термохімічне рівняння реакції горіння 1 моль ацетилену, якщо при цьому виділяється 1255,61 кДж теплоти.
- •Приклад 3. Не здійснюючи обчислень, поясніть, як змінюється ентропія системи (s): а) при переході води в пару; б) у реакції:
- •Приклад 4. Обчисліть зміну енерґії Ґіббса у хімічній реакції
- •І зробіть висновки про можливість мимовільного перебігу даної реакції за стандартних умов.
- •Стандартні зміни енерґій Ґіббса простих речовин прийнято вважати рівними нулю. Для даної системи:
- •6.1. Поняття про швидкість хімічної реакції
- •6.2. Основний закон хімічної кінетики – закон діючих мас.
- •Межі застосування закону діючих мас.
- •6.3. Молекулярність реакції.
- •6.4. Порядок реакції.
- •6.5. Особливості кінетики гетероґенних реакцій.
- •6.6. Механізм хімічних реакцій.
- •6.7. Вплив температури на швидкість реакції. Правило Вант-Гоффа.
- •6.8. Рівняння Арреніуса. Енерґія активації
- •Вихідні Активов. Продукти
- •Мал.6.3. Енерґетична діаграма Мал.6.4. Розподіл молекул за
- •Глава 7. Хімічна рівновага.
- •7.1. Константа хімічної рівноваги
- •7.2. Зсув хімічної рівноваги. Принцип Ле-Шательє
- •7.3. Рівновага у гетероґенних системах
- •Константа рівноваги.
- •Глава 8. Поняття про каталіз.
- •8.1. Автокаталіз
- •8.2.Промотори та каталітичні отрути
- •8.3. Селективність каталізаторів
- •8.4. Механізми гомоґенного та гетероґенного каталізу
- •Підставляючи дані нашої задачі, одержуємо:
- •Глава 9. Розчини
- •9.1. Процес розчинення. Типи розчинів
- •9.2. Способи виразу концентрації речовин
- •9.3. Хімічна (гідратна) теорія розчинів д.І. Менделєєва
- •9.4. Теплові ефекти розчинення
- •9.5. Розчинність
- •Глава 10. Властивості розчинів
- •10.1. Тиск пари розчинника над розчином
- •10.2. Температури замерзання та кипіння розчинів
- •10.3. Осмотичний тиск
- •Глава 11. Електролітична дисоціація.
- •11.1. Основні положення теорії електролітичної дисоціації
- •11.2. Ступінь дисоціації
- •11.3. Слабкі електроліти. Константа дисоціації слабких електролітів
- •11.4. Вплив однойменних іонів на дисоціацію слабких електролітів
- •11.5. Розчини сильних електролітів
- •11.6. Електролітична дисоціація води. Йонний добуток води. Водневий показник
- •11.7. Поняття про індикатори
- •11.8. Іонні реакції
- •11.8. Гідроліз солей
- •Типові випадки гідролізу.
- •11.8.1. Ступінь і константа гідролізу
- •Глава 12. Комплексні сполуки
- •12.1. Основні положення координаційної теорії а.Вернера
- •12.2. Класифікація комплексних сполук
- •12.3. Номенклатура комплексних сполук
- •12.3.1. Назви катіонних комплексних сполук
- •12.3.2. Назви аніонних комплексних сполук
- •12.3.3. Назви нейтральних комплексних сполук
- •12.4. Ізомерія комплексних сполук
- •12.5. Дисоціація комплексних сполук
- •Якщо у гібридизації беруть участь d-орбіталі передостаннього рівня, тоді йон називається внутрішньоорбітальним. Іноді у комплексах проявляється йонно-дипольний зв’язок, наприклад в аквакомплексах.
- •Глава 13. Електрохімічні процеси
- •13.1. Хімічні процеси на електродах
- •13.2. Електродний потенціал
- •13.3. Електрохімічний ряд напруг металів
- •13.4. Гальванічний елемент
- •13.5. Окисні й відновні потенціали
- •13.6. Рівняння Нернста
- •13.7. Акумулятори
- •13.8. Паливні елементи
- •13.9. Електроліз
- •13.9.1. Закони Фарадея
- •1. Кількість речовини, що виділяється на електроді під час електролізу, пропорційна кількості електрики, яка пройшла крізь електроліт.
- •2. Однакова кількість електрики виділяє на електродах під час електролізу еквівалентну кількість різних речовин.
- •13.10. Корозія металів
- •0,01 Моль/л 0,1 моль/л
- •Глава 14. Окисно-відновні реакції складання рівнянь окисно-відновних реакцій
- •Контрольні завдання
- •Додатки
- •Додаток 6 – Перехідні коефіцієнти
- •Предметний покажчик
- •Відновлення 18-19, 77, 81, 124, 126, 128, 135-139
- •Водень 14, 17, 37, 75, 125, 130-132, 139
- •Ізомерія 119
- •Лантаноїди 25
- •Натрій 20-21, 69, 89
- •Термодинамічні 8, 54
- •Атомів 33, 50
- •Список рекомендованої літератури
- •Глава 1. Основні поняття та закони хімії ........................ 5
1.3. Закони газового стану
1.3.1. Закон об’ємних відношень гей-люсака
Об’єми газів, що вступають до реакції відносяться один до іншого, а також до об’ємів одержуваних газоподібних продуктів як невеликі цілі числа. Наприклад: 1 л хлору сполучається з одним літром водню, у підсумку чого утворюється 2 л хлороводню.
1.3.2. Закон авогадро
Одним з основних газових законів є закон Авогадро: в однакових об’ємах газів за однакових умов (температура, тиск) містяться однакові кількості молекул.
Наслідки із закону Авогадро:
1.
За
нормальних умов (to
= 0o
C,
p
= 101,3 кПа) один моль будь-якого газу займає
один і той самий об’єм, що дорівнює 22,4
л. Цей об’єм називається молярним
об’ємом газу (VM).
Молярний об’єм – це відношення об’єму
газоподібної речовини до кількості
цієї речовини:
![]()
2. Відношення маси певного об’єму одного газу до маси такого ж об’єму другого газу називається відносною густиною першого газу за другим (позначається літерою D).
Враховуючи,
що із закону Авогадро випливає, що m1
: m2
= M1
: M2,
можна записати, що
![]() або
або![]() .
.
Звичайно
густини визначають за найлегшим газом
– воднем (![]() ).
Молярна маса водню дорівнює 2 г/моль,
звідси М =
2
).
Молярна маса водню дорівнює 2 г/моль,
звідси М =
2![]() .
.
Молекулярна маса речовини у газоподібному стані дорівнює його подвоєній густині за воднем у а.о.м., а молярна маса цієї речовини стільки ж, тільки у г/моль.
Якщо відома густина за повітрям (Dпов.), то М = 29Dпов., бо середня молярна маса повітря дорівнює 29 г/моль.
1.3.3. Закон бойля – маріотта
Для порівняння тисків і об’ємів певної кількості того ж самого газу за різних умов (але сталій температурі) зручно користуватися законом Бойля – Маріотта:
При сталій температурі тиск, який спричинює певна маса газу обернено пропорційний об’єму цієї маси газу: р2/р1 = V1/V2. або pV = const.
1.3.4. ЗАКОН ГЕЙ-ЛЮССАКА
При сталому тискові об’єм газу змінюється пропорційно абсолютній температурі (Т): V1/T1 = V2/T2 або V/T = const.
1.3.5. ОБ’ЄДНАНИЙ ЗАКОН БОЙЛЯ – МАРІОТТА ТА ГЕЙ-ЛЮСАКА
Рівняння
стану газу можна подати у вигляді
співвідношення: 
зручного для порівняння параметрів певного газу в двох його різних станах.
Цей
закон часто використовують для приведення
об’єму до нормальних умов:
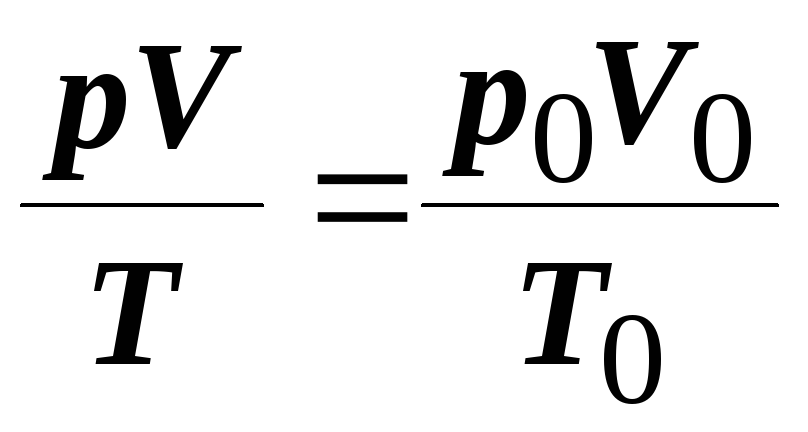 ,
,
де p0, V0, T0 – відповідно тиск, об’єм і температура за нормальних умов (р0 = 101325 Па, T0 = 273К).
1.3.6. РІВНЯННЯ МЕНДЕЛЄЄВА – КЛАПЕЙРОНА
Загальним
рівнянням стану ідеального газу є
рівняння є рівняння Менделєєва –
Клапейрона:
рV
= RT
або
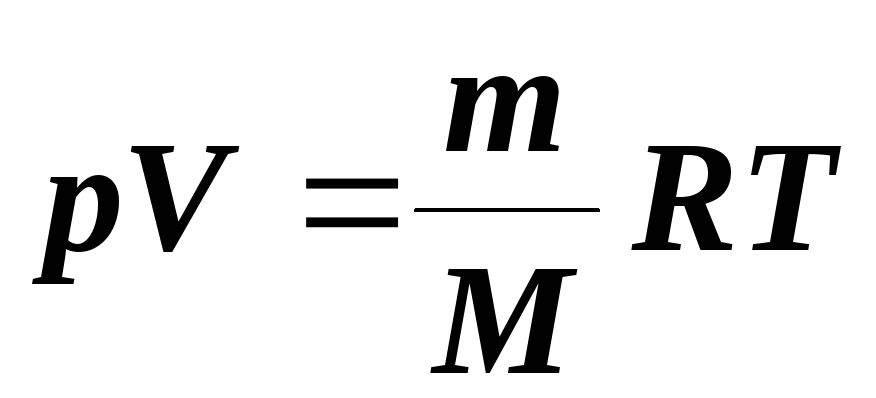 ,
,
де - число молів газу; m – маса газу, кг; р – тиск газу, Па; М – молярна маса газу, кг/моль; V – об’єм газу, м3; Т – температура, К; R – універсальна газова стала (R = =8,314 Дж/(мольК)).
1.4. ПРАВИЛО ДЮЛОНҐА ТА ПТІ
Для визначення атомних мас елементів, що не утворюють летких простих речовин, запропоновано метод, який базується на правилі Дюлонґа та Пті (1819): атомна теплоємність більшості простих речовин у твердому стані приблизно однакова для всіх елементів і дорівнює ~26 Дж/(моль К). Атомна теплоємність (кількість теплоти, потрібна для нагрівання 1 моля атомів елемента на 1 К) є добутком питомої теплоємності (кількості теплоти, необхідної для нагрівання 1 кг речовини на 1 К) на молярну масу атомів елемента.
С = сА, де С і с – атомна та питома теплоємності; А – атомна маса.
Поділивши число 26 на визначену експериментально питому теплоємність речовини, можна знайти наближено значення молярної маси атомів відповідного елемента: А=26/с
Питання для самоперевірки
1. Які основні положення атомно-молекулярного вчення?
2. Що означають поняття: елемент, атом, молекула, формульна одиниця, речовина?
3. Що називається відносною густиною газу? Яка залежність між молекулярною масою газу та його густиною щодо водню, повітря?
Як оцінюються абсолютні маси атомів і молекул? Чόму дорівнюють маси молекул води, фтору?
Що показує число Авогадро?
Що таке еквівалент елемента? Чи є еквівалент елемента сталою величиною?
Обчисліть еквівалентні маси манґану в наступних сполуках: MnSO4, MnО2, K2MnО4, KMnО4.
У чому сутність закону еквівалентів?
