
- •Оглавление
- •Введение
- •3. Применение хроматографических методов для контроля качества водорастворимых витаминов
- •3.1. Использование хроматографических методов для идентификации
- •3.1.1 Применение тонкослойной хроматографии
- •3.1.2 Определение водорастворимых витаминов в биологически-активных веществах и фармацевтических препаратах методом высокоэффективной жидкостной хроматографии
- •3.1.3 Индентификация отдельных водорастворимых витаминов
- •3.2 Применение хроматографии для определения сопутствующих примесей водорастворимых витаминов
- •3.2.1 Тиамин
- •3.2.2 Рибофлавин
- •3.2.3 Аскорбиновая кислота
- •3.2.4 Фолиевая кислота
- •3.2.5 Рутин
- •3.2.6 Никотиновая кислота
- •3.2.7 Цианокобаламин
- •Заключение
- •Литература
3.2.2 Рибофлавин
В медицинской практике применяют рибофлавин и рибофлавина натрия фосфат (рисунок 16). Для определения сопутствующих примесей рибофлавина используют жидкостную хроматографию. Испытания проводят с защитой от яркого света.
Готовят
3 раствора: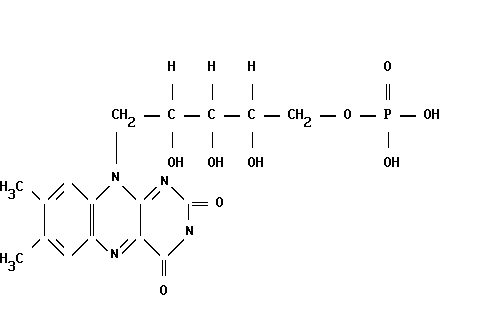
Рисунок 16 – Рибофлавина натрия фосфат
испытуемый раствор: 0,1 г испытуемого образца растворяют в 50 мл воды и доводят подвижной фазой до объема 100,0 мл. 8,0 мл полученного раствора доводят подвижной фазой до объема 50,0 мл;
раствор сравнения (а): 60 мг рибофлавина растворяют в 1 мл кислоты хлористоводородной и доводят водой до объема 250,0 мл. 4,0 мл полученного раствора доводят подвижной фазой до объема 100,0 мл;
раствор сравнения (в): 0,1 г рибофлавина натрия фосфата растворяют в 50 мл воды и доводят объем подвижной фазой до 100,0 мл. 8,0 мл полученного раствора доводят подвижной фазой до объема 50,0 мл.
Условия хроматографирования:
колонка, заполненная силикагелем октадецилсилильным для хроматографии;
подвижная фаза: метанол – раствор калия дигидрофосфата (150:850);
скорость подвижной фазы: 2 мл/мин;
спектрофотометрический детектор, длина волны 266 нм;
объем вводимой пробы: 100 мкл;
время хроматографирования: до полного выхода пика рибофлавина.
Относительное удерживание (по отношению рибофлавина 5´-монофосфату, время удерживания – около 20 мин)
Пригодность хроматографической системы: раствор сравнения (в):
разрешение: не менее 1,5 между пиком рибофлавина 4´-монофосфата и пиком рибофлавина 5´-монофосфата.
Содержание свободного рибофлавина и рибофлавина в форме дифосфатов рассчитывается в процентах исходя из площадей пиков хроматограмме испытуемого раствора и количества свободного рибофлавина в растворе сравнения (а).
Содержание свободного рибофлавина должно быть не более 6,0% в пересчете на сухое вещество.
Содержание рибофлавина в форме дифосфатов должно быть не более 6,0% в пересчете на сухое вещество [14].
3.2.3 Аскорбиновая кислота
Применяют в качестве лекарственного средства кислоту аскорбиновую. Для определения сопутствующих примесей аскорбиновой кислоты применяют жидкостную хроматографию. Растворы готовят непосредственно перед использованием. Готовят:
фосфатный буферный раствор: 6,8 г дигидрофосфата растворяют в воде и доводят до объема около 175 мл этим же растворителем, фильтруют и доводят водой до объема 1000 мл;
испытуемый раствор: 0,5 г испытуемого образца растворяют в подвижной фазе и доводят до объема 10,0 мл эитм же растворителем;
раствор сравнения (а): 10 мг аскорбиновой кислоты примеси С (D - сорбосоновая кислота) растворяют в подвижной фазе и доводят до объема 5,0 мл этим же растворителем;
раствор сравнения (в): 2,5 мл раствора сравнения (а) доводят подвижной фазой до объема 100,0 мл;
раствор сравнения (с): 1,0 мл испытуемого раствора доводят подвижной фазой до объема 200,0 мл.к 1,0 мл полученного раствора прибавляют 1,0 мл раствора сравнения (а);
Условия хроматографирования:
колонка, заполненная силикагелем аминопропилсилильным для хроматографии;
температура 45º С;
подвижная фаза: фосфатный буферный раствор – ацетонитрил (30:70);
скорость подвижной фазы: 1,0 мл/мин;
спектрофотометрический детектор, длина волны 210 нм;
объем вводимой пробы: по 20 мкл испытуемого раствора и растворов сравнения (в) и (с);
время хроматографирования: 2-кратное время удерживания аскорбиновой кислоты.
Относительное удерживание (по отношению к аскорбиновой кислоте, время удерживания – около 8 мин): примесь С – около 1,4.
Пригодность хроматографической системы: раствор сравнения (с):
разрешение: не менее 3,0 между пиками аскорбиновой кислоты и примеси С.
Предельное содержание примесей:
примесь
С (не более 0,1%): на хроматограмме
испытуемого раствора площадь пика
примеси С (D
– сорбосоновая кислота (рисунок 17)) не
должна превышать площадь соответствующего
пика на хроматограмме раствора сравнения
(в);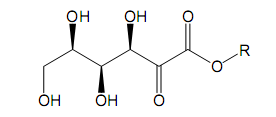
![]()
неспецифицированные примеси ( не более 0,1%): на хроматограмме испытуемого раствора площадь любого пика, кроме основного и пика примеси С, не должна превышать площадь пика примеси С на хроматограмме раствора сравнения (в);
Рисунок 17 - D – сорбосоновая кислота
сумма примесей (не более 0,2%): на хроматограмме испытуемого раствора площадь любого пика, кроме основного, не должна превышать 2-кратную площадь примеси С на хроматограмме раствора сравнения (в).
На хроматограмме испытуемого раствора не учитывают пики с площадью менее 0,5 площади пика примеси С на хроматограмме раствора сравнения (в) (0,05%) [14].
