
- •Оглавление
- •Введение
- •3. Применение хроматографических методов для контроля качества водорастворимых витаминов
- •3.1. Использование хроматографических методов для идентификации
- •3.1.1 Применение тонкослойной хроматографии
- •3.1.2 Определение водорастворимых витаминов в биологически-активных веществах и фармацевтических препаратах методом высокоэффективной жидкостной хроматографии
- •3.1.3 Индентификация отдельных водорастворимых витаминов
- •3.2 Применение хроматографии для определения сопутствующих примесей водорастворимых витаминов
- •3.2.1 Тиамин
- •3.2.2 Рибофлавин
- •3.2.3 Аскорбиновая кислота
- •3.2.4 Фолиевая кислота
- •3.2.5 Рутин
- •3.2.6 Никотиновая кислота
- •3.2.7 Цианокобаламин
- •Заключение
- •Литература
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
УО «ВИТЕБСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ»
КАФЕДРА ФАРМАЦЕВТИЧЕСКОЙ ХИМИИ С КУРСОМ ФПК И ПК
Желубовская
Екатерина Петровна
Курсовая работа
Тема «Применение хроматографических методов для контроля качества водорастворимых витаминов»
Научный руководитель:
Ст. преподаватель Абраменко Леонид Леонидович
Витебск, 2013
Оглавление
Введение…………………………………………………………………….…..3
Основная характеристика водорастворимых витаминов……………...…4
Основная характеристика хроматографических методов………………..9
3 Применение хроматографических методов для контроля качества водорастворимых витаминов…………………………………………………...12
3.1 Использование хроматографических методов для идентификации .12
3.1.1 Применение тонкослойной хроматографии ………………………..12
3.1.2 Определение водорастворимых витаминов в биологически-активных веществах и фармацевтических препаратах методом высокоэффективной жидкостной хроматографии…………………………………………………..13
3.1.3 Идентификация отдельных водорастворимых витаминов…………..15
3.2 Применение хроматографических методов для определения сопутствующих примесей в водорастворимых витаминов……………….…..16
3.2.1 Тиамин………………………………….…………………………….….16
3.2.2 Рибофлавин……………………………………………………….……..17
3.2.3 Аскорбиновая кислота………………………………………………….18
3.2.4 Фолиевая кислота……………………………………………………….19
3.2.5 Рутин……………………………………………………………………..21
3.2.6 Никотиновая кислота…………………………………………………...22
3.2.7 Цианокобаламин……………………………………………………..….22
Заключение……………………………………………………………………….24
Литература……………………………………………………………………….25
Введение
Витамины представляют собой группу веществ различной химической структуры, необходимых в малых количествах для нормальной жизнедеятельности. Ряд витаминов входят в состав ферментных систем и являются своеобразными биологическими катализаторами химических и фотохимических процессов, происходящих в живой клетке. Витамины не синтезируются в организме человека, они поступают с пищей либо в виде самих витаминов, либо в виде провитаминов, ферментов, коферментов [1]. Известно около полутора десятков витаминов. Исходя из растворимости, витамины делят на жирорастворимые — A, D, E, F, K и водорастворимые — все остальные (B, C и др.). Жирорастворимые витамины накапливаются в организме, причём их депо являются жировая ткань и печень. Водорастворимые витамины в существенных количествах не депонируются (не накапливаются) и при избытке выводятся с водой [2].
Для поддержания баланса витаминов в организме широкое применение нашли витаминизированные продукты и биологически активные добавки к пище. Разработка и совершенствование методов определения витаминов является актуальной задачей, от решения которой зависит качество и безопасность подобной продукции. Безусловно, предпочтение отдается методам, требующим минимальной подготовки пробы к анализу при максимальной информативности.
Однако, несмотря на интенсивное развитие инструментальных методов анализа в последние 10 лет, в литературных источниках практически отсутствуют методики определения витаминов в таких объектах, как БАД. Трудности в создании методик во многом обусловлены сложностью объектов анализа, таких как обогащенные продукты, в состав которых входят лекарственное растительное сырье, растительные экстракты, различные минеральные добавки, красители и другие наполнители; низкими концентрациями витаминов в объектах анализа и высокой чувствительностью к термическому, фотоокислительному и химическому воздействиям. Поэтому разработка экспрессных методик одновременного количественного определения витаминов в БАД является актуальной задачей [3].
Основная характеристика водорастворимых витаминов
Роль этих особых органических веществ – витаминов – для организма огромна. Сами по себевитамины не являются ни строительным материалом, ни источником энергии, однако, несмотря на это, нормальная жизнедеятельность организма и даже само существование без этих веществ (в минимально определенных количествах) невозможны [2].
Обмен веществ в организме и крепкий, устойчивый иммунитет – тоже их заслуга. Показанием к применению витаминов может стать витаминная недостаточность, которая развивается из-за нехватки в организме определенного витамина. Чаще всего эту ситуацию провоцируют неполноценное питание и заболевания желудочно-кишечного тракта. Также витамины применяются при комплексном лечении заболеваний печени, сердца, почек, нервной системы и многих других.
Источники витаминов – продукты питания животного и растительного происхождения, благодаря которым они попадают внутрь организма. Многие считают безвредным содержание избыточных доз витаминов, что является абсолютно ошибочным мнением [4].
Важнейшие водорастворимые витамины:
1. Витамин В1 (тиамин)
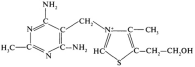 В
химической структуре тиамина (рисунок
1) содержится два кольца – пиримидиновое
и тиазоловое, соединенные метиленовой
связью. Тиамин хорошо растворим в воде,
водные растворы его в кислой среде
выдерживают нагревание до высоких
температур. В нейтральной и щелочной
среде тиамин быстро разрушается [1].
В
химической структуре тиамина (рисунок
1) содержится два кольца – пиримидиновое
и тиазоловое, соединенные метиленовой
связью. Тиамин хорошо растворим в воде,
водные растворы его в кислой среде
выдерживают нагревание до высоких
температур. В нейтральной и щелочной
среде тиамин быстро разрушается [1].
Рисунок 1 – ВитаминВ1
Тиамин содержат преимущественно в продуктах растительного происхождения: в злаках, в крупах (овес, гречиха, пшено), в муке грубого помола, бобовых, фундуке, грецких орехах, дрожжах [7].
Витамин В1 помогает лечить радикулит, полиневрит, парезы, нервные заболевания, сердечно-сосудистую и эндокринную системы, органы пищеварения, кожные болезни, имеющие нервное происхождение [4].
Потребность в сутки – 1,3-2,6 мг [7].
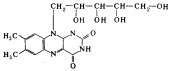
2. Витамин В2 (рибофлавин)
Витамин В2 (рисунок 2)представляет собой метилированное производное изоаллоксазина, к которому в положении 9 присоединен спирт рибитол.
Рибофлавин имеет характерную желто-оранжевую окраску, обусловленную несколькими сопряженными связями в молекуле. Медленно растворим в воде, нерастворим в этаноле и хлороформе. Рибофлавин растворим в растворах кислот и щелочей, т. к. является амфотерным соединением [1].
 Наибольшее
содержание рибофлавина в мясе и молочных
продуктах. Также содержат
витамин В2
зеленый
лук, горох, томаты, злаковые зерна (в
особенности проросшие),
шиповник, капуста, абрикосы.
Наибольшее
содержание рибофлавина в мясе и молочных
продуктах. Также содержат
витамин В2
зеленый
лук, горох, томаты, злаковые зерна (в
особенности проросшие),
шиповник, капуста, абрикосы.
Потребность в сутки – 2-4 мг [7].
Рисунок 2 – Витамин В2
3.Витамин В5 (пантотеновая кислота)
Пантотеновая
кислота (рисунок 3) состоит из α,γ-дигидрокси,
β,β-диметилмасляной кислоты и β-аланила,
связанных пептидной связью [7]. Представляет
собой светло-желтое масло, хорошо
растворимое в воде. Она малоустойчива
и легко гидролизуется по месту пептидной
связи под действием слабых кислот [1].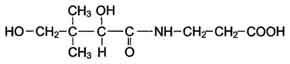
Рисунок 3 – Витамин В5
Содержится в печени, почках, мясе, рыба, бобовых, грибах, спарже, горохе, ржи, пшенице [7].
Помогает излечивать нервные заболевания, хронические ожоги и язвы [4].
Суточная потребность – 5-10 мг [7].
4. Витамин В6 – пиридоксин
Группа
витамина В6состоит
из 3 взаимопревращающихся друг в друга
веществ: пиридоксина, пиридоксоля
(рисунок 4) и пиридоксамина. Данные
вещества по своей химической природе
являются производными пиридина [7].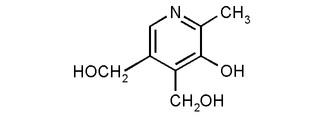
Показано употребление пиридоксина при хорее, бессоннице, дрожательном параличе, заболеваниях нервной системы, пеллагре, гепатитах, токсикозах при беременности [6].
Рисунок 4 - Пиридоксол
Содержится витамин В6 в неочищенных зернах злаковых, стручках гороха, клубнях картофеля, фасоли, грецких орехах, фундуке, мясных продуктах, рыбе, яйцах.
Суточная потребность - от 1,5 до 3 мг [7].
5.Витамин В9 (фолиевая кислота)
Фолиевая кислота (рисунок 5) состоит из следующих компонентов: птеридина, пара-аминобензойной кислоты и L-глутаминовой кислоты. Она практически нерастворима в воде, этаноле, ацетоне, растворима в кислотах и щелочах [1].
Основным
источником фолацина являются зерновые,
мука грубого помола, салат, ранняя
капуста, зеленый горошек [7].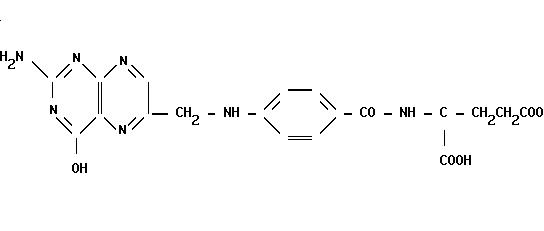
Помогает бороться с болезнями печени (особенно при ожирении), кроветворной системы. Сочетаясь с цианокобаламином, поможет победить анемию, пеллагру, спру, язвенные колиты, крапивницу, глосситы [4].
Рисунок 5 - Витамин В9
Потребность в сутки – не более 200 мг [7].
6.Витамин РР (никотиновая кислота)
Никотиновая кислота представляет собой белый кристаллический порошок, умеренно растворим в воде, мало – в этаноле [1].
Витамин
РР
(рисунок 6)
необходима для улучшения углеводного
обмена, циркуляции крови, тканевого
дыхания, действует сосудорасширяюще,
помогает нормализовать моторную и
секреторную желудочные функции.
Никотиновая кислота полезна для улучшения
состава и секреции поджелудочной железы,
незаменим он в нормализации функции
печени
[5].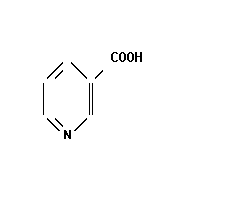
Рисунок 6 - Витамин РР
Назначают никотиновую кислоту при болезнях печени, атеросклерозе, психозе, отравлениях, энтероколитах [4].
Пополнить запасы витамина РР в организме можно употреблением овощей, фруктов, злаков, бобовых, грибов.
Суточная потребность – 15-25 мг [7].
7. Витамин Н (биотин)
Биотин
(рисунок 7) состоит из имидазолового и
тиофенового колец, составляющих
гетероцикл. Боковая цепь представлена
валериановой кислотой [7].
Витамин Н необходим для переноса углекислого газа, обмена жирных кислот и ускорения углеводного обмена [5].
Содержится в горохе, сое, яйцах, овсяной крупе, луке, арахисе, пивных дрожжах, молоке, почках.
Рисунок 7 - Витамин Н
Потребность в сутки - от 0,15 до 0,3 мг [7].
Витамин В12 (цианкобаламин)
Витамин
В12(рисунок
8)состоит из планарной структуры,
сложенной из четырех пиррольных колец
с атомом кобальта в центре, трех
пирролиновых и одного пирролидинового.
Эта система колец называется коррин.
Перпендикулярно плоскости коррина
расположен нуклеотид, содержащий
5,6-диметил-бензимидазол, α-D-рибозу
и остаток фосфорной кислоты. У 13 и 19
углеродных атомов, составляющих ядро
коррина, атомы водорода замещены
метильными группами, ацетамидными и
пропионамидными радикалами. Атом
кобальта находится в трех валентном
состоянии и ковалентно связан с группой
CN.
Вся структура получила название
цианокобаламин [7]. Он представляет собой
кристаллический порошок темно-красного
цвета, умеренно растворимый в воде,
практически нерастворим в эфире и
хлороформе [1].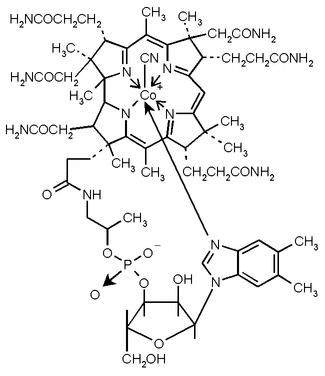
Рисунок 8 - Витамин В12
Витамин В12 оказывает антианемическое действие, влияет на синтез белков и нуклеиновых кислот. Полезен цианкобаламин детям для улучшения общего состояния и стимулирования роста. Это очень важный витамин, который помогает в укреплении иммунитета, накоплении протеина, ускорении обмена веществ, нормализации кровяного давления и участвует во многих других важных процессах [5].
Витамин В12 содержат зеленолистные растения, цельные зерна, проросшее зерно, пивные дрожжи, орехи. Также пополнить запасы витамина В12 в организме можно, употребляя в пищу говяжье мясо, морскую капусту, печень и почки, рыбу, яйца, сыр и молоко.
Необходимая потребность в сутки – 3 мкг [7].
9. Витамин С (аскорбиновая кислота)
Витамин
С (рисунок 9) по химическому строению
представляет γ-лактон 2,3-дегидро-L-гулоновой
к-ты
[7].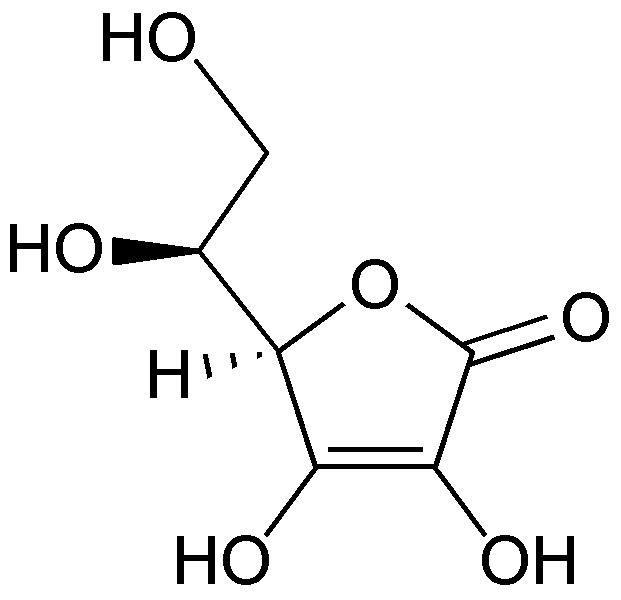
Она представляет собой белый кристалический порошок, легко растворимый в воде, медленно растворимый в этаноле и практически нерастворим в эфире, бензоле и хлороформе [1].
Аскорбиновая кислота регулирует окислительно-восстановительные процессы и обмен веществ, способствуя свертыванию крови, повышению сопротивляемости организма к различным инфекциям [6].
Рисунок 9 - Витамин С
Содержат витамин С многие овощи, фрукты, ягоды, сушеные плоды шиповника, красный перец, хрен, петрушка, укроп, иглах хвои [7].
Витамин С применяется при авитаминозах, интоксикациях, кровотечениях, различных инфекциях, печеночных болезнях, диатезах, токсикозе и во многих других случаях [4].
Потребность в сутки – от 60 до 100 мг [7].
10. Витамин Р (рутин (рисунок 10))
Витамин
Р –
биологически активные вещества –
биофлавоноиды. Рутин
представляет собой зеленовато-желтый
мелкокристаллический, нерастворим в
воде и хлороформе, растворим в кипящем
этаноле порошок[1]. С
помощью рутина повышается прочность
капилляров
[6]. 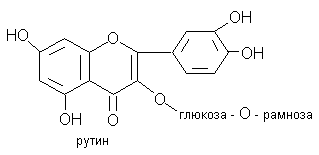
Рисунок 10 - Рутин
Источниками содержания витамина Р являются клюква, абрикосы, черная смородина, персики, крыжовник, черешня, вишня.
Суточная норма потребления около 30 мг [7].
Основная характеристика хроматографических методов
Хроматография – метод разделения смесей веществ или частиц, основанный на различии в скоростях их перемещения в системе, состоящей из несмешивающихся и движущихся друг относительно друга фаз.
В качестве неподвижной фазы в хроматографическом процессе выступает твердое вещество или пленка жидкости, нанесенная на твердый носитель, а в качестве подвижной фазы – жидкость или газ, протекающий через неподвижную фазу.
Хроматография
является динамическим процессом. При
перемещении через неподвижную фазу
подвижная фаза встречает на своем пути
все новые и новые слои сорбента, что
сопровождается многократными повторениями
актов сорбции и десорбции разделяемых
веществ (рисунок 11). 
В основе классификации хроматографических методов может быть положены:
Рисунок 11 – Динамический процесс хроматограммы
агрегатное состояние подвижной и неподвижной фазы;
геометрическая форма неподвижной фазы;
преобладающий механизм разделения;
цель проведения;
способ получения хроматограммы и т.д [8].
По агрегатному состоянию применяемых фаз. Согласно этой классификации хроматографию подразделяют на газовую и жидкостную. Газовая включает газожидкостную и газоадсорбционную хроматографию. Жидкостная хроматография подразделяется на жидкостно – жидкостную, жидкостно – адсорбционную и жидкостно – гелевую. Первое слово в этой классификации характеризует агрегатное состояние подвижной фазы.
По механизмам разделения, т.е. по характеру взаимодействия между сорбентом и сорбатом. По этой классификации хроматографию подразделяют на следующие виды:
1. адсорбционная хроматография – разделение основано на различии в адсорбируемости разделяемых веществ твердым адсорбентом;
2. распределительная хроматография – разделение основано на различии в растворимости разделяемых веществ в неподвижной фазе (газовая хроматография) и на различии в растворимости разделяемых веществ в подвижной и неподвижной жидких фазах;
3. ионообменная хроматография – разделение основано на различии в способности разделяемых веществ к ионному обмену;
4. проникающая хроматография – разделение основано на различии в размерах или формах молекул разделяемых веществ, например, при применении молекулярных сит (цеолитов);
5. осадочная хроматография – разделение основано на образовании различных по растворимости осадков разделяемых веществ с сорбентом;
6. адсорбционно-комплексообразовательная хроматография – разделение основано на образовании координационных соединений различной прочности в фазе или на поверхности адсорбента.
Следует иметь в виду, что очень часто процесс разделения протекает по нескольким механизмам.
По применяемой технике:
1. колоночная хроматография – разделение веществ проводится в специальных колонках;
2. плоскостная хроматография: а – бумажная – носителем неподвижной жидкой фазы является специальная бумага, неподвижной фазой считается жидкость, находящаяся в порах хроматографической бумаги; б – тонкослойная – сорбент нанесен в виде тонкого слоя на пластинку, изготовленного из стекла, алюминиевой фольги, различных полимеров [9].
В колоночной и тонкослойной хроматографии можно использовать любой из приведенных выше механизмов разделения, в бумажной хроматографии чаще всего применяют распределительный и ионообменный механизмы.
По способу относительного перемещения фаз различают фронтальную, или элюэнтную, и вытеснительную хроматографию.
Фронтальный метод. Это простейший по методике вариант хроматографии. Он состоит в том, что через колонку с адсорбентом непрерывно пропускают анализируемую смесь, например, компонентов А и В в растворителе. В растворе, вытекающем из колонки, определяют концентрацию каждого компонента и строят график в координатах концентрация вещества – объем раствора, прошедшего через колонку. Эту зависимость обычно и называют хроматограммой или выходной кривой.
Вследствие сорбции веществ А и В сначала из колонки будет вытекать растворитель, а затем растворитель и менее сорбирующийся компонент А, затем и компонент В и, таким образом, через некоторое время состав раствора при прохождении через колонку меняться не будет. Метод применяется, например, для очистки раствора от примесей, если они сорбируются существенно лучше, чем основной компонент, или для выделения из смеси наиболее слабо сорбирующегося вещества.
Проявительный (элюентный) метод. При работе по этому методу в колонку водят порцию анализируемой смеси, содержащей компонентыА и В в растворителе, и колонку непрерывно промывают газом-носителем или растворителем. При этом компоненты анализируемой смеси разделяются на зоны: хорошо сорбирующееся вещество В занимает верхнюю часть колонки, а менее сорбирующийся компонент А будет занимать нижнюю часть.
В газе или растворе, вытекающем из колонки, сначала появляется компонент А, далее – чистый растворитель, а затем компонент В. Чем больше концентрация компонента, тем выше пик и больше его площадь, что состовляет основу количественного хроматографического анализа. Проявительный метод дает возможность разделять сложные смеси, он наиболее часто применяется в практике. Недостатком метода является уменьшение концентрации выходящих растворов за счет разбавления растворителем или газом-носителем.
Вытеснительный метод. В этом методе анализируемую смесь компонентов А и В в растворителе вводят в колонку и промывают раствором вещества D (вытеснитель), которое сорбируется лучше, чем любой из компонентов анализируемой смеси.
Концентрация раствора при хроматографировании не уменьшается, в отличие от проявительного метода. Существенным недостатком вытеснительного метода является возможное наложение зоны одного вещества на зону другого, поскольку зоны компонентов в этом методе не разделены зоной растворителя [10].
Для идентификации веществ используют хроматографическую характеристику время удерживания (tR), представляющую собой время от момента вводы пробы до момента регистрации максимума пика. В идеальном случае время удерживания не зависит от концентрации вещества, но зависит от его природы, а также от природы подвижной и неподвижной фазы и условий хроматографирования. Время удерживания вещества зависит от упаковки сорбента и поэтому может изменяться при переходе от одной колонки до другой. Более надежной характеристикой является исправленное время удерживания (tR´), которое равно разности между временем удерживания данного вещества и несорбируемого компонента.
В
качестве аналитического сигнала в
хроматографии, используемого для
количественного определения веществ,
используют высоту или площадь
хроматографического пика (рисунок 12),
которые пропорциональны содержанию
вещества в хроматографической зоне
[8].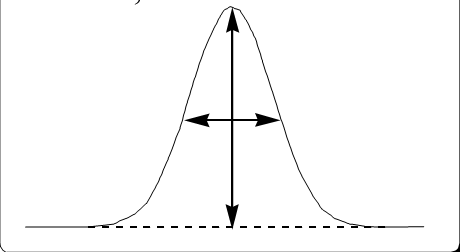
![]()
Рисунок 12 – Хроматографический пик
