
2579
.pdf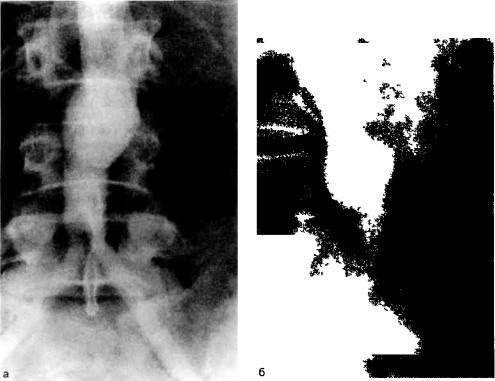
ких масс в полости аневризматического мешка не всегда позволяет ус тановить истинные размеры анев ризмы и может повлечь за собой ложноотрицательный результат. Только при значительных размерах прямая проекция обеспечивает надежную информативность.
Показания и противопоказания к повторным операциям на аортобедренном сегменте:
• наличие тромбоза одной или обеих браншей аортобедренного трансплантата при наличии ишемии не ниже ПБ степени по классификации А.В.Покровского;
•стеноз дистального анастомоза более 70 %;
•наличие ложной аневризмы дистального или проксимального анастомоза независимо от ее размеров.
Больным с плохими путями оттока, окклюзией основного ствола глубокой артерии бедра и подколенной артерии ниже щели коленного сустава повторные оперативные вмешательства показаны при хронической ишемии III—IV степени. В тех случаях, когда у пациентов с функционирующими аортобедренными трансплантатами при окклюзии бедрен-но- подколенного сегмента сохранялась ПБ—IV степень ишемии при наличии проходимой подколенной артерии и артерии голени, показано бедренно-подколенное шунтирование.
Общими противопоказаниями к выполнению реконструктивных вмешательств являются инфаркт миокарда, нарушение мозгового кровообращения (менее 3 мес), терминальная стадия почечной недостаточности, сердечно-легочные забо-
Рис. 6.65. Ангиограмма. Ложная аневризма проксимального анастомоза. а— прямая;б — боковая проекция.
160
левания в стадии декомпенсации, неоперабельные онкологические заболевания.
Местными противопоказаниями служат гангрена стопы с переходом на проксимальный отдел или нижнюю треть голени; тотальная окклюзия глубокой и поверхностной бедренной артерии на протяжении, создающая техническую неосуществимость наложения разгрузочного анастомоза на уровне бедра при выполнении одномоментных многоэтажных реконструкций; окклюзия подколенной и всех берцовых артерий; острая ишемия свыше ША степени. Таким пациентам показана первичная ампутация конечности.
Выбор характера операции у больных с реокклюзиями. В отношении выбора видов повторных оперативных вмешательств на аортобедренном сегменте не существует единого подхода. Большинство авторов предпочитают методику непрямой тромбэктомии с реконструкцией дистального анастомоза [Тхор С.Н., 1987; Покровский А. В., Зотиков А.Е., 1996; Brewster D. et al., 1987]. Выпол-
нение непрямой тромбэктомии с реконструкцией дистального анастомоза показано в тех случаях, когда удается восстановить адекватный кровоток из бранши протеза, однако в структуре повторных операций непрямые тромбэктомии с реконструкцией дистального анастомоза составляют лишь 58—62 % [Гамбарин Б.Л.,
1982; Brewster D. et al, 1987]. Успех или неудача при выполнении тромбэктомии из бранши протеза обусловлены как состоянием аорты выше проксимального анастомоза, так и временем, прошедшим с момента возникновения тромбоза.
Ряд исследователей ограничивают возможность выполнения тромбэктомии сроком 2—3 мес после тром-
боза [Bernhard et al., 1977]. Другие ав-
торы сообщают об успешных тромбэктомиях через 6 и даже 7 мес [Conn et al, 1970; Brewster D. et al., 1987].
Так, если в первый месяц с момента
11 - 4886
возникновения тромбоза успех тромбэктомии достигает 95 %, то в более поздние сроки адекватную тромбэктомию удается выполнить лишь в 80 % случаев [Brewster D. et al., 1987].
Большую роль в успехе тромбэктомии играет тип протеза. Выполнение тромбэктомии из протезов из политетрафторэтилена (гортекс, экофлон) наиболее затруднительно и возможно лишь в более ранние сроки. Наиболее легко тромбэктомия осуществима из отечественных тканых протезов "Север". Так, нам удавалось выполнять тромбэктомию из этих протезов в сроки более 2 лет с момента наступления тромбоза.
Ряд авторов предпочитают повторное аортобедренное протезирование при тромбозе протеза с заменой тромбированной бранши новой
[Grawford et al., 1977; Volmar, 1980; Benhamou et al., 1984]. В качестве ар-
гумента эти исследователи приводят данные о происходящих структурных нарушениях в тромбированной бранше протеза. Вместе с тем нет единого мнения о том, что замена протеза статистически достоверно дает лучшие результаты, чем непрямая тромбэктомия с реконструкцией анастомоза. Большинство хирургов стоят на позиции, что повторное аортобедренное протезирование показано лишь при невозможности выполнения адекватной тромбэктомии или при поражении аорты выше проксимального анастомоза [Говорунов Г.В., 1987; Покровский А.В. и др., 1990; Затевахин И.И. и др., 1993; Bernhard et al., 1987]. Прежде всего это обусловлено более высокой госпитальной летальностью при замене аортального протеза, которая колеблется от 5,7 до 20 % [Crawford et al., 1977; Benhamou et al., 1984; Szilagyi et al., 1986; Ernst et al., 1987], в то время как летальность при тромбэктомиях с резекцией анастомоза составляет от 1 до 1,9 % и не превышает 3 % [Brewster et al., 1987]. При невозможности или неадекватности выполнения
161
тромбэктомии у наиболее тяжелых больных возможно выполнение перекрестного шунтирования от функционирующей бранши [Crawford et al., 1977; Benhamou et al., 1984].
Причиной возникновения тромбозов служат гемодинамические нарушения, в первую очередь возникающие из-за стенозов дистальных анастомозов или прогрессирования процесса в дистальном артериальном русле. В связи с этим тромбэктомия в подавляющем большинстве случаев должна завершаться реконструкцией дистального анастомоза. Интраоперационными критериями адекватности тромбэктомии служили появление отчетливой пульсации на бранше протеза и наличие пульсирующего струйного кровотока.
Показаниями к повторным аортобедренным реконструкциям являются:
•тромбоз обеих и основной браншей протеза;
•наличие низко наложенного проксимального анастомоза при тромбозах одной бранши протеза;
•поражение аорты, выявляемое ангиографически выше зоны проксимального анастомоза;
•невозможность получения адекватного кровотока из браншей после
выполнения неоднократных тромбэктомии во время реконструкций дистальных анастомозов;
• наличие аневризмы проксимального анастомоза.
Чрезвычайно важным является восстановление кровотока по глубокой артерии бедра, поскольку у 85 % пациентов с реокклюзиями шунтов имеется окклюзия поверхностной бедренной артерии [Brewster D. et al.,
1987]. Включение в кровоток глубокой артерии бедра при повторных операциях выполняют более чем у 75 % больных. Причиной неадекватности восстановления кровотока по глубокой артерии бедра может быть анатомо-функциональное состояние глубокой артерии бедра (плохие перетоки из системы глубокой артерии
162
бедра в подколенную), недостаточный ее диаметр (менее 4 мм) или короткий ствол. В этих случаях тромбэктомию с реконструкцией дистального анастомоза необходимо дополнить одномоментным бедренноподколенным или бедренно-берцо- вым шунтированием. Необходимость выполнения одномоментных комбинированных вмешательств колеблется от 5 до 32 % [Harris, 1985; Szilagyi, 1986; Brewster et al., 1987]. При ок-
клюзии глубокой артерии бедра на протяжении выполняют аортоподколенное шунтирование с разгрузкой в огибающую артерию бедра.
Выбор тактики лечения у больных с ложными аневризмами анастомо-
зов. Выбор тактики лечения ложных аневризм анастомозов зависит прежде всего от этиологии ложной аневризмы и ее локализации. Хирургическое лечение ложных аневризм, обусловленных парапротезной инфекцией, рассматривается в соответствующем разделе (см. "Парапротезная инфекция").
Наличие ложной аневризмы анастомоза независимо от ее размеров является показанием к хирургическому вмешательству, поскольку ложные аневризмы имеют тенденцию к росту, высока вероятность их разрыва и эмболизации мелких тромбов в дистальное артериальное русло
[Говорунов Г.В., 1987; Szilagyi et al., 1986; Gawenda et al, 1994]. Это обус-
ловлено тем, что формирование ложных аневризм связано с разрывом или прорезыванием швов по линии анастомоза; кроме того, возникающая в этой области турбуленция потока крови вызывает прогрессивный рост аневризмы, что повышает вероятность тромбоза в области анастомоза и тромбоэмболии в дистальное артериальное русло.
При неинфицированных аневризмах дистального анастомоза подавляющее большинство хирургов применяют методику резекции ложной аневризмы. При наличии небольших и средних размеров ложных анев-
ризм дистального анастомоза (менее 5 см), которые пальпаторно определяются ниже пупартовой связки, используют бедренный доступ. Забрюшинный доступ был показан в тех случаях, когда верхний полюс аневризмы уходит под пупартову связку, в случаях ранее выполненных высоких дистальных анастомозов, а также при разрывах ложных аневризм или их инфицировании. Малооправданным является предложение В.И.Трипониса (1982) проводить повторное протезирование обходным путем, оставляя саму аневризму. Практически все хирурги отказались от предложенного Christensen и соавт. (1977) ушивания дефекта в анастомозе даже при его небольших размерах. При резекции ложных аневризм дистального анастомоза последний необходимо накладывать по типу "конец в конец".
Особую группу составляют пациенты с ложными аневризмами проксимального анастомоза. Резекция аневризмы с протезированием аорты аллонадставкой из основной бранши сосудистого протеза является операцией выбора. Исключение составляют больные с инфицированными трансплантатами (см. "Парапротезная инфекция"). Мнение некоторых авторов [Скрипниченко Д.Ф., Иваненко А.А., 1986], что все ложные аневризмы проксимального анастомоза являются инфицированными, малообосновано. Поэтому операция экстраанатомического шунтирования должна выполняться лишь при доказанном инфекционном генезе аневризмы.
Широкое использование подмы- шечно-бедренных шунтов, предлагаемое некоторыми авторами, менее рационально, чем повторные реконструктивные операции, в связи с более высоким риском тромботических осложнений [Нерр et al., 1988; Mason et al, 1989; Harris et al., 1990; Schroe et al., 1990; Dujardin et al., 1991; Schneider et al, 1992].
Повторное аортобедренное шун-
и*
тирование целесообразно выполнять лишь при наличии аневризмы проксимального и дистального анастомозов или при сочетании аневризмы проксимального анастомоза с реокклюзиями в области дистального анастомоза или тромбозе бранши
[Kraus et al., 1994].
6.11.1. Техника повторных операций на аортобедренном сегменте. Тромбэктомия с реконструкцией дистального анастомоза
Иссекают старый послеоперационный рубец. Пальпаторно находят тромбированную браншу протеза, которая определяется в виде плотного непульсирующего жгута. Скальпелем рассекают соединительную капсулу вокруг протеза выше зоны дистального анастомоза. При сохраненном кровотоке (при стенозах анастомоза) выделяют переднюю поверхность анастомоза, глубокую и поверхностную бедренные артерии без пересечения бранши протеза.
При тромбозе бранши протеза ее пересекают до выделения бедренных сосудов и дистального анастомоза, что значительно облегчает выделение задней стенки анастомоза, общей и глубокой артерии бедра. Следует помнить, что браншу целесообразно пересекать максимально близко к дистальному анастомозу, оставляя достаточно длинный участок бранши ниже пупартовой связки, что создает дополнительные удобства при выполнении тромбэктомии. Тупым и острым путем, поднимая кверху оставленный участок бранши в области дистального анастомоза, выделяют заднюю стенку анастомоза, глубокую и поверхностную бедренные артерии. При окклюзии поверхностную бедренную артерию пересекают. Глубокую артерию выделяют до малоизмененного участка. Иссекают дистальный анастомоз. Глубокую артерию бедра рассекают по передней стенке. При получении из нее удовлетворительного ретроградного
163

Рис. 6.66. Тромбэктомия с протезированием аллонадставкой.
а, б, в — этапы вмешательства.
кровотока накладывают косой ана- |
бедренные артерии ниже места ранее |
|||||||
стомоз между аллонадставкой и глу- |
наложенного |
анастомоза. |
Браншу |
|||||
бокой артерией бедра. Из бранши |
протеза и бедренные артерии берут |
|||||||
протеза выполняют тромбэктомию |
на держалки. Выделяют боковые стен- |
|||||||
металлическими или ультразвуковы- |
ки ложной аневризмы. Пережимают |
|||||||
ми петлями. Сначала петлями враща- |
браншу протеза и бедренные артерии. |
|||||||
тельными движениями тромб отсла- |
Браншу пересекают. Вскрывают лож- |
|||||||
ивают от стенок протеза. Затем кате- |
ную аневризму. При сохраненной |
|||||||
тером Фогарти удаляют тромботичес- |
проходимости |
по общей |
бедренной |
|||||
кие массы до получения хорошего |
артерии ее ушивают. При ложных |
|||||||
центрального кровотока (рис. 6.66). |
аневризмах дистального |
анастомоза |
||||||
Во время введения петель или катете- |
обязательным правилом является на- |
|||||||
ра |
в проксимальном |
направлении |
ложение дистального анастомоза по |
|||||
чрескожно пережимают |
контралате- |
типу конец в конец. При стенозе глу- |
||||||
ральную бедренную артерию для пре- |
бокой или поверхностной бедренной |
|||||||
дотвращения тромбоэмболии в эту |
артерии выполняют один из вариан- |
|||||||
конечность. |
|
|
тов профундопластики (см. "Синд- |
|||||
|
|
|
|
ром Лериша"). |
|
|
|
|
6.11.2. Резекция ложной аневризмы |
|
|
|
|
|
|||
дистального анастомоза |
|
|
6.11.3. Повторное аортобедренное |
|||||
с реконструкцией аллонадставкой |
протезирование |
|
|
|||||
В |
большинстве случаев |
ложные |
На бедрах выделяют бранши протеза |
|||||
аневризмы дистального |
анастомоза |
(см. выше). Для выделения прокси- |
||||||
оперируют через бедренный доступ. |
мального |
анастомоза |
используют |
|||||
Лишь при больших ложных аневриз- |
повторный лапаротомный доступ или |
|||||||
мах, высоко наложенных дистальных |
торакофренолюмботомию (см. "Син- |
|||||||
анастомозах у некоторых |
больных |
дром Лериша"). При высоком распо- |
||||||
требуется выполнение забрюшинно- |
ложении ложных аневризм прокси- |
|||||||
го доступа (см. "Синдром Лериша"). |
мального |
анастомоза или |
высоком |
|||||
Выделяют браншу протеза выше лож- |
расположении тромбированного про- |
|||||||
ной аневризмы. Из рубцов выделяют |
ксимального анастомоза предпочти- |
|||||||
164 |
|
|
|
|
|
|
|
|

тельнее использовать торакофрено- |
лонадставкой, зажим перемещают на |
|||
люмботомический доступ по девято- |
аллонадставку, которую анасто- |
|||
му межреберью (см. Доступы к аорте |
мозировали |
с основной браншей |
||
в разделе "Синдром Лериша"). При |
старого протеза. После формирова- |
|||
операциях по поводу ложных анев- |
ния проксимального анастомоза при |
|||
ризм проксимального анастомоза и |
отсутствии |
признаков |
инфицирова- |
|
реокклюзий основной бранши важ- |
ния старого протеза для проведения |
|||
ным моментом является предвари- |
браншей рекомендуется пользовать- |
|||
тельное выделение аорты выше зоны |
ся следующим приемом: раздельно |
|||
проксимального анастомоза. |
После |
выделяют старые бранши протеза на |
||
этого производят пережатие |
аорты |
2—3 см ниже их отхождения от ос- |
||
на 2—3 см выше ранее наложенного |
новной бранши. Бранши старого |
|||
анастомоза, пережимают дисталь- |
протеза пересекают, проксимальный |
|||
ную часть аорты или подвздошные |
участок их перевязывают, затем |
|||
артерии, бранши протеза. Приступа- |
новые бранши подводят к месту пе- |
|||
ют к вскрытию просвета ложной |
ресечения старых браншей и двумя |
|||
аневризмы. При отсутствии призна- |
швами подшивают к ним. Тупым пу- |
|||
ков инфицирования анастомоза края |
тем по ходу старого протеза из бед- |
|||
основной бранши освежают, иссека- |
ренного доступа отслаивают капсулу |
|||
ют зону ранее наложенных швов. |
вокруг старого протеза. После этого |
|||
Аорту пересекают, дистальный сег- |
старые бранши, подтягивая книзу, |
|||
мент ушивают непрерывным |
швом |
удаляют, проводя тем самым новые |
||
(рис. 6.67). После этого накладывают |
бранши по старому ложу протеза. |
|||
проксимальный анастомоз по |
типу |
Затем накладывают |
дистальные |
|
конец в конец между аортой и ал- |
анастомозы. |
|
|
|
Рис. 6.67. Повторное аортобифеморальное протезирование при ложной аневризме проксимального анастомоза, а, б, в — этапы операции.
165
6.11.4. Ближайшие и отдаленные результаты повторных реконструкций
Мероприятия ближайшего послеоперационного периода направлены на предотвращение специфических местных осложнений: кровотечения, тромбоза и инфицирования трансплантата. Необходимым условием контроля за тщательностью гемостаза является дренирование ран. Следует помнить, что при использовании тканых протезов нельзя применять прямые антикоагулянты, поскольку при их применении резко возрастает угроза кровотечений из протеза. Используют дезагрегантную терапию, включающую введение декстранов, трентала и сосудорасширяющих препаратов. Для предотвращения возникновения ранней парапротезной инфекции применяют комплекс мероприятий, в числе которых хирургические приемы и проведение адекватной антибиотикотерапии. Послеоперационная летальность при реконструкциях дистального анастомоза составляет не более 2 %, при повторном аортобедренном протезировании колеблется от 5 до 15 и даже 20 %. Хуже результаты при осложнениях, обусловленных инфекцией трансплантатов. Основная причина летальности в ближайшем послеоперационном периоде у больных после повторных операций на аортобедренном сегменте обусловлена кардиальными осложнениями.
Отдаленные результаты повторных реконструктивных вмешательств сравнимы с результатами первичных операций на аортобедренном сегменте.
Согласно большинству литературных наблюдений, они несколько хуже, чем при первичных вмешательствах [Трипонис В.И., 1982; Клионер Л.И., Арбузов И.В., 1987; Evans et al., 1987; Olsen et al., 1988; Nevelsteenetal., 1991; Valentine etal., 1995].
По материалам D.Brewster и соавт. (1987), кумулятивная 3-, 5- и 10-лет-
166
няя проходимость составила соответственно 75, 74 и 62 %. A.Nevelsteen и соавт. (1991), сравнивая результаты первичных и повторных операций, отметили, что 10-летняя проходимость при повторных операциях равна 61 %, а при первичных — 74 %. В то же время на основе анализа результатов более 1700 операций, выполненных в Детройтском сосудистом центре, авторами не было выявлено статистически достоверного различия в кумулятивной проходимости протезов после первичных и повторных реконструктивных вме-
шательств [Szilagyi et al., 1986].
Выполнение многократных оперативных вмешательств у больных с реокклюзиями позволяет значительно улучшить отдаленные результаты повторных операций.
Завершая раздел, посвященный повторным операциям на аортобедренном сегменте, следует подчеркнуть, что основными причинами развития тромботических осложнений являются прогрессирование процесса в дистальном русле и стенозы анастомозов. Реконструкция дистального анастомоза с протезированием является операцией выбора у больных с односторонними тромбозами трансплантатов и стенозами анастомозов. Мы считаем, что расширение показаний к повторному аортобедренному вмешательству вряд ли оправдано и должно ограничиваться случаями тромбозов основной бранши, ложных аневризм проксимальных анастомозов, невозможностью выполнения адекватной тромбэктомии и распространением атеросклеротического процесса выше или в области проксимального анастомоза.
Предпочтительным является выполнение повторных вмешательств у больных до возникновения тромботических осложнений в случаях гемодинамически значимых стенозов анастомозов. У больных с тромбозами и рестенозами на почве прогрессирования атеросклеротического процесса отдаленные результаты
наиболее неблагоприятные. Этим па- |
ких поражений//Вестн.хир. — 1990. — № 11. |
|
циентам показана превентивная ме- |
- С. 59-61. |
|
дикаментозная терапия, направлен- |
Покровский А.В., Дан В.Н., Каразеев Г.Л. |
|
ная на снижение уровня холестерина |
Диагностика ложных аневризм прокси- |
|
и подавление активности атероскле- |
мальных анастомозов после аортобедрен-ных |
|
реконструктивных операций//Кар-диология. - |
||
ротического процесса (см. "Синдром |
||
1993. - № 9. - С. 20-25. |
||
Лериша", "Атеросклероз аорты и ар- |
Benchamou А.С, Kieffer E., Tricot J. et al. |
|
терий"). |
||
"Redo" surgery for late aortofemoral graft |
||
|
occlisive failures // J. Cardiovasc.Surg. — 1984. |
|
Литература |
- Vol.25. - P. 118-125. |
Вахидов В.В., Гамбарин Б.Л., Бахритди-нов Б.Ш., Трынкин А.В. Результаты реваскуляризации нижних конечностей через глубокую артерию бедра при тяжелой ишемии//Хирургия. - 1987. - № 12. - С. 9-12.
Волколаков Я.В., Тхор С.Н. Реконструктивная хирургия брюшной аорты. — Рига: Зи-натне,
1981.-167 с.
Затевахин И.И., Говорунов Г.В., Сухарев И. И.
Реконструктивная хирургия поздней реокклюзии аорты и периферических артерий. — М, 1993.
Зырянов Б.Н., Чернов А.И., Коломиец Л.А.
Ложные аневризмы на месте анастомозов синтетических протезов//Вестн.хир. — 1980. - Т. 124, № 1. - С. 87-89.
Орехова Н.М., Тарарак Э.М., Шехонин Б. В. и
др. Морфология бедренных артерий в области постоперационной реокклюзии дистального анастомоза и атеросклеротичес-
Branchereau, Espinoza H., Rudondy P. et al.
Descending thoracic aorta as an inflow source for late occlusive failares following aortoiliac reconstruction//Ann.Vase.Surg. — 1991. — Vol. 5, N 1. - P. 8-15.
Brewster D., Darling С Optimal methods of aortoiliac reconstruction//Surgery. — 1978. — Vol.84. - P. 739-748.
Crawford E.S., Bomberger R.A., Glaeser D. et al.
Aortoiliac occlusive disease: Factors influencing survival and function following reconstructive operation over a twenty-five year period//Surgery. - 1981. - Vol.90. - P. 1055-1067.
Nevelsteen A., Wouters L., Suy R. Aortofemoral Dacron Reconstruction for Aorto-piliac Occlusive Disease: A 25-year Survey // Europ. J. Vase. Surg. - 1991. - Vol.5, N 2. - P. 179-187.
Szilagyi E., Elliot J., Smith R. et al. A Thirty survey of the reconstructive surgical treatment of aortoilliac occlusive disease//?Vase.Surg. — 1986. - N 3. - P. 421-436.
6.12. Парапротезная инфекция в сосудистой хирургии
Развитие инфекции после импланта- |
ся от 25 до 88 % в зависимости от ло- |
|||
ции сосудистых протезов является |
кализации |
и |
распространенности |
|
одним из наиболее грозных ослож- |
инфицирования [Balas, 1997], а час- |
|||
нений в сосудистой хирургии. Не- |
тота ампутаций достигает 45 %. Час- |
|||
смотря на разработку новых видов |
тота развития |
ложных |
аневризм |
|
трансплантатов и совершенствование |
проксимального |
анастомоза колеб- |
||
антибактериальной терапии, частота |
лется, по данным Broek, Elkelboom |
|||
развития инфекции вокруг сосудис- |
(1997), от 1,8 до 5,9 %, а частота лож- |
|||
тых трансплантатов колеблется, по |
ных аневризм дистального анастомо- |
|||
сообщению Perker и соавт. (1998), от |
за — от 6,1 до 16,3 %. Наиболее тяже- |
|||
1 до 6 % и не имеет тенденции к сни- |
лым проявлением инфекции остается |
|||
жению. По данным того же автора, |
образование аортодуоденального сви- |
|||
ежегодно в США наблюдаются более |
ща. По обобщенным данным клиники |
|||
10 000 пациентов с инфекцией транс- |
Мейо, частота развития аортодуоде- |
|||
плантатов. |
нального |
свища после |
резекции |
|
Даже в лучших европейских и аме- |
аневризмы брюшной аорты состав- |
|||
риканских клиниках летальность при |
ляет 0,14 (5 из 3650) и 0,6 % (10 из |
|||
этом виде осложнений колеблет- |
1792) после аортобедренных реконс- |
|||
|
|
|
|
167 |
трукций по поводу облитерирующих |
6.12.1. Патогенез парапротезной |
||||||||||
поражений аорты и подвздошных ар- |
инфекции |
|
|
|
|||||||
терий. |
|
|
|
|
|
Особенностями инфекционного про- |
|||||
По |
данным |
Hicks, |
Greenhalgh |
||||||||
цесса вокруг синтетического матери- |
|||||||||||
(1997), |
|
летальность при инфекции |
|||||||||
|
ала являются склонность к хрониза- |
||||||||||
аортобедренных трансплантатов до- |
|||||||||||
ции воспаления, толерантность к про- |
|||||||||||
стигает |
33—58 %, а при инфекции |
||||||||||
водимому консервативному лечению |
|||||||||||
бедренно-подколенных |
шунтов |
со- |
|||||||||
и отсутствие тенденции к самостоя- |
|||||||||||
ставляет 22 %. Частота потери конеч- |
|||||||||||
тельному купированию воспаления. |
|||||||||||
ности при инфекции ниже пупарто- |
|||||||||||
Роль микроорганизмов в развитии |
|||||||||||
вой связки оценивается в 79 %. |
|
||||||||||
Наиболее употребимым термином |
инфекции |
после |
реконструктивных |
||||||||
для определения гнойных осложне- |
операций при использовании синте- |
||||||||||
ний после имплантации искусствен- |
тических материалов широко обсуж- |
||||||||||
ных материалов в русскоязычной ме- |
дается на страницах отечественных и |
||||||||||
дицинской литературе является "ин- |
зарубежных журналов. Многократ- |
||||||||||
фекция имплантата", а в англоязыч- |
ные исследования, направленные на |
||||||||||
ной — "implant infection" или "pro- |
изучение частоты выделения тех или |
||||||||||
sthetic infection". Это определение не |
иных |
патогенных |
микроорганизмов |
||||||||
может считаться активным, так как, |
при инфицировании трансплантатов, |
||||||||||
по сути, гнойный процесс развивает- |
показали, что наиболее частыми воз- |
||||||||||
ся не в протезе, а в окружающих тка- |
будителями являются низковирулен- |
||||||||||
нях и на поверхности имплантата. На |
тные штаммы золотистого и эпидер- |
||||||||||
сегодняшний день отсутствуют обос- |
мального стафилококка. |
|
|||||||||
нованное определение и клиническая |
По данным некоторых авторов, |
||||||||||
классификация |
этого |
патологи- |
частота высевания коагулазонегатив- |
||||||||
ческого процесса, что приводит, с |
ных стафилококков из артериальной |
||||||||||
одной стороны, к значительному |
стенки у больных, перенесших про- |
||||||||||
разбросу в оценке частоты гнойных |
тезирование, достигает 43 % при от- |
||||||||||
осложнений, а с другой — к субъек- |
сутствии каких-либо клинических |
||||||||||
тивному подходу в лечении больных. |
проявлений инфекции [Macbeth G.A., |
||||||||||
На наш взгляд, более логично бы- |
1984]. В то же время высеваемость |
||||||||||
ло бы использовать термин "па- |
микроорганизмов при наличии кли- |
||||||||||
рапротезная инфекция" (ППИ), по- |
нической картины хронической ин- |
||||||||||
нимая под ним патологическое состо- |
фекции составляет при использова- |
||||||||||
яние, обусловленное персистирова- |
нии стандартных методик лишь 60— |
||||||||||
нием микроорганизмов на поверхнос- |
70 %. Таким образом, создается па- |
||||||||||
ти ксеноматериала и проявляющееся |
радоксальная ситуация, когда нали- |
||||||||||
реакцией острого или хронического |
чие микроорганизмов не является ни |
||||||||||
воспаления окружающих тканей. |
|
необходимым, ни достаточным фак- |
|||||||||
Таким образом, в понятие ППИ не |
тором |
для |
развития |
клинической |
|||||||
включают случаи поверхностного на- |
картины нагноения, а клинические |
||||||||||
гноения |
послеоперационных |
ран, |
проявления |
воспаления |
могут быть |
||||||
случаи неинфекционного воспаления |
вызваны неинфекционными причи- |
||||||||||
(острое или хроническое гранулема- |
нами. |
|
|
|
|
||||||
тозное воспаление, иммунная реак- |
Ведущая роль стафилококков в раз- |
||||||||||
ция на ксеноматериал или продукты |
витии ППИ связана с их способнос- |
||||||||||
его деградации в тканях и т.п.), а так- |
тью продуцировать так |
называемый |
|||||||||
же случаи транзиторного инфициро- |
гликокаликс, или |
экстрацеллюляр- |
|||||||||
вания |
эндопротеза, когда микроор- |
||||||||||
ный матрикс. Адсорбированная к им- |
|||||||||||
ганизмы |
с поверхности |
имплантата |
|||||||||
плантату биопленка защищает микро- |
|||||||||||
высеваются без клинических и гис- |
организмы от воздействия иммунных |
|
тологических проявлений воспаления. |
||
факторов и антибиотиков и позволя- |
||
|
||
168 |
|
ет им в течение длительного времени |
ют лучшую резистентность к инфек- |
|||||||
персистировать на поверхности эн- |
ции, чем плетеные. По нашим дан- |
|||||||
допротеза. |
|
|
|
|
ным, частота бактериемии при на- |
|||
В патогенезе ППИ, помимо взаи- |
гноении вокруг протезов "Gore-tex" |
|||||||
модействия микроб — макроорга- |
составила 18,8 %, а при наличии пле- |
|||||||
низм, играют роль механизмы, связан- |
теных протезов ("Север", "Bard") — |
|||||||
ные с реакцией тканей на инородное |
29,2 % (р < 0,05). |
|
|
|||||
тело и особенности персистирования |
Кроме того, на состояние окружаю- |
|||||||
микроорганизмов на поверхности им- |
щих тканей влияет их постоянная |
|||||||
плантата. |
|
|
|
|
травматизация при пульсации протеза. |
|||
Внедрение инородного материала |
Ведущим путем первичного инфи- |
|||||||
в ткани вызывает реакцию неспеци- |
цирования протезов является интра- |
|||||||
фического |
гранулематозного воспа- |
операционное обсеменение во время |
||||||
ления, которая сопровождается ак- |
имплантации. |
Нарушение |
жестких |
|||||
тивной продукцией |
макрофагами и |
правил асептики приводит к попада- |
||||||
гигантскими клетками |
высокоток- |
нию микроорганизмов в рану с рук |
||||||
сичных перекисных |
соединений и |
хирургов, с пылевыми частицами из |
||||||
свободных радикалов. В неослож- |
воздуха операционной или в резуль- |
|||||||
ненных случаях этот процесс заканчи- |
тате нарушения стерильности проте- |
|||||||
вается формированием нежной, бед- |
за. Источниками инфекции могут |
|||||||
ной клеточными элементами капсулы. |
также служить кожа, лимфатические |
|||||||
В некоторых случаях выраженная |
узлы, патологически измененная ар- |
|||||||
"агрессивная" реакция гранулематоз- |
териальная стенка. Микроорганизмы |
|||||||
ного воспаления может служить са- |
могут попадать в зону сосудистой |
|||||||
мостоятельной |
причиной поздних |
реконструкции |
при |
сопутствующих |
||||
осложнений, симулирующих ППИ и |
условно стерильных вмешательствах, |
|||||||
известных |
как псевдоинфекция [De |
таких как аппендэктомия, холецист- |
||||||
Santis, Speziale F., 1992]. Механизм |
эктомия, резекция кишки. |
|
||||||
этих осложнений может быть также |
Кроме того, экспериментально до- |
|||||||
связан с иммунными реакциями на |
казана возможность |
гематогенного |
||||||
антигенные структуры протеза, ме- |
инфицирования |
и |
проникновения |
|||||
ханическими (пульсация) или хими- |
микробов из мочеполового тракта или |
|||||||
ческими факторами. Диагноз псев- |
кишечника per |
diapedesum |
[Bandyk, |
|||||
доинфекции основывается на отри- |
1994], однако клиническое значение |
|||||||
цательных |
результатах |
повторных |
этих путей определить трудно. |
|||||
бактериологических исследований и |
Вторичное инфицирование проте- |
|||||||
на характерной |
цитологической |
за происходит на фоне таких после- |
||||||
картине хронической перипротезной |
операционных осложнений, как по- |
|||||||
воспалительной реакции в виде гига- |
верхностное нагноение раны, краевой |
|||||||
нтских многоядерных клеток ино- |
некроз кожи, парапротезная гемато- |
|||||||
родных тел, макрофагов, лимфоци- |
ма, скопление серозной жидкости |
|||||||
тов и плазматических клеток. |
или лимфорея. Именно поэтому мы |
|||||||
На фоне дистрофических измене- |
выделяем первичную и вторичную па- |
|||||||
ний в тканях вокруг имплантата фак- |
рапротезную инфекцию. При пер- |
|||||||
торы антимикробной защиты оказы- |
вичной инфекции процесс начинает- |
|||||||
ваются неэффективными, что при- |
ся на поверхности протеза и прохо- |
|||||||
водит к нарушению фагоцитоза и |
дит по описанному выше механизму |
|||||||
развитию феномена "дремлющей ин- |
(рис. 6.68). |
|
|
|
||||
фекции". |
|
|
|
|
Вторичное инфицирование объ- |
|||
Значительную |
роль в |
патогенезе |
единяет все случаи распространения |
|||||
ППИ играют структура и поверхность |
воспалительного процесса с окружа- |
|||||||
имплантата. Известно, что протезы из |
ющих тканей на протез. В этих слу- |
|||||||
политетрафторэтилена демонстриру- |
чаях целесообразно указывать в диа- |
|||||||
|
|
|
|
|
|
|
|
169 |
