
Андреева, СД методы исследования печени
.pdf
21
Они неподвижны, имеют неправильную форму с отростками, располагаются в пространстве Диссе, обычно между двумя смежными гепатоцитами (рис.16). В цитоплазме находятся крупные липидные включения, содержащие витамин А. В них аккумулируется до 75% всех ретиноидов организма.
Клетки имеют хорошо выраженный цитоскелет, развитую гранулярную эндоплазматическую сеть (ЭПС), мелкие митохондрии и пероксисомы. В условиях патологии клетки Ито теряют липидные включения и начинают синтезировать коллагеновые волокна, гликозаминогликаны и протеогликаны, что приводит к фиброзу печени.
Активированные клетки Ито интенсивно продуцируют следующие биологически активные вещества: инсулиноподобный фактор роста 1, трансформированные факторы роста, интерлейкин-6, колониестимулирующий фактор макрофагов, хемо-аттрактанты моноцитов, фактор роста гепатоцитов и др.
1.3.5 Pit-клетки. Pit-клетки расположены в стенке синусоида (рис. 19-21) и не способны к активным движениям. В цитоплазме Pit-клеток имеются немногочисленные гранулы с плотной сердцевиной и светлым ободком, содержащие серотонин и др. вещества (рис.17-19). На плазмолемме Pit-клеток экспрессируются антигены CD8, CD56. Эти клетки проявляют высокую цитотоксическую активность, направленную против опухолевых клеток и инфицированных вирусами гепатоцитов.
Э
1
2
3
Рисунок 17 - Печень свиньи: 1 – гепатоцит; 2 – Pit-клетка; 3 – секреторные гранулы (препарат Андреевой С.Д.). Ув. х 4000

22
Эффект Pit-клеток отличается от активности клеток Купфера, которые проявляют цитолитическую активность только после специфических стимулов, таких как липополисахариды. Цитотоксическая активность Pit-клеток является спонтанной. Они активно продуцируют интер- лейкины-1, 2, 3, -интерферон, фактор некроза опухолей. Pit-клетки проявляют высокую чувствительность к интерлейкину-2, при введении которого происходит многократное увеличение количества этих клеток.
Рисунок 18 - Сканирующая электроно- |
Рисунок 19 - Электронограмма Pit-клетки |
грамма Pit-клетки (Л) в контакте с клеткой |
(Л). Цитоплазма содержит характерные гра- |
Купфера (К) в просвете синусоида (С). |
нулы (стрелки). К - клетка Купфера. |
Ув. х 5500 (по Зайцеву В.Б.) |
Ув. х 4000 (по Зайцеву В.Б.) |
1.4 Анатомо-гистологическое строение желчевыводящих путей
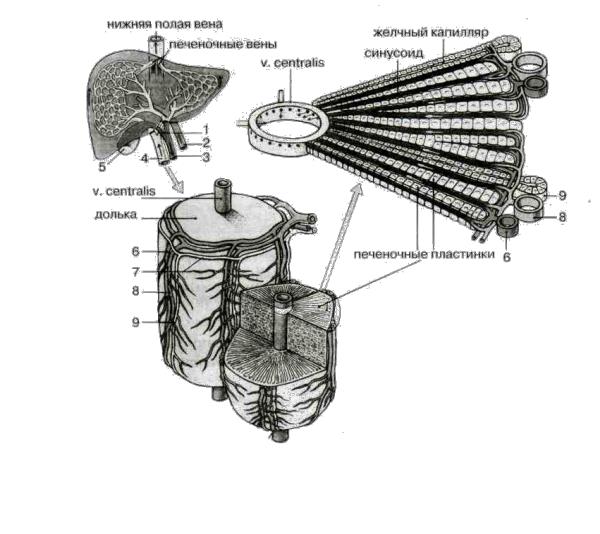
Желчь вырабатывается гепатоцитами и проходит через сложную систему желчных ходов, расположенных внутри и вне печени. Эта система включает в себя желчные капилляры, терминальные желчные канальцы Геринга, холангиолы, междольковые желчные протоки, входящие в состав триад, долевые желчные протоки, общий печеночный проток – ductus hepaticus communis, который, сливаясь с пузырным протоком, формирует общий желчный проток – ductus choledochus (рис. 20).
Внутрипеченочные желчные пути. Желчные капилляры образуются билиарными полюсами двух и более смежных гепатоцитов, соединенных между собой специальными плотными контактами, и, следовательно, не имеют собственной стенки. Желчные капилляры, сливаясь друг с другом
23
на периферии дольки, образуют терминальные канальцы Геринга, имеющие базальную мембрану. Стенка канальцев представлена билиарным эпителием, среди клеток которого встречаются гепатоциты. Из терминальных желчных канальцев Геринга желчь поступает в холангиолы, выстланные кубическим эпителием. Далее желчь поступает в междольковые желчные протоки, лежащие в портальных трактах. Эти протоки выстланы однослойным кубическим эпителием, который замещается в дистальных отделах на однослойный цилиндрический эпителий.
Внепеченочные желчные пути представлены правым и левым печеночным протоками, сливающимися в общий печеночный проток. Дистальнее в него впадает проток желчного пузыря.
Внепеченочные желчные пути имеют сходный план строения. Стенка представлена следующими оболочками:
1.Слизистая оболочка, выстлана однослойным призматическим эпителием и имеет собственную пластинку слизистой, содержащую мелкие слизистые железы.
2.Мышечная оболочка представлена косым и циркулярным слоями гладкомышечных клеток.
3.Адвентициальная оболочка, состоящая из рыхлой волок нистой неоформленной соединительной ткани.
Рисунок 20 - Схема кровоснабжения и желчеоттока печени: 1 - пузырный проток; 2
– печёночная артерия; 3 – общий желчный проток; 4 – портальная вена; 5 – желчный пузырь; 6 – междольковая артерия; 7 – вокругдольковая артерия; 8 – междольковая вена; 9 – междольковый желчный проток (по R. Corola)

24
1.5 Гистологическое строение стенки желчного пузыря
Желчный пузырь (vesica fellea) - полый орган, накапливающий и концентрирующий желчь.
1) Стенка желчного пузыря образована тремя оболочками : слизистой, волокнисто-мышечной, серозной (рис. 21).
Слизистая включает в себя:
•однослойный призматический каемчатый эпителий;
•собственную пластинку слизистой, представленную рыхлой волокнистой неоформленной соединительной тканью.
Эпителий слизистой обеспечивает реабсорбцию воды из желчи, что
|
|
|
|
|
приводит к концентрации |
|||||
1 |
|
|
|
|
желчи. |
Волокнисто-мыше- |
||||
2 |
|
|
|
|||||||
|
|
|
|
чная оболочка |
образована |
|||||
|
|
|
|
|
||||||
|
|
|
|
|
пучками |
гладкомышечных |
||||
|
|
3 |
|
|||||||
|
|
клеток |
и |
соединительнот- |
||||||
|
|
|
|
|
||||||
|
|
|
|
|
канными прослойками. Хо- |
|||||
|
|
|
|
|
||||||
|
|
|
|
|
лецистокинин-панкреозимин |
|||||
|
|
|
|
|
и мотилин, |
вырабатываемые |
||||
|
|
|
|
|
эндокриноцитами слизистой |
|||||
|
|
|
|
|
оболочки |
желудочно-ки- |
||||
|
|
|
|
|
шечного тракта, стимули- |
|||||
|
|
|
|
|
руют |
сокращение |
гладко- |
|||
|
|
|
|
|
мышечных |
клеток |
стенки |
|||
4 |
|
|
|
|
желчного пузыря, а сомато- |
|||||
|
|
|
|
статин угнетает. |
|
|
||||
|
|
|
|
|
|
|
||||
|
|
|
|
|
Серозная |
оболочка |
||||
|
|
|
|
|
покрывает только нижнюю |
|||||
|
|
|
|
|
поверхность желчного пу- |
|||||
|
|
|
|
|
зыря и представлена мезо- |
|||||
Рисунок 21 – Гистологическая картина стенки желчного |
||||||||||
телием и подлежащей рых- |
||||||||||
пузыря: 1 – складки слизистой оболочки; 2 – каёмчатый |
||||||||||
эпителий; 3 – собственная пластинка слизистой оболочки; |
лой |
|
волокнистой |
|||||||
4 – гладкая мускулатура. Ув. х100 (по Синельникову В.А) |
неоформленной |
соедини- |
||||||||
|
|
|
|
|
||||||
тельной тканью. Нарушение оттока желчи, а также воспалительные заболевания жел-
чевыводящих путей могут приводить к образованию камней в просвете желчного пузыря или (и) желчевыводящих путей. Приблизительно 80% камней содержат в больших концентрациях холестерол (холестериновые камни), реже встречаются камни, содержащие большие объемы солей желчных кислот (пигментные камни). Холестериновые камни, как правило, крупные (1-3 см), имеют бледно-желтый цвет, единичны. Пигментные камни мельче (1 см), темной окраски, встречаются чаще, чем холестериновые.
25
1.6 Регенерация печени
Печень обладает мощным регенераторным потенциалом. Возможно полное восстановление печени после резекции 70% органа, либо гибели такого же объема печеночной ткани при гепатите. Восстановление исходной массы и функции происходит менее чем через месяц. По уровню обновления гепатоциты относятся к растущей клеточной популяции. В покоящейся печени гепатоциты находятся в Go периоде (митоза), но при стимуляции (например, резекции) вновь вступают в клеточный цикл, чтобы восполнить свою нормальную численность. Уже на вторые сутки после оперативного удаления ткани печени митотическая активность гепатоцитов увеличивается в десятки раз. Наряду с клеточной регенерацией осуществляется и внутриклеточная регенерация, проявляющаяся увеличением количества и размеров митохондрий, элементов гладкой и гранулярной ЭПС. В гепатоцитах в ходе восстановления сначала повышается содержание жиров, затем белков и, наконец, сложных белково-углево-дородных комплексов. Регенерация органа происходит за счет гиперпластических процессов, бурно протекающих во всей оставшейся после резекции части печени. Происходит так называемая регенерационная гипертрофия в результате деления и гипертрофии клеток печени. Удаленная часть органа никогда не восстанавливается в первозданном виде и не происходит её отделения от раневой поверхности. Установлено, что процесс регенерации печени нуждается в интенсивном кровоснабжении (уменьшение количества протекающей крови его замедляет), адекватном желчевыделении (препятствие оттоку желчи вызывает повреждение функциональных структур органа), поступлении белков, витаминов (особенно В]2 - для синтеза нуклеиновых кислот), гормонов (например, удаление надпочечников подавляет регенераторную активность гепатоцитов). В последние годы обнаружено влияние на регенерацию печени простагландинов (способствуют аккумуляции энергии в клетках), кейлонов (подавляют митотическую активность), специфических факторов роста (фактор роста гепатоцитов).
2. ОСНОВНЫЕ ФУНКЦИИ ПЕЧЕНИ
Невозможно найти такое звено обмена веществ в организме, которое так или иначе не было бы связано с процессами, протекающими в печени. Важнейшее значение печени в обмене веществ во многом определяется её связующей ролью между портальным и общим кругом кровообращения. Большая часть веществ, абсорбирующихся в кишечнике, проходит через печень.
Одной из многочисленных функций печени является первичная регуляция содержания в крови веществ, поступающих в организм с пищей. Несмотря на то, что всасывание питательных веществ из кишечника в кровь происходит прерывисто, непостоянно (и потому в портальном круге кро-
26
вообращения могут наблюдаться изменения концентрации ряда веществ: глюкозы, аминокислот и др.). В общем же круге кровообращения изменения
вконцентрации указанных соединений незначительны благодаря важной роли печени в поддержании постоянства внутренней среды организма.
Многообразие функций печени находит отражение в обилии лабораторных исследований, предложенных для оценки функционального состояния этого органа. Необходимо подчеркнуть, что ни в одном органе разграничение нормы и патологии не представляет таких трудностей, с какими приходится сталкиваться при исследовании функции печени. Следует иметь
ввиду очень большую регенерирующую способность печени, позволяющую ей длительное время компенсировать патологический процесс. Не всегда при том или ином патологическом процессе изменены все функции печени, нарушение может касаться лишь одной или некоторых из них.
Около половины сухого остатка ткани печени приходится на белки, причем из них большую часть составляют глобулины. Остальные белки представлены альбуминами, нуклеопротеидами и коллагеном. Из белков, специфических для печени, а также для селезенки и костного мозга следует отметить хромопротеид - ферритин, содержащий железо.
Наряду с ферментами, имеющимися и в других органах, печень содержит ферменты, присущие только ей. К их числу, в частности, относятся ферменты, вызывающие распад цистеина и гистидина, а также катализирующие синтез мочевины, метилирование гуанидинуксусной кислоты, отщепление фосфорной кислоты от глюкозо-6-фосфата, образование эфиров глюкуроновой кислоты. Повышенная активность некоторых ферментов в крови новорожденных может быть обусловлена повышенной проницаемостью клеточных мембран, и по мере снижения проницаемости активность таких ферментов приближается к нормативам взрослых животных. В частности, это установлено для аспартатаминотрансферазы (АСТ) и фруктозодифосфатальдолазы.
2.1 Функция кроветворения и регулирования объёма циркулирующей крови
Вэмбриональный период печень является основным органом крове-
творения. В постэмбриональный период витамин В12 , образующийся в печени, регулирует эритропоэз; печень синтезирует белки крови и участвует в синтезе гемоглобина.
Вразвитии крови как ткани в эмбриональный период можно выделить 3 основных этапа, последовательно сменяющих друг друга – мезобластический, гепатолиенальный и медуллярный (рис.22).
Первый, мезобластический, этап – это появление клеток крови во внезародышевых органах, а именно в мезенхиме стенки желточного мешка, мезенхиме хориона и стебля. При этом появляется первая генерация стволовых
27
клеток крови (СКК). Мезобластический этап протекает с 3-й по 9-ю неделю развития зародыша у крупного рогатого скота. В мезенхиме стенки желточного мешка обособляются зачатки сосудистой крови, или кровяные островки. В них мезенхимные клетки округляются, теряют отростки и преобразуются в стволовые клетки крови. Клетки, ограничивающие кровяные островки, уплощаются, соединяются между собой и образуют эндотелиальную выстилку будущего сосуда. Часть стволовых клеток дифференцируется в первичные клетки крови (бласты). Большинство первичных кровяных клеток митотически делится и превращается в первичные эритробласты, характеризующиеся крупным размером – мегалобласты. Это превращение совершается в связи с накоплением эмбрионального гемоглобина (HbF) в цитоплазме бластов. В некоторых первичных эритробластах ядро подвергается кариорексису и удаляется из клеток, в других ядро сохраняется. В результате образуются безъядерные и ядросодержащие первичные эритроциты, отличающиеся большим размером по сравнению с нормоцитами и поэтому получившие название мегалоцитов. Такой тип кроветворения называется мегалобластическим. Он характерен для эмбрионального периода, но может появляться в постнатальном периоде при некоторых заболеваниях.
Наряду с мегалобластическим в стенке желточного мешка начинается нормобластическое кроветворение, при котором из бластов образуются вторичные эритробласты, из которых образуются вторичные эритроциты (нормоциты).
Развитие эритроцитов в стенке желточного мешка происходит внутри первичных кровеносных сосудов, т.е. интраваскулярно. Одновременно экстраваскулярно из бластов, расположенных вокруг сосудистых стенок, дифференцируется небольшое количество гранулоцитов — нейтрофилов и эозинофилов.
Часть стволовых клеток крови остается в недифференцированном состоянии и разносится током крови по различным органам зародыша, где происходит их дальнейшая дифференцировка в клетки крови или соединительной ткани. После редукции желточного мешка основным кроветворным органом временно становится печень.
Второй, гепатолиенальный, этап начинается примерно с 5-6-й недели развития плода крупного рогатого скота, когда печень становится основным органом гемопоэза, в ней образуется вторая генерация стволовых клеток крови. Кроветворение в печени достигает максимума к пятому месяцу внутриутробного развития и завершается перед рождением. Стволовые клетки крови из печени перемещаются в тимус, селезенку и лимфатические узлы. Печень у крупного рогатого скота закладывается примерно на 3-4-й неделе эмбриональной жизни, а с 5-й недели она становится центром кроветворения. Кроветворение в печени происходит экстраваскулярно, по ходу капилляров, врастающих вместе с мезенхимой внутрь печеночных долек. Источ-
28
ником кроветворения в печени являются стволовые клетки крови, из которых образуются бласты, дифференцирующиеся во вторичные эритроциты.
Одновременно с развитием эритроцитов в печени образуются зернистые лейкоциты, главным образом нейтрофильные и эозинофильные. Кроме гранулоцитов в печени формируются гигантские клетки - мегакариоциты, предшественники тромбоцитов. К концу внутриутробного периода кроветворение в печени прекращается.
Тимус закладывается в конце 1-го месяца внутриутробного развития, и на 7-8-й неделе его эпителий начинает заселяться стволовыми клетками крови, которые дифференцируются в лимфоциты тимуса. Увеличивающееся число лимфоцитов тимуса дает начало T-лимфоцитам, заселяющим T-зоны периферических органов иммунопоэза. Закладка селезенки у крупного рогатого скота также происходит в конце 1-го месяца эмбриогенеза. Из вселяющихся сюда стволовых клеток происходит экстраваскулярное образование всех видов форменных элементов крови, т.е. селезенка в эмбриональном периоде представляет собой универсальный кроветворный орган. Образование эритроцитов и гранулоцитов в селезенке достигает максимума на 5-м месяце эмбриогенеза. После этого в ней начинает преобладать лимфоцитопоэз.
Первые закладки лимфоузлов появляются на 7-8-й неделе эмбрионального развития. Большинство лимфатических узлов развивается на 9-10-й неделе. В этот же период начинается проникновение в лимфатические узлы стволовых клеток крови, из которых на ранних стадиях дифференцируются эритроциты, гранулоциты и мегакариоциты. Однако формирование этих элементов быстро подавляется образованием лимфоцитов, составляющих основную часть лимфатических узлов.
Появление единичных лимфоцитов происходит уже в течение 8-15-й недели развития, однако массовое «заселение» лимфатических узлов предшественниками T- и B-лимфоцитов начинается с 16-й недели, когда формируются посткапиллярные венулы, через стенку которых осуществляется процесс миграции клеток. Из клеток-предшественников дифференцируются сначала лимфобласты (или большие лимфоциты), а далее средние и малые лимфоциты. Дифференцировка T- и B-лимфоцитов происходит, соответственно, в T- и B-зависимых зонах лимфатических узлов.
Третий, медуллярный (костномозговой), этап - это появление третьей генерации стволовых клеток крови в красном костном мозге, где гемопоэз начинается с 10-й недели и постепенно нарастает к моменту рождения. После рождения костный мозг становится центральным органом гемопоэза. Закладка костного мозга осуществляется на 2-м месяце эмбрионального развития крупного рогатого скота. Первые гемопоэтические элементы появляются на 12-й неделе развития; в это время основную массу их составляют эритробласты и предшественники гранулоцитов. Из стволовых клеток крови в костном мозге формируются все форменные элементы крови, развитие ко-

29
торых происходит экстраваскулярно. Часть СКК сохраняется в костном мозге в недифференцированном состоянии. Они могут расселяться по другим органам и тканям и являться источником развития клеток крови и соединительной ткани. Таким образом, костный мозг становится центральным органом, осуществляющим универсальный гемопоэз, и остается им в течение постнатальной жизни. Он обеспечивает стволовыми кроветворными клетками тимус и другие гемопоэтические органы.
В процессе развития происходят также изменения и в самой молекуле гемоглобина. Молекула гемоглобина (молекулярная масса 64 500) состоит из четырех полипептидных цепей, связанных с молекулой гема. На разных стадиях онтогенеза и в двух различных популяциях эритроцитов строение некоторых полипептидных цепей гемоглобина изменяется, что отражает активность разных генов в процессе развития. Независимо от типа и периода синтеза большинство молекул гемоглобина имеют две одинаковые полипептидные цепи ( -цепи). Две другие цепи могут отличаться и определяют тем самым тип молекулы гемоглобина (рис. 24). Первоначальный тип гемоглобина, образующийся в процессе эритропоэза в желточном мешке, - это эмбриональный гемоглобин, в молекуле которого соединены две α- и две ε- цепи. Эмбриональный гемоглобин присутствует только в течение первых 2 месяцев и затем замещается фетальным гемоглобином (гемоглобином плода, F-Hb), содержащим две α- и две γ-цепи и доминирующим на протяжении остальной эмбриональной жизни. И наконец, вскоре после рождения начинает преобладать гемоглобин дефинитивного типа. Большинство типов дефинитивного гемоглобина содержит, помимо двух α-цепей, две β- или две δ- цепи.
Рисунок 22 - Стадии эритропоэза у человека и крупного рогатого скота. Синусоидами обозначены пики активности гемопоэза в онтогенезе
Эмбриональный и фетальный гемоглобины имеют более высокое
30
сродство к кислороду, чем гемоглобин взрослого организма. Это свойство является важной адаптацией к внутриутробной жизни, поскольку фетальный гемоглобин способен более эффективно, чем дефинитивный, связывать кислород, диффундирующий через плацентарный барьер. В течение плодного периода все более возрастает синтез гемоглобина взрослого типа. После рождения содержание фетального гемоглобина быстро уменьшается и через 4-6 месяцев его уже не удается обнаружить в крови.
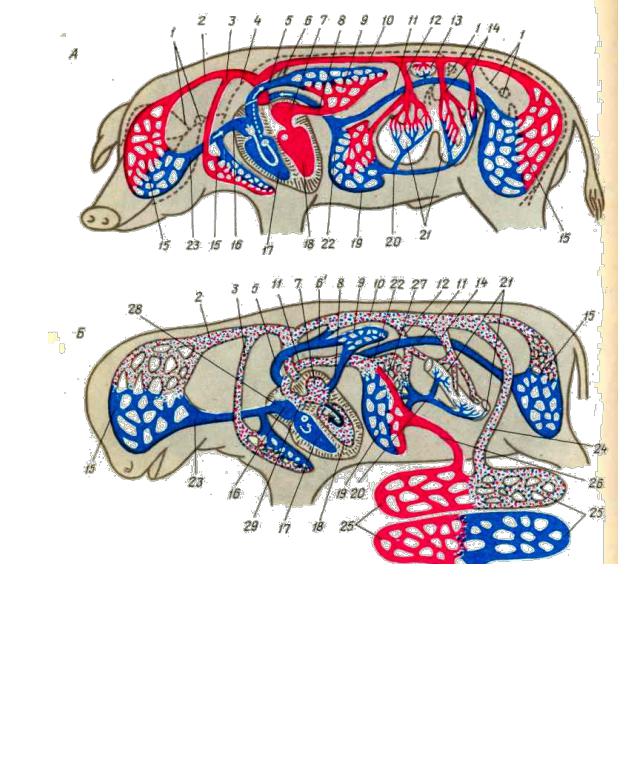
Кровообращение плода также отличается от кровообращения взрослого организма (рис. 23).
Рисунок 23 - Схема кругов кровообращения у взрослых свиней (А) и плода (Б): 1 - лимфатические узлы и сосуды; 2 – общая сонная артерия; 3 – подмышечная артерия; 4 – грудной проток; 5- легочная артерия; 6-связка; 6 / - артериальный проток; 7- левое предсердие; 8-легочная вена; 9 – капилляры легких; 10 - аорта; 11 - каудальная полая вена; 12 - чревная артерия; 13 – артерии и вены почек; 14 – брыжеечные артерии; 15 – капилляры тела, проток; 16 - правое предсердие; 17 – правый и 18 – левый желудочек сердца; 19 – капилляры печени; 20 – воротная вена печени; 21 – желудок и кишечник; 22 – печеночная вена; 23 – краниальная полая вена; 24 – пупочная артерия; 25 – капилляры плаценты и матки; 26 – пупочная артерия; 27 - венозный проток; 28 – межвенозный бугорок; 29 – овальное отверстие; 30 – артерии и вены матки (по Сысоеву А.А.)
