
электив-пособие
.pdf
HO OH
N
CONH2
транс-10,11-дигидрокси- карбамазепин
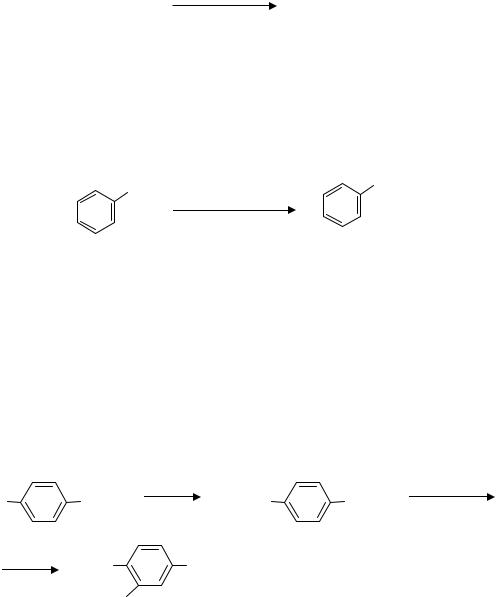
Гидроксилирование ароматических соединений
Ароматические углеводороды гидроксилируются ферментами микросом печени с выделением фенолов. Гидроксилирование может протекать посредством двух ферментных механизмов: 1) гидроксилирование свободным радикалом или через образование эпоксида с последующей внутримолекулярной перегруппировкой его в фенол; 2) образование 1,2-дигидроарен-1,2- диолов или 1,2-дигидроаренмоноолов, общим предше- ственником которых, вероятно,является эпоксид.
1) |
OH |
микросом. арилгидроксилаза |
|
|
НАДФН2 + O2 |
бензол |
фенол |
2) |
O |
|
|
|
микросом. ферменты |
|
НАДФН2 + O2 |
нафталин |
эпоксид |
OH
|
|
H2O |
1-нафтол |
-H2O |
OH |
|
|
OH |
OH |
-2H |
|
OH |
|
|
|
|
1,2-дигидронафталин- |
|
1,2-диол |
|
1,2-нафтадиол |
|
|
21

Если в молекуле имеется несколько ароматических колец, гидроксилированию, как правило, подвергается одно из них. Например:
|
HN |
микросом. |
HN |
|
|
|
|
ферменты |
|
|
|
O |
O |
|
O |
O |
OH |
|
|
||||
|
NH |
|
NH |
|
|
|
фенитоин |
|
п-гидроксифенитоин |
||
Ориентация |
гидроксилирования |
|
монозамещённых |
||
бензолов определяется, главным образом, природой
заместителя. |
Соединения, |
|
содержащие |
||
электронодонорные |
заместители, |
гидроксилируются |
|||
легко, |
преимущественно |
в |
|
пара-положение. |
|
Гидроксилирование |
ароматических |
соединений, |
|||
содержащих |
электроноакцепторные |
заместители, |
|||
протекает |
труднее |
(в мета- |
и |
пара-положения). В |
|
ряде случаев гидроксилирование вообще невозможно из-за электроноакцепторного влияния заместителей.
Если в соединении есть два ароматических кольца, то реакция гидроксилирования протекает по кольцу, где выше электронная плотность. Например,
гидроксилирование |
диазепама |
|
преимущественно |
|||
протекает |
|
по |
кольцу, |
не |
|
содержащему |
электроноакцепторного заместителя: |
|
|
||||
|
CH |
3 |
|
|
CH3 |
|
|
|
|
|
|
O |
|
|
N |
O |
|
|
N |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
гидроксилирование |
|
|
|
|
Cl |
|
N |
Cl |
|
N |
|
|
|
|
|
|
||
диазепам |
OH |
|
|
|
4'-гидроксидиазепам |
Полициклические ароматические углеводороды подвергаются эпоксидированию с последующим образованием транс-диолов. Например, таким образом
22

метаболизируется бенз[a]пирен – потенциально канцерогенное соединение, попадающее в организм из окружающей среды:
|
микросомальное |
|
окисление |
7 |
|
8 |
O |
бенз[a]пирен |
7,8-эпоксид |
HO
OH
7,8-трансдиол
Основным продуктом метаболизма является 7,8- диол, хотя могут образоваться и 4,5-эпоксид; 7,8- эпоксид; 9,10-эпоксид. Они проявляют мутагенные свойства.
Окислительное дезалкилирование
Большое число ксенобиотиков метаболизируется в организме путём удаления N-, O-, S-алкильных групп с образованием соответствующих аминов, фенолов или тиолов. Ферментные системы, катализирующие дезалкилирование, локализованы в микросомах печени. Для их работы необходимы НАДФН2 и кислород.
N-Дезалкилирование
Дезалкилирование вторичных и третичных аминов с образованием первичных и вторичных аминов - это
одна |
из |
важнейших |
реакций |
в |
метаболизме |
|||
лекарственных веществ. |
|
|
|
|
|
|||
Обычно третичные амины дезалкилируются до |
||||||||
вторичных быстрее, чем вторичные до первичных. |
|
|||||||
Механизм |
N-дезалкилирования |
заключается |
в |
|||||
ферментативном |
образовании |
N-оксида |
или |
|||||
неустойчивого |
гидроксиалкильного |
|
промежуточного |
|||||
продукта |
карбиноламина, |
который |
претерпевает |
|||||
ферментативную |
|
или |
|
самопроизвольную |
||||
23

перегруппировку и распадается на амин и оксосоединение:
α |
O2 |
|
|
N-CH2-R |
-OH- |
N-CH-R |
N-H + R-CHO |
|
|
| |
|
третичный |
|
OH |
вторичный альдегид |
амин |
|
карбиноламин |
амин |
Например, одним из путей метаболизма никотина является окислительное деметилирование:
N |
окислительное |
N |
|
||
|
|
+ HCHO |
CH3 деметилирование |
H |
|
N |
|
N |
никотин |
|
норникотин |
Наиболее изучены процессы N-дезалкилирования наркотических веществ и анальгетиков. Установлено, что морфин, героин, кодеин подвергаются в организме N-дезалкилированию с образованием соответствующих норпроизводных и альдегида:
HO |
HO |
|
O |
|
N-CH3 |
НАДФН, O2 |
|
O |
|
|
|
|
||
|
|
|
|
N-CH2OH |
|
|
|
|
|
|
|
HO |
|
|
|
|
HO |
|
морфин |
|
|
|
|
|
|
|
|
производное |
|
|
|
|
|
|
|
|
|
|
|
|
карбиноламина |
|
|
|
HO |
|
|
|
|
|
O |
NH |
|
|
|
|
|
+ HCHO |
|
|
|
|
|
|
HO
норморфин
Несмотря на то, что микросомальная монооксигеназная система возникла в ходе эволюции для детоксикации чужеродных соединений, в процессе N-дезалкилирования образуются соединения с
24

повышенной токсичностью по сравнению с исходным субстратом. Например, норкодеин в шесть раз
токсичнее кодеина. |
|
|
|
|
||
В |
некоторых |
случаях |
окислительное |
N- |
||
дезалкилирование |
вызывает активацию лекарственных |
|||||
соединений. |
Так |
при |
|
деметилировании |
||
антидепрессанта |
|
имипрамина |
образуется |
|||
дезметилимипрамин (дезипрамин), который также обладает фармакологической активностью. Он даёт лучшие результаты при применении, так как не
оказывает |
побочных |
эффектов, |
свойственных |
||||||||||||||||||
имипрамину. |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
НАДФН2,O2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
-HCHO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
N |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
CH2CH2CH2N(CH3)2 |
|
|
|
|
|
CH2CH2CH2NHCH3 |
|||||||||||
|
|
|
имипрамин |
|
|
|
|
|
|
дезипрамин |
|
||||||||||
Только небольшая часть дезипрамина подвергается дальнейшему деметилированию.
Среди метаболитов амидопирина обнаружены и монометиламиноантипирин, и аминоантипирин, то есть деметилирование протекает в две стадии:
CH3 |
|
|
|
|
|
|
|
|
|
|
N |
|
CH3 |
CH3NH |
|
|
CH3 |
H2N |
|
|
CH3 |
CH3 |
|
-HCHO |
|
|
|
-HCHO |
|
|
|
|
|
|
N |
|
|
|
N |
|
|
|
N |
O |
|
CH3 |
O |
|
|
CH3 |
O |
|
|
CH3 |
|
N |
|
N |
|
N |
|||||
|
|
C6H5 |
|
|
|
C6H5 |
|
|
|
C6H5 |
|
|
|
|
|
|
|||||
амидопирин |
монометилантипирин |
аминоантипирин |
||||||||
O-Дезалкилирование
Механизм O-дезалкилирования простых эфиров
сходен с механизмом N-дезалкилирования |
аминов. |
||||
Сначала |
идёт |
гидроксилирование |
по |
α-атому |
|
углерода, |
а |
затем |
расщепление |
полученного |
|
полуацеталя с |
образованием гидроксипроизводного |
||||
(спирта или фенола) и соответствующего альдегида:
25

|
НАДФН2,O2 |
|
Ar-O-CH2R |
микросом.ферм. Ar-O-CH-R |
Ar-OH + R-CHO |
простой |
| |
фенол |
эфир |
OH |
|
|
полуацеталь |
|
|
|
O-Деалкилирование |
|
фенацетина |
приводит |
к |
||||||||
образованию N-ацетил-п-аминофенола: |
|
|
||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
OC2H5 |
|
|
|
O-CH-CH3 |
|
|
OH |
|
|
|||
|
|
|
микросом.ферм. |
|
|
|
|
|
|
|
|
+ CH3CHO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
NHCOCH3 |
|
|
|
NHCOCH3 |
|
|
NHCOCH3 |
|
||||
|
|
фенацетин |
полуацеталь |
N-ацетил- |
|
|
||||||||
|
|
|
|
|
|
|
|
|
п-аминофенол |
|
||||
|
|
Установлено, что N-ацетил-п-аминофенол также |
||||||||||||
обладает |
анальгезирующим |
и |
жаропонижающим |
|||||||||||
эффектом. Это дало основание использовать его в
качестве самостоятельного |
лекарственного средства |
||||||||||||||||
(парацетамол). |
|
|
|
|
|
|
|
|
|
|
|||||||
За счёт O-дезалкилирования кодеин превращается |
|||||||||||||||||
в организме в морфин: |
|
|
|
|
|
|
|
|
|
|
|||||||
H3CO |
|
HO |
|||||||||||||||
|
|
|
|
|
|
|
O-дезалкилирование |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
O |
|
|
|
|
|
|
|
O |
|
|
N-CH3 |
||||||
|
|
|
N-CH3 |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
HO |
|||||||||||||||
|
кодеин |
|
|
|
|
морфин |
|||||||||||
S-Дезалкилирование
S-Дезалкилирование тиоэфиров под действием микросомальных монооксигеназ приводит к образованию тиолов и соответствующих альдегидов. Реакция требует наличия НАДФН2 и кислорода.
НАДФН2,O2 |
|
|
R-S-CH2-R’ |
R-SH + R’-CHO |
|
микросом.ферм. |
тиол |
альдегид |
26

Таким образом метаболизируются, например, метилмеркаптан, 6-метилтиопурин, S- метилцистеин, S-метилбарбитурат (метилтиурал).
Диметилсульфид |
и метионин не дезалкилируются в |
||
этой микросомальной системе. |
|
||
Деметилирование 6-метилтиопурина приводит к |
|||
образованию |
6-меркаптопурина, |
используемого |
|
самостоятельно |
при |
лечении |
злокачественных |
опухолей: |
|
|
|
S-CH3 |
S-CH2OH |
SH |
|
||
N |
N |
N |
N |
N |
N |
|
|
НАДФН2,O2 |
|
|
|
N |
NH |
N |
NH |
N |
NH |
6-метилтиопурин |
|
|
6-меркаптопурин |
||
Окислительное дезаминирование
Первичные амины метаболизируются путём окислительного дезаминирования под действием аминооксидазы в присутствии НАДФН2 и кислорода, образуя соответствующий кетон и аммиак. Реакция протекает через образование промежуточного имина:
|
|
|
НАДФН2,O2 |
|
|
|
|
-H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
R-CH2-NH2 |
|
R-CH-NH2 |
|
R-CH=NH |
R-CHO + NH3 |
||||||||||
первичный |
|
| |
|
|
имин |
альдегид |
|||||||||
амин |
|
|
OH |
|
|
|
|
|
|
|
|
|
|||
|
Дезаминирование приводит к полной потере |
||||||||||||||
биологической |
|
|
активности ксенобиотиков, в том |
||||||||||||
числе лекарственных препаратов. |
|
|
|
||||||||||||
|
Примером |
окислительного дезаминирования служит |
|||||||||||||
метаболизм |
амфетамина: |
|
|
|
|
|
|
|
|||||||
|
|
|
CH2-CH-CH3 окислит. |
|
|
|
|
CH2-C-CH3 |
|||||||
|
|
|
| |
|
|
дезаминирование |
|
|
|
|
|
|
+ NH3 |
||
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
O |
||
|
|
амфетамин |
|
|
|
|
|
|
|
фенилацетон |
|||||
27
N-Окисление аминов
Первичные и вторичные амины могут подвергаться также N-окислению. Продуктами окисления являются соответствующие N-гидроксиламины:
|
N-окисление |
R-NH-CH3 |
R-N-CH3 |
вторичный |
| |
амин |
OH |
|
гидроксиламин |
Например, продуктом N-окисления анилина являет- ся фенилгидроксиламин:
NH2 |
NHOH |
|
N-окисление |
анилин |
фенилгидроксиламин |
Гидроксиамины более токсичны, чем исходные амины. Гидроксиламины могут изомеризоваться в о- аминофенолы. Предполагают, что гидроксиламины являются промежуточными продуктами орто- гидроксилирования. Например, метаболизм сульфаниламидов включает стадию N-окисления и изомеризацию полученного гидроксиламина в орто- производное:
H2N |
SO2NHR |
HO-NH |
SO2NHR |
|
сульфаниламид |
замещённый фенилгидроксиламин |
|
|
H2N |
SO2NHR |
|
HO
о-оксисульфаниламид
Таким образом, амины метаболизируются за счёт N-дезалкилирования, окислительного дезаминирования и N-окисления.
Десульфирование
В результате десульфирования происходит замещение серы на кислород. Реакция протекает с
28

участием |
|
|
микросомальных |
ферментов. |
Например, |
|||||
десульфирование |
тиобарбитала |
|
|
приводит |
к |
|||||
образованию барбитала: |
|
|
|
|
|
|
||||
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HN |
|
|
С2H5 |
десульфирование |
|
|
|
C2H5 |
|
|
|
|
C2H5 |
|
HN |
|
|
C2H5 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||
S |
NH |
|
O |
|
O |
NH |
|
O |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
тиобарбитал |
|
барбитал |
|
|
||||||
Тем же путём в организме десульфируются тиофосфорорганические инсектициды. В результате
образуются |
|
токсичные |
|
соединения, |
ингибиторы |
|||
холинэстеразы. |
|
|
|
|
|
|
||
Окислительное дегалогенирование |
|
|||||||
Многие |
|
галогенопроизводные |
углеводородов – |
|||||
инсектициды, |
пестициды, |
средства |
для |
общей |
||||
анестезии, |
|
растворители |
– |
|
подвергаются |
|||
биотрансформации |
путём |
|
окислительного |
|||||
дегалогенирования. |
Реакция |
|
катализируется |
|||||
цитохромом |
|
P450. |
Промежуточными |
продуктами |
||||
являются |
гем-галогеногидрины, |
|
которые |
затем |
||||
отщепляют |
|
галогеноводород, |
|
|
образуя |
|||
карбонилсодержащие соединения – альдегиды, кетоны, ацилгалогениды. Гем-тригалогенопроизводные дегалогенируются легче, чем ди- и моногалогенопроизводные. Галогенангидриды кислот являются очень реакционноспособными соединениями и могут дальше реагировать с водой, образуя
карбоновые кислоты, |
или |
с белками тканей. |
||
Например, |
фторотан |
может |
метаболизироваться |
|
следующим образом: |
|
|
||
Cl |
|
Cl |
|
|
| |
CYP450 |
| |
-HBr |
O |
CF3-C-H |
|
CF3-C-OH |
|
CF3-C |
| |
|
| |
|
Cl |
Br |
|
Br |
|
|
белок |
H2O |
CF3-CO-NH-белок |
CF3COOH |
|
трифторуксусная |
|
кислота |
29

Сходным образом протекает окислительное дегалогенирование левомицетина:
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O2N |
|
|
|
CH-CH-NH-CO-CHCl2 |
O2N |
|
|
|
CH-CH-NH-CO-C-Cl |
||
|
|
| | |
|
|
|
| | |
| |
||||
|
|
|
|
|
|||||||
|
|
|
|
OH CH2-OH |
|
|
|
|
|
OH CH2-OH |
OH |
|
|
|
|
левомицетин |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
||
|
|
|
|
|
|
|
|
|
|
-HCl |
|
R-NH-CO-CO-NH-белок |
белок |
|
|
|
R-NH-CO-COCl |
|
|||||
|
|
|
|
|
|
|
|
|
|
производное |
|
оксалилхлорида
H2O
R-NH-CO-COOH
производное оксаминовой кислоты
Реакции восстановления
Кроме окислительной системы в микросомах печени содержатся ферменты редуктазы, которые катализируют восстановление азо- и нитросоединений до первичных аминов.
Ароматические нитросоединения вначале восстанавливаются в нитрозосоединения, производные гидроксиламина, а затем в ароматические амины:
Ar-NO2 |
Ar-N=O |
Ar-NH-OH |
Ar-NH2 |
нитро- |
нитрозо- |
гидроксиламин |
амин |
соединение |
соединение |
|
|
Таким образом происходит, например, восстановление нитразепама в его 7-аминометаболит:
|
HN |
O |
|
HN |
O |
|
|
|
|
||
|
|
|
редуктаза |
|
|
O2N |
|
N |
H2N |
|
N |
нитразепам |
7-аминометаболит |
Восстановление азосоединений протекает через стадию образования гидразосоединений, затем NH-NH-
30
